
| A. | 該溫度下此反應的平衡常數K=400 | |
| B. | 其他條件不變,再充入0.3mol SO2和0.2mol O2平衡時,SO2的體積分數增大 | |
| C. | 平衡時,SO2的轉化率為95% | |
| D. | 前2min SO2的平均反應速率0.02mol/(L•s) |
分析 依據化學平衡三段式列式計算,設二氧化硫轉化物質的量為x,則
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
變化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
氣體物質的量之比和氣體壓強之比,以此解答該題.
解答 解:在500℃時,把0.3mol SO2和0.2mol O2充入一個體積為10L并盛有V2O5(催化劑)的真空密閉容器中,保持溫度不變,經2min后,容器內的壓強不再變化,此時容器內壓強減小20%,設二氧化硫轉化物質的量為x,則
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
變化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
容器內的壓強不再變化,此時容器內壓強減小20%,即氣體物質的量減少20%,得到(0.3+0.2)×(1-20%)=0.3-x+0.2-0.5x+x,
x=0.20mol,
A.該溫度下此反應的平衡常數K=$\frac{(\frac{0.2mol}{10L})^{2}}{(\frac{0.1mol}{10L})^{2}(\frac{0.1mol}{10L})}$=400,故A正確;
B.其他條件不變,再充入0.3mol SO2和0.2mol O2平衡時,相當于在原來基礎上增大壓強,平衡正向移動,則SO2的體積分數減小,故B錯誤;
C.平衡時,SO2的轉化率為$\frac{0.2mol}{0.3mol}×100%$=66.7%,故C錯誤;
D.前2min SO2的平均反應速率為$\frac{\frac{0.2mol}{10L}}{2min}$=0.01mol/(L•s),故D錯誤.
故選A.
點評 本題考查了化學平衡常數、化學反應速率的計算及化學平衡的影響因素等知識,題目難度中等,試題涉及的知識面廣,應加強平時知識的積累,試題有利于培養學生靈活應用所學知識的能力.


 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案科目:高中化學 來源: 題型:選擇題
| A. | 126C和146C是2種核素,他們互稱同位素 | |
| B. | 近期化學研究者開發出被稱為第五形態的固體碳,這種新的碳結構稱作“納米泡沫”,它外形類似海綿,比重極小,并具有磁性.納米泡沫碳與C60互稱同素異形體 | |
| C. |  與 與 互為同分異構體 互為同分異構體 | |
| D. | 硝基苯可看成是由  和-NO2兩種基團組成 和-NO2兩種基團組成 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
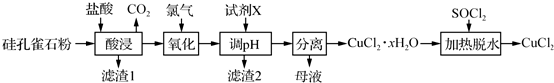
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:實驗題


查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
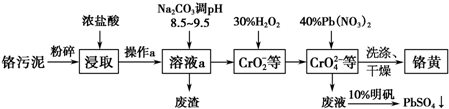
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
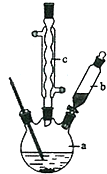 苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線:
苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線: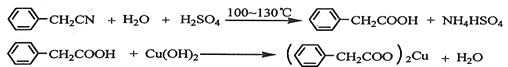
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤ | B. | ①④⑤ | C. | ②③④ | D. | ②④⑤ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com