
| 實驗方案 | 實驗操作 | 實驗現象 | 結論 |
| 方案1 | 取少量白色物質于試管中,加入適量水,振蕩,樣品全部溶于水,向其中加入無色酚酞試液 | 溶液變成紅色 | 白色物質為Na2O |
| 方案2 | ①取少量白色物質于試管中,加入適量水,振蕩,樣品全部溶于水,向其中加入過量的CaCl2溶液. ②靜置片刻,取上層清液于試管中,滴加無色酚酞試液 | ①出現白色沉淀. ②無明顯現象 | 白色物質為Na2CO3 |
分析 (1)Mg與二氧化碳反應生成MgO和C;
(2)加入無色酚酞試液,溶液變紅,可知溶液顯堿性;
(3)鈉在二氧化碳中,瓶底有黑色顆粒為C,瓶壁上附著白色物質,由實驗可知為碳酸鈉,則燃燒生成碳酸鈉和C;
(4)結合元素守恒可知,反應前后沒有H元素.
解答 解:(1)Mg與二氧化碳反應生成MgO和C,反應為2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C,故答案為:2Mg+CO2$\frac{\underline{\;點燃\;}}{\;}$2MgO+C;
(2)甲同學認為方案1得到的結論不正確,其理由是因為碳酸鈉水解生成的氫氧化鈉使溶液呈堿性,也能使酚酞試液變紅色,
故答案為:因為碳酸鈉水解生成的氫氧化鈉使溶液呈堿性,也能使酚酞試液變紅色;
(3)鈉在二氧化碳中,瓶底有黑色顆粒為C,瓶壁上附著白色物質,由實驗可知為碳酸鈉,則燃燒生成碳酸鈉和C,反應為4Na+3CO2$\frac{\underline{\;點燃\;}}{\;}$2Na2CO3+C,
故答案為:4Na+3CO2$\frac{\underline{\;點燃\;}}{\;}$2Na2CO3+C;
(4)由質量守恒定律可知,反應物是鈉和二氧化碳,僅三種元素,沒有氫元素,則結論不同意,故答案為:不同意,反應物是鈉和二氧化碳,僅三種元素,沒有氫元素.
點評 本題考查物質的鑒別及檢驗,為高頻考點,把握物質的性質、發生的反應及實驗現象與結論為解答的關鍵,側重分析與實驗能力的考查,題目難度不大.


 心算口算巧算一課一練系列答案
心算口算巧算一課一練系列答案 應用題作業本系列答案
應用題作業本系列答案科目:高中化學 來源: 題型:解答題
 E的氫化物的電子式
E的氫化物的電子式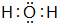 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①<②<③<④<⑤ | B. | ④<②<①<③<⑤ | C. | ②<④<③<①<⑤ | D. | ②<④<①<③<⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
. .
. .
. 合成D 的路線流程圖(其他原料任選)合成
合成D 的路線流程圖(其他原料任選)合成查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2Na2O2+2H2O═4NaOH+O2↑ | B. | 3NO2+H2O═2HNO3+NO | ||
| C. | CO+H2O$\frac{\underline{\;高溫\;}}{\;}$CO2+H2 | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 堿式碳酸銅是一種具有廣泛用途的化工產品,主要用于固體熒光粉激活劑和銅鹽的制造等.
堿式碳酸銅是一種具有廣泛用途的化工產品,主要用于固體熒光粉激活劑和銅鹽的制造等.| 實驗序號 | 樣品質量/g | CO2體積/mL(已折算成標準狀況下) |
| 1 | 0.542 | 44.82 |
| 2 | 0.542 | 44.80 |
| 3 | 0.542 | 44.78 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com