
【題目】下列水解反應離子方程式書寫正確的是( )
A.CH3COOH+OH﹣CH3COO﹣+H2O
B.S2﹣+2H2OH2S+2OH﹣
C.CH3COOH+H2OCH3COO﹣+H3O+
D.CO32﹣+H2OHCO3﹣+OH﹣
科目:高中化學 來源: 題型:
【題目】【化學—選修3:物質結構與性質】銅、硼、硅、砷等元素的化合物是制造新型激光武器和新型太陽能電池的重要材料。回答下列問題:
(1)基態硅(2814Si)原子中,電子占據的最高能層的軌道數有______個。
(2)已知:藍色晶體(CuSO4·5H2O)![]() 天藍色溶液
天藍色溶液![]() 深藍色溶液
深藍色溶液![]() 深藍色晶體
深藍色晶體
①藍色晶體中陰離子的空間構型是_________;
②天藍色溶液中的陽離子是_____,其配體中心原子的雜化軌道類型是________;
③24.6g深藍色晶體(其摩爾質量為246g.mol-1)中配離子含有的σ鍵數是_____;
④實驗測得無水乙醇易溶于水,其原因是______________。
(3)砷化鎵是具有空間網狀結構的晶體,熔點為1230℃,是優良的第三代半導體材料。
①砷化鎵屬于________晶體。已知氮化硼與砷化鎵屬于同種晶體類型。則兩種晶體熔點較高的是_____(填化學式),其理由是_________。上述兩種晶體中的四種元素電負性最小的是_______(填元素符號)。
②砷化鎵晶胞結構如圖所示。其晶胞邊長為a pm,密度為_______g.cm-3。(砷化鎵的摩爾質量為M g.mol-1,阿伏伽德羅常數為NA)
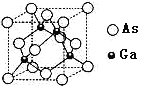
【答案】 9 四面體 [Cu(H2O)4]2+ sp3 1.6NA 乙醇分子與水分子間存在氫鍵,乙醇分子和水分子都是極性分子 原子晶體 BN 二者均為原子晶體,B、N間的鍵長比Ga、As的鍵長短,鍵能大 Ga 4Mx1030/a3NA
【解析】(1)基態硅(2814Si)原子核外電子數為14,基態原子核外電子排布為1s22s22p63s23p2,電子占據的最高能層符號為M,該能層具有的原子軌道數為1+3+5=9;(2)①藍色晶體CuSO4·5H2O中陰離子SO42-,根據價層電子對互斥理論,價層電子對個數=σ鍵+孤電子對個數,SO42-中中心原子S的價層電子對為![]() =4,孤電子對數為
=4,孤電子對數為![]() =0,不含孤電子對,所以空間構型是正四面體結構;②藍色晶體溶于水得到天藍色溶液中的陽離子是[Cu(H2O)4]2+;其配體H2O中心原子O原子雜化軌道數為
=0,不含孤電子對,所以空間構型是正四面體結構;②藍色晶體溶于水得到天藍色溶液中的陽離子是[Cu(H2O)4]2+;其配體H2O中心原子O原子雜化軌道數為![]() =4,,采取sp3雜化方式;③每個配離子[Cu(NH3)4]2+含有的σ鍵數是3×4+4=16,故24.6g深藍色晶體{[Cu(NH3)4]SO4H2O }為0.1mol,其中配離子[Cu(NH3)4]2+含有的σ鍵數是0.1mol×16×NA mol-1=1.6NA;④乙醇分子與水分子間存在氫鍵,乙醇分子和水分子都是極性分子,故無水乙醇易溶于水;(3)①砷化鎵是具有空間網狀結構的晶體,熔點為1230℃,是優良的第三代半導體材料,與晶體硅相似,故砷化鎵屬于原子晶體;氮化硼與砷化鎵都屬于原子晶體,B、N間的鍵長比Ga、As的鍵長短,鍵能大,故BN晶體熔點較高;非金屬性越強,電負性越強,則B、N、Ga、As四種元素電負性最小的Ga;②一個晶胞中含有As 8×
=4,,采取sp3雜化方式;③每個配離子[Cu(NH3)4]2+含有的σ鍵數是3×4+4=16,故24.6g深藍色晶體{[Cu(NH3)4]SO4H2O }為0.1mol,其中配離子[Cu(NH3)4]2+含有的σ鍵數是0.1mol×16×NA mol-1=1.6NA;④乙醇分子與水分子間存在氫鍵,乙醇分子和水分子都是極性分子,故無水乙醇易溶于水;(3)①砷化鎵是具有空間網狀結構的晶體,熔點為1230℃,是優良的第三代半導體材料,與晶體硅相似,故砷化鎵屬于原子晶體;氮化硼與砷化鎵都屬于原子晶體,B、N間的鍵長比Ga、As的鍵長短,鍵能大,故BN晶體熔點較高;非金屬性越強,電負性越強,則B、N、Ga、As四種元素電負性最小的Ga;②一個晶胞中含有As 8×![]() +6×
+6×![]() =4個,Ga在內部,共4個,即一個晶胞中含有4個砷化鎵,其晶胞邊長為apm=a×10-10cm,V=a3×10-30cm3,密度為
=4個,Ga在內部,共4個,即一個晶胞中含有4個砷化鎵,其晶胞邊長為apm=a×10-10cm,V=a3×10-30cm3,密度為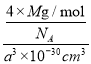 =
=![]() 。
。
點睛:本題考查了方程式的書寫、分子空間構型以及雜化類型的判斷、晶胞密度計算等知識,題目難度較大,注意相關基礎的把握和方法的積累。先根據分攤法計算每個晶胞含有多少個原子,再根據晶胞的邊長,確定晶胞的體積,再根據ρ=![]() 計算密度。
計算密度。
【題型】綜合題
【結束】
12
【題目】【化學—選修5:有機化學基礎】PVB是重要的建筑材料。其合成路線如下(部分反應條件和產物略去)。
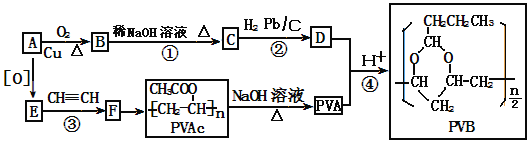
已知:
Ⅰ.A分子式為C2H6O,其核磁共振氫譜圖顯示有三個波峰。
![]()
Ⅲ. ![]()
回答下列問題:
(1)A的結構簡式_______,B→C的反應類型有加成反應和_______,D的官能團為_______。
(2)PVAC的名稱是___________(3)C分子中最多有_____個原子共平面。
(3)E→F的反應方程式為_____________。
(4)已知-OH直接連在不飽和C原子上不穩定,會自動發生分子內重排形成-CHO。則D的同分異構體中能與金屬Na反應產生H2的有____種。
(5)以溴乙烷為原料制備丁醛(其他無機試劑任選),其流程圖為_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】堿性電池具有容量大、放電電流大的特點,因而得到廣泛應用。
鋅—錳堿性電池以氫氧化鉀溶液為電解液,電池總反應式為:Zn(s)+2MnO2(s)+H2O(l)==Zn(OH)2(s)+Mn2O3(s),
下列說法錯誤的是( )
A. 電池工作時,鋅失去電子
B. 電池工作時,電子由負極通過外電路流向正極
C. 電池正極的電極反應式為:2MnO2(s)+H2O(1)+2e-=Mn2O3(s)+2OH-(aq)
D. 外電路中每通過0.4mol電子,鋅的質量理論上減小6.5g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為一原電池的結構示意圖,下列說法中,錯誤的是( ) 
A.Cu電極為正電極
B.原電池工作時,電子從Zn電極流出
C.原電池工作時的總反應為:Zn+Cu2+=Zn2++Cu
D.鹽橋(瓊脂﹣飽和KCl溶液)中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】火力發電在我國的能源利用中占較大比重,但是排放出的SO2會造成一系列環境和生態問題,直接排放含SO2的煙氣會形成酸雨,危害環境.
(1)用化學方程式表示SO2形成硫酸型酸雨的反應: .
(2)工業上用Na2SO3溶液吸收煙氣中的SO2 . 將煙氣通入1.0molL﹣1的Na2SO3溶液,溶液pH不斷減小.當溶液pH約為6時,吸收SO2的能力顯著下降,應更換吸收劑. ①此時溶液中c(SO32﹣)的濃度是0.2molL﹣1 , 則溶液中c(HSO3﹣)是molL﹣1 .
②向pH約為6的吸收劑中通入足量的O2 , 可將其中的NaHSO3轉化為兩種物質,反應的化學方程式是 .
③某研究小組為探究提高含硫煙氣中SO2的吸收效率的措施,模擬實驗吸收含硫煙氣,實驗結果如圖所示.則: , 有利于提高SO2的吸收效率.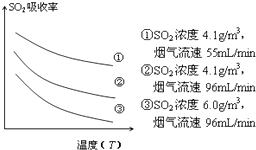
(3)工廠倉庫存放的Na2SO3藥品已部分被空氣氧化,該化學小組想用已知濃度的酸性KMnO4溶液來確定其含量,具體步驟如下: 步驟i稱取樣品1.000g.
步驟ii將樣品溶解后,完全轉移到250mL容量瓶中,定容,充分搖勻.
步驟iii移取25.00mL樣品溶液于250mL錐形瓶中,用0.01000molL﹣1 KMnO4標準溶液滴定至終點.
按上述操作方法再重復2次.
①寫出步驟iii所發生反應的離子方程式;
②在配制0.01000molL﹣1 KMnO4溶液時若仰視定容,則最終測得藥品中Na2SO3的含量(填“偏大”、“偏小”或“無影響”).
③某同學設計用下列儀器進行滴定實驗(夾持部分略去),最合理的組合是(填字母).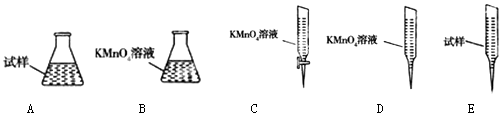
④滴定結果如下表所示:
滴定次數 | 待測溶液的體積/mL | 標準溶液的體積 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 2.20 | 20.20 |
則該藥品中Na2SO3的質量分數為 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【選修3:物質結構與性質】銅元素可形成多種重要化合物。回答下列問題:
(1)銅元素位于元素周期表中的_____區,其基態原子的價電子排布圖為_________。
(2)往硫酸銅溶液中加入過量氨水,可形成[Cu(NH3)4]SO4溶液,該溶液可用于溶解纖維素。
①[Cu(NH3)4]SO4中陰離子的立體構型是__________。
②在[Cu(NH3)4]SO4中,Cu2+與NH3之間形成的化學鍵稱為______,提供孤電子對的成鍵原子是_________。
③除硫元素外,[Cu(NH3)4]SO4中所含元素的電負性由小到大的順序為________。
④NF3與NH3的空間構型相同,中心原子的軌道雜化類型均為_________。但NF3不易與Cu2+形成化學鍵,其原因是_______________。
(3)一種Hg-Ba-Cu-O高溫超導材料的晶胞(長方體)如圖所示。

①該物質的化學式為__________。
②已知該晶胞中兩個Ba2+的間距為cpm.則距離Ba2+最近的Hg+數目為_____個,二者的最短距離為_______pm。(列出計算式即可,下同)
③設該物質的摩爾質量為M,阿伏加德羅常數的值為NA,則該晶體的密度為______g·cm-3。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏伽德羅常數的值,下列說法中正確的是( )
A.常溫常壓下,22.4 L乙烯中含C﹣H鍵的數目為4NA
B.1molFe與足量鹽酸反應轉移電子數為3NA
C.1.6g由氧氣和臭氧組成的混合物中含有的氧原子數目為0.1NA
D.向1L 1 molL﹣1氯化鋁溶液中加入足量的氨水,生成AlO2﹣的個數為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SO2是大氣污染物之一,為探究SO2氣體的性質,某實驗小組利用如圖1所示裝置進行實驗。
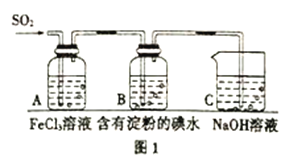
(1)裝置A中發生反應的離子方程式為:______________;
(2)裝置C的作用是:______________;
(3)在上述裝置中通入過量的SO2,為了驗證A 中SO2 與Fe3+發生了氧化還原反應,取A 中的溶液少 量,分成兩份,并設計了如下實驗方案:
方案①:向第一份溶液中加入少量酸性KMnO4溶液,發現紫紅色褪去;
方案②,向第二份溶液中加入少量KSCN 溶液,發現不變紅,再加入少量新制的氯水,深液變紅;
上述方案中不合理的是:________,原因是: ________________;
(4)能表明I-的還原性弱于SO2 的現象是: ________________;
(5)設計實驗驗證反應結束后A 裝置中的Cl-:________________;
(6) 該小組同學設計實驗模報測定硫酸工業生產排放的尾氣中SO2的體積分數(其他氣體均難溶于水且不發生任何反應),選用了如圖2所示的簡易實驗裝置。
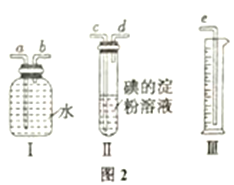
①若混合氣體的流向按從左向右時,右圖裝置組裝連接的順序合理的是:混合氣體→A (填寫a、b等儀器接口字母)。___________
②你認為下列試劑中,可以用來代替試管中碘的淀粉溶液的是:______ (填標號);
A.酸性KMnO4溶液 B.NaOH 溶液 C.溴水 D.氨水
③若碘溶液的濃度為0.05 mol/L、體積為30 mL,與SO2氣體恰好完全反應時,量簡內水的體積為386.4 mL(已折算為標準狀況下的體積)。則SO2的體積分數為:_______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如圖為元素周期表前四周期的一部分,下列有關R、W、X、Y、Z五種元素的敘述中,正確的是
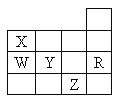
A. 常溫常壓下五種元素的單質中Z單質的沸點最高
B. Y、Z的陰離子電子層結構都與R原子相同
C. W的氫化物的熱穩定性比X的氫化物的熱穩定性高
D. Y元素的非金屬性比W元素的非金屬性強
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com