
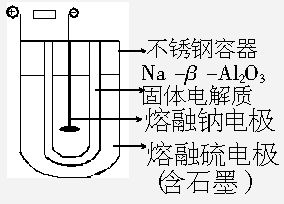
 作無噪音、無污染、價廉、安全、使用壽命長以及維修費用低等特點。常用的電池是由液體電解質將兩個固體電極隔開,而Na-S電池正好相反,它是由固體電解質將兩個液體電極隔開:一個由Na-β-Al2O3固體電解質做成的中心管,將內室的熔融鈉(熔點98℃)和外室的熔融硫(熔點113℃)隔開,并允許電子通過。整個裝置密封于不銹鋼容器內,此容器又兼作硫電極的集流器。在電池內部,電子穿過固體電解質和硫反應從而傳遞電流。350℃時,Na-S電池的斷路電壓為2.08V。已知該硫的化學式為S8,在外電路中被還原成多硫離子。
作無噪音、無污染、價廉、安全、使用壽命長以及維修費用低等特點。常用的電池是由液體電解質將兩個固體電極隔開,而Na-S電池正好相反,它是由固體電解質將兩個液體電極隔開:一個由Na-β-Al2O3固體電解質做成的中心管,將內室的熔融鈉(熔點98℃)和外室的熔融硫(熔點113℃)隔開,并允許電子通過。整個裝置密封于不銹鋼容器內,此容器又兼作硫電極的集流器。在電池內部,電子穿過固體電解質和硫反應從而傳遞電流。350℃時,Na-S電池的斷路電壓為2.08V。已知該硫的化學式為S8,在外電路中被還原成多硫離子。見解析
解析:本題考查了蓄電池的一些性質,充電時電能轉化為化學能,可看作電解池;放電時化學能轉化為電能,可看作原電池。在充、放電的過程中,反應物和產物可以相互轉化。
(1)高溫下,鈉與硫均為熔融態,因此Na-S電池充、放電時的化學方程式為: Na2Sn 2Na (l) +
2Na (l) +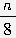 S8(l)。
S8(l)。
(2)Na-S電池放電時為原電池,失電子發生氧化反應的為負極,得電子發生還原反應的為正極,因此放電時,Na為負極:16Na-16e-=16Na+,S為正極:nS8+16e-= 。
。
(3)內室的熔融鈉放出電子,通過外電路將硫還原成多硫離子 ,但由于硫是絕緣體,故在外室填充多孔石墨增強導電性,以保證有效導電。
(4)由于Na-S電池在350℃時的斷路電壓為2.08V,即電池的電動勢為2.08V,故可以用電壓表測定Na-S電池的電動勢。即放電時,電動勢降至某額定限量即停止放電;充電時,電動勢升至某額定限量(2.08V)即停止充電。


科目:高中化學 來源: 題型:
.以氨氣代替氫氣來研發氨燃料電池是當前科研的一個熱點。氨燃料電池使用的電解質溶液是KOH溶液,電池反應為:
有關下列說法錯誤的是( )
A.氨燃料電池在放電時,氨氣被氧化
B.氨燃料電池在放電時,正極反應為:2NH3+6e-+6OH- N2+6H2O
C.以氨氣代替氫氣的主要原因是:氨氣易液化易儲存
D.燃料電池的能量轉化率一般比普通的電池高
查看答案和解析>>
科目:高中化學 來源:2013-2014學年山東省德州市高三上學期期末考試化學試卷(解析版) 題型:填空題
碳和氮的許多化合物在工農業生產和生活中有重要的作用。
(1)工業上生產硝酸所需要的一氧化氮常用氨氣來制備,該反應的化學方程式為 ?????????????????????????????????????????????????????????????????? 。
(2)以CO2與NH3為原料可合成化肥尿素[化學式為CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2 NH4(s)??? ? △H=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)? △H=+116.5 kJ·mol-1
③H2O(1)=H2O(g)? ??????????????????? △H=+44.0kJ·mol-1
寫出CO2與NH3合成尿素和液態水的熱化學反應方程式?????????????????
(3)以氨氣代替氫氣研發氨燃料電池是當前科研的一個熱點,已知氨燃料電池使用的電解質溶液是2mol·L-1的KOH溶液,電池反應為:4NH3+3O2=2N2+6H2O。該電池負極的電極反應式為??????????????? ;每消耗3.4g NH3轉移的電子數為??????????????? (阿伏加德羅常數的值用NA表示)。
(4)用活性炭還原法可以處理氮氧化物。某研究小組向某密閉容器加入一定量的活性炭和NO,發生反應C(s)+2NO(g) N2(g)+CO2(g)? △H=Q kJ·mol-1。
N2(g)+CO2(g)? △H=Q kJ·mol-1。
在T1℃時,反應進行到不同時間測得各物質的濃度如下:
???????? 時間(Min) 濃度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃時,該反應的平衡常數K= ????? ;
②30min后,只改變某一條件,反應重新達到平衡,根據上表中的數據判斷改變的條件可能是? ?? ? (填字母編號)。
a.加入一定量的活性炭 ???? b.通人一定量的NO
c.適當縮小容器的體積?????? d.加入合適的催化劑
③若30min后升高溫度至T2℃,達到平衡時,容器中NO、N2、CO2的濃度之比為5:3:3,則Q ??? 0(填“>”或“<”)。?
查看答案和解析>>
科目:高中化學 來源:2014屆河北省高一下學期三調考試化學試卷(解析版) 題型:選擇題
.以氨氣代替氫氣來研發氨燃料電池是當前科研的一個熱點。氨燃料電池使用的電解質溶液是KOH溶液,電池反應為:
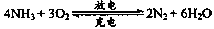
有關下列說法錯誤的是( )
A.氨燃料電池在放電時,氨氣被氧化
B.氨燃料電池在放電時,正極反應為:2NH3+6e-+6OH-
N2+6H2O
C.以氨氣代替氫氣的主要原因是:氨氣易液化易儲存
D.燃料電池的能量轉化率一般比普通的電池高
查看答案和解析>>
科目:高中化學 來源:2011-2012學年安徽省高三第一次統考理科綜合試卷化學部分(解析版) 題型:選擇題
以氨氣代替氫氣來研發氨燃料電池是當前科研的一個熱點。氨燃料電池使用的電解質溶液是KOH溶液,電池反應為:
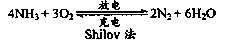
有關下列說法錯誤的是( )
A.氨燃料電池在充電時,OH-向電池的負極移動
B.氨燃料電池在放電時,負極反應為:2NH3-6e-+6OH-
N2+6H2O
C.以氨氣代替氫氣的主要原因是:氨氣易液化易儲存
D.燃料電池的能量轉化率一般比普通的電池高
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com