
【題目】近年科學家提出“綠色自由”構想。把含有大量CO2的空氣吹入K2CO3溶液中,再把CO2從溶液中提取出來,并使之與H2反應生成可再生能源甲醇。其工藝流程如圖所示:
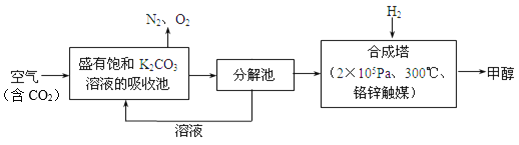
(1)分解池中主要物質是_______________。
(2)在合成塔中,若有4400 g CO2與足量H2反應,生成氣態的H2O和甲醇,可放出5370 kJ的熱量,寫出該反應的熱化學方程式_______________。
(3)該工藝在哪些方面體現了“綠色自由”構想中的“綠色”_______________。
(4)一定條件下,往2L恒容密閉容器中充入1 mol CO2和3 mol H2,在不同催化劑作用下發生反應I、反應II與反應III,相同時間內CO2的轉化率隨溫度變化如下圖所示:
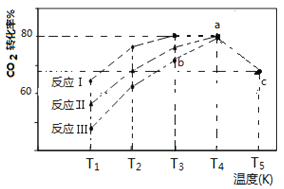
(圖中c點的轉化率為66.67%,即轉化了2/3)
①催化劑效果最佳的反應是________(填“反應I”,“反應II”,“反應III”)。
②b點v (正)_________v (逆)(填 “>”, “<”, “=”)。
③若此反應在a點時已達平衡狀態,a點的轉化率比c點高的原因是____________。
④c點時該反應的平衡常數K =____________________。
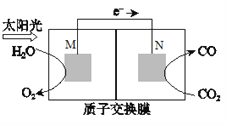
(5)科學家還研究了其它轉化溫室氣體的方法,利用下圖所示裝置可以將CO2轉化為氣體燃料CO。該裝置工作時,N電極的電極反應式為_______________。
【答案】 KHCO3(或碳酸氫鉀) CO2(g)+ 3H2(g)![]() H2O(g)+ CH3OH(g) △H=== -53.7kJ/mol 減少大氣中CO2并產生清潔能源甲醇;K2CO3可循環使用;能量可以循環利用,低碳經濟等。 反應I > 該反應為放熱反應,溫度升高,平衡逆向移動 K=16/3 (或K=3.70) CO2+2H++2e-===CO +H2O
H2O(g)+ CH3OH(g) △H=== -53.7kJ/mol 減少大氣中CO2并產生清潔能源甲醇;K2CO3可循環使用;能量可以循環利用,低碳經濟等。 反應I > 該反應為放熱反應,溫度升高,平衡逆向移動 K=16/3 (或K=3.70) CO2+2H++2e-===CO +H2O
【解析】(1)把含有大量CO2的空氣吹入K2CO3溶液中,碳酸鉀與二氧化碳和水反應生成碳酸氫鉀進入到分解池中,故分解池中的主要物質是碳酸氫鉀;
(2)根據4400gCO2與足量H2反應,可放出5370 kJ的熱量,則1molCO2與H2合成甲醇放出熱量為53.70kJ,所以熱化學方程式為CO2(g)+ 3H2(g)![]() H2O(g)+ CH3OH(g) △H=== -53.7kJ/mol;
H2O(g)+ CH3OH(g) △H=== -53.7kJ/mol;
(3)“綠色自由”構想流程中常包括物質的“循環利用”,上述流程中能體現“循環利用”的“綠色”有減少大氣中CO2并產生清潔能源甲醇;K2CO3可循環使用;能量可以循環利用,低碳經濟等;
(4)①根據圖中信息可知,在相同溫度下,反應I的CO2的轉化率最高,故其催化劑效果最佳;②a點時達到平衡,故b點時反應往正方向進行,v (正)>v (逆);③若此反應在a點時已達平衡狀態,a點的轉化率比c點高的原因是:該反應為放熱反應,溫度升高,平衡逆向移動,故a點的轉化率比c點高;
④往2L恒容密閉容器中充入1 mol CO2和3 mol H2,
CO2(g)+ 3H2(g)![]() H2O(g)+ CH3OH(g)
H2O(g)+ CH3OH(g)
開始時的濃度/mol 0.5 1.5 0 0
改變的濃度/mol 0.5×![]() 1.5×
1.5×![]() 0.5×
0.5×![]() 0.5×
0.5×![]()
平衡時的濃度/mol 0.5×![]() 1.5×
1.5×![]() 0.5×
0.5×![]() 0.5×
0.5×![]()
K=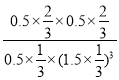 =
=![]() =3.70;
=3.70;
(5)根據圖中信息可知,電子從M電極流向N電極,CO2得電子轉化為CO,則N電極的電極反應式為:CO2+2H++2e-=CO +H2O。


科目:高中化學 來源: 題型:
【題目】實驗室用H2還原WO3制備金屬W的裝置如圖所示(Zn粒中往往含有硫等雜質,焦性沒食子酸溶液用于吸收少量氧氣, KMnO4可用于吸收H2S),下列說法正確的是

A. ①、②、③中依次盛裝KMnO4溶液、濃H2SO4、焦性沒食子酸溶液
B. 管式爐加熱前,用試管在④處收集氣體并點燃,通過聲音判斷氣體純度
C. 結束反應時,先關閉活塞K,再停止加熱
D. 裝置Q(啟普發生器)也可用于二氧化錳與過氧化氫反應制備氧氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列過程涉及化學變化的是( )
A. 將I2溶于酒精制備碘酊
B. 將NaCl溶于水中制備生理鹽水
C. 被果汁沾污的衣服浸入漂白液中清洗
D. 用激光筆照射雞蛋清溶液產生丁達爾效應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液組成的混合溶液中,部分離子的濃度如圖所示。
(1)混合液中,NaCl的物質的量為_______mol,MgCl2的質量為_______g。
(2)該混合溶液中CuCl2的物質的量濃度為_____molL﹣1,將該混合溶液加水稀釋至體積為1 L,稀釋后溶液中Cu2+的物質的量濃度為_______molL﹣1。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】A、B、C是由H、O、Na三種元素中的兩種或三種組成的化合物。甲、乙、丙是三種單質,分別由上述元素組成。上述單質和化合物之間存在如下反應關系:
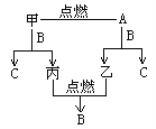
完成下列空白:
(1)B的分子式____________。
(2)寫出甲+B→C+丙的化學方程式_______________________________。
(3)用脫脂棉花包住約0.2g A的粉末,置于石棉網上,往脫脂棉花上滴水,可觀察到脫脂棉花劇烈燃燒起來。
①由實驗現象所得出的有關A和H2O反應的結論是___________(填代號)。
a.反應放熱 b.棉花在空氣中可以自燃
c.有O2生成 d.A在空氣中可以自燃
②寫出A和H2O反應的化學方程式_____________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種瑞香素的衍生物的結構簡式如圖,下列有關該有機物性質的說法正確的是

A. 能與FeCl3溶液發生顯色反應
B. 1 mol該有機物最多可與3 mol H2加成
C. 1 mol該有機物最多可與含4 molNaOH溶液反應
D. 1 mol該有機物與足量NaHCO3溶液反應可放出3 mol CO2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質A有如圖所示的轉化關系(部分產物已略去),已知H能使溴的CCl4溶液褪色。
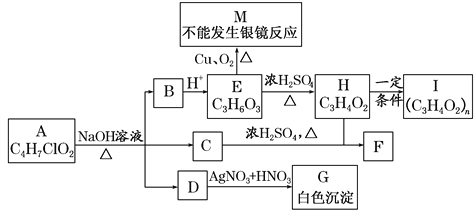
回答下列問題:
(1)A的結構簡式為________。
(2)1 mol E與足量NaOH溶液反應時,消耗NaOH的物質的量為________mol。
(3)M的某些同分異構體能發生銀鏡反應,寫出其中任意一種結構簡式:________________。
(4)寫出化學方程式H―→I:__________________________________。
(5)E通常可由丙烯、NaOH溶液、H2、O2、Br2等為原料合成,請按“A―→B―→C―→…”的形式寫出反應流程,并在“―→”上注明反應類型但不需要注明試劑及反應條件________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯化芐(C6H5CH2Cl)是一種重要的有機化工原料。工業上采用甲苯與干燥氯氣在光照條件下反應合成氯化芐。
(1)寫出甲苯與干燥氯氣在光照條件下反應合成氯化芐的化學方程式________________。
(2)用下列方法分析氯化芐粗產品的純度:
步驟I:稱取2.555 g樣品于燒瓶中,加入100.00 mL 4mol/L氫氧化鈉溶液共熱,冷卻至室溫。加入100.00 mL4mol/L硝酸,一段時間后,將燒瓶中的溶液全部轉移至250.00 mL的容量瓶中,加水定容。
步驟II:從容量瓶中各取50.00 mL溶液于三只錐形瓶中,各加入25.00 mL0.2000mol/L硝酸銀溶液。
步驟m:用硫酸鐵銨作指示劑,用0.2000 mol/LNH4SCN溶液分別滴定剩余的硝酸銀,所得滴定數據如下表。
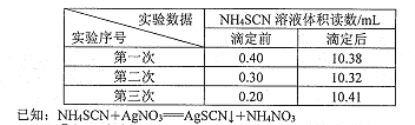
①加入硝酸的目的是____________。
②在步驟III操作中,判斷達到滴定終點的現象是____。
③該樣品中氯化芐的質量分數(寫出計算過程)____。
④上述測定結果通常高于氯化芐中氯元素的理論含量,原因是___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有機物的結構表示不正確的是
A.CH4的球棍模型示意圖為:![]()
B.乙烯的實驗式為:CH2
C.乙醇的結構簡式:C2H5OH
D.2-乙基-1,3-丁二烯分子的鍵線式:![]()
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com