
2013年初,霧霾天氣多次肆虐我國中東部地區。其中,汽車尾氣和燃煤尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示。
2CO2(g)+N2(g)。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線如圖所示。

據此判斷:
①該反應的ΔH________0(填“>”或“<”)
②在T2溫度下,0~2 s內的平均反應速率v(N2)=______________________。
③當固體催化劑的質量一定時,增大其表面積可提高化學反應速率。若催化劑的表面積S1>S2,在上圖中畫出c(CO2)在T1、S2條件下達到平衡過程中的變化曲線。
④若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是________(填代號)。


(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
①煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g)??N2O4(g) ΔH2=-56.9 kJ/mol
寫出CH4(g)催化還原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的熱化學方程式:________________________________________________________________________。
②將燃煤產生的二氧化碳回收利用,可達到低碳排放的
目的。如圖是通過人工光合作用,以CO2和H2O為原料制備HCOOH和O2的原理示意圖。催化劑b表面發生的電極反應式為__________________________。

③常溫下,0.1 mol·L-1的HCOONa溶液pH為10,則HCOOH的電離常數Ka=________。
(1)①<
②0.025 mol·L-1·s-1或0.025 mol/(L·s)
③如圖
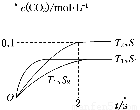
④bd
(2)①CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-810.1 kJ/mol ②CO2+2H++2e-=HCOOH ③10-7mol·L-1
【解析】(1)①由圖中曲線可以看出,在催化劑表面積相同的情況下,T1溫度時先達到平衡,則T1>T2,但溫度高時CO2的濃度小,說明升高溫度平衡逆向移動,該反應的正反應為放熱反應,即ΔH<0。②v(N2)=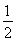 v(CO2)=
v(CO2)=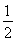 ×
×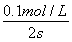 =0.025 mol·L-1·s-1。③溫度相同,質量相同的催化劑,表面積越小反應速率越慢。④a項,只能說明t1時正反應速率最快,但不一定處于平衡狀態;c項,t1時,只能說明n(NO)=n(CO2),不能說明正逆反應速率相等,不是平衡狀態。(2)①根據蓋斯定律,將兩個熱化學方程式相減可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-810.1 kJ/mol。②CO2轉變成HCOOH,碳的化合價降低,CO2被還原,即CO2發生還原反應與H+結合生成HCOOH。(3)甲酸的電離平衡為HCOOH??H++HCOO-,0.1 mol·L-1的HCOONa溶液中存在水解平衡:H2O+HCOO-??HCOOH+OH-,溶液中c(HCOO-)=(0.1-1.0×10-4) mol·L-1,c(H+)=10-10mol·L-1,c(HCOOH)=10-4mol·L-1,故電離平衡常數Ka=
=0.025 mol·L-1·s-1。③溫度相同,質量相同的催化劑,表面積越小反應速率越慢。④a項,只能說明t1時正反應速率最快,但不一定處于平衡狀態;c項,t1時,只能說明n(NO)=n(CO2),不能說明正逆反應速率相等,不是平衡狀態。(2)①根據蓋斯定律,將兩個熱化學方程式相減可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g) ΔH=-810.1 kJ/mol。②CO2轉變成HCOOH,碳的化合價降低,CO2被還原,即CO2發生還原反應與H+結合生成HCOOH。(3)甲酸的電離平衡為HCOOH??H++HCOO-,0.1 mol·L-1的HCOONa溶液中存在水解平衡:H2O+HCOO-??HCOOH+OH-,溶液中c(HCOO-)=(0.1-1.0×10-4) mol·L-1,c(H+)=10-10mol·L-1,c(HCOOH)=10-4mol·L-1,故電離平衡常數Ka=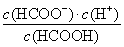 =
=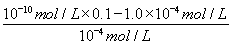 =10-7 mol·L-1。
=10-7 mol·L-1。


科目:高中化學 來源: 題型:閱讀理解

| 催化劑 |
查看答案和解析>>
科目:高中化學 來源:2013屆天津市天津一中高三第四次月考化學試卷(帶解析) 題型:填空題
2013年初,霧霾天氣多次肆虐我國中東部地區。其中,汽車尾氣和燃煤尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為: 。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如右圖所示。
。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如右圖所示。 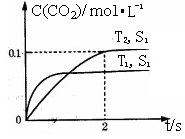
據此判斷:
①該反應的△H 0(填“>”、“<”)。
②在T2溫度下,0~2s內的平均反應速率v(N2)= 。
③當固體催化劑的質量一定時,增大其表面積可提高化學反應速率。若催化劑的表面積S1>S2,在上圖中畫出c(CO2)在T1、S2條件下達到平衡過程中的變化曲線。
④若該反應在恒容的密閉體系中進行,下列示意圖正確且能說明該反應進行到t1時刻達到平衡狀態的是 (填代號) 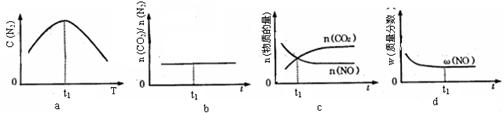
(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
①煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
例如: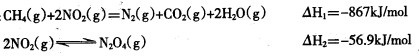
寫出CH4 (g)催化還原N2O4(g)生成N2 (g)和H2O (g)的熱化學方程式 。
②將燃煤產生的二氧化碳回收利用,可達到低碳排放的目的。右圖是通過人工光合作用,以CO2和H2O為原料制備HCOOH和O2的原理示意圖。催化劑b表面發生的電極反應式為 。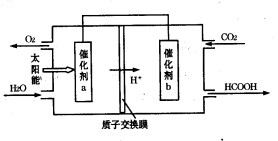
查看答案和解析>>
科目:高中化學 來源:2013-2014學年湖北省高三上學期12月月考化學試卷(解析版) 題型:填空題
Ⅰ、下列實驗操作或對實驗事實的描述正確的是____________________
① 用量筒量取稀硫酸溶液8.0mL;
②中和熱的測定實驗中,可用金屬絲(棒)代替環形攪拌玻璃棒;
③用熱的濃鹽酸洗滌附著有MnO2的試管;
④在硫酸銅晶體結晶水含量的測定中,若加熱后的無水硫酸銅粉末表面發黑,則所測結晶水含量可能會偏高 ;
⑤Fe(OH)3膠體與FeCl3溶液可用過濾的方法分離;
⑥用堿式滴定管量取KMnO4溶液20.50mL ;
⑦將水沿燒杯內壁緩緩注入濃硫酸中,不斷用玻璃棒攪拌以稀釋濃硫酸;
⑧用濕潤的pH試紙測量某溶液pH時,測量值一定比真實值小;
⑨鋅和一定量稀硫酸反應,為加快速率而不影響H2的量可向溶液中加適量Cu(NO3)2晶體。
Ⅱ、2013年初,霧霾天氣多次肆虐天津、北京等地區。其中,燃煤和汽車尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g) + 2CO(g) 2CO2(g)+
N2(g)。△H<0
2CO2(g)+
N2(g)。△H<0
①該反應平衡常數表達式
②若該反應在絕熱、恒容的密閉體系中進行,下列示意圖正確且能說明反應在進行到t1時刻達到平衡狀態的是 (填代號)。


(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) △H=-867 kJ/mol
②2NO2(g)
 N2O4(g) △H=-56.9 kJ/mol
N2O4(g) △H=-56.9 kJ/mol
③H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
寫出CH4催化還原N2O4(g)生成N2和H2O(l)的熱化學方程式: 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年天津市高三第四次月考化學試卷(解析版) 題型:填空題
2013年初,霧霾天氣多次肆虐我國中東部地區。其中,汽車尾氣和燃煤尾氣是造成空氣污染的原因之一。
(1)汽車尾氣凈化的主要原理為: 。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如右圖所示。
。在密閉容器中發生該反應時,c(CO2)隨溫度(T)、催化劑的表面積(S)和時間(t)的變化曲線,如右圖所示。

據此判斷:
①該反應的△H 0(填“>”、“<”)。
②在T2溫度下,0~2s內的平均反應速率v(N2)= 。
③當固體催化劑的質量一定時,增大其表面積可提高化學反應速率。若催化劑的表面積S1>S2,在上圖中畫出c(CO2)在T1、S2條件下達到平衡過程中的變化曲線。
④若該反應在恒容的密閉體系中進行,下列示意圖正確且能說明該反應進行到t1時刻達到平衡狀態的是 (填代號)

(2)直接排放煤燃燒產生的煙氣會引起嚴重的環境問題。
①煤燃燒產生的煙氣含氮的氧化物,用CH4催化還原NOX可以消除氮氧化物的污染。
例如:

寫出CH4 (g)催化還原N2O4(g)生成N2 (g)和H2O (g)的熱化學方程式 。
②將燃煤產生的二氧化碳回收利用,可達到低碳排放的目的。右圖是通過人工光合作用,以CO2和H2O為原料制備HCOOH和O2的原理示意圖。催化劑b表面發生的電極反應式為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com