
| A. | 3p2表示3p能級有兩個軌道 | B. | 原子晶體中可能存在離子鍵 | ||
| C. | 分子晶體中一定存在共價鍵 | D. | sp2雜化軌道模型為 |
分析 A.3p2表示3p能級有兩個電子;
B.原子晶體中只含有共價鍵;
C.單原子分子中沒有共價鍵;
D.sp2雜化軌道是一個s軌道和2個p軌道雜化形成的.
解答 解:A.3p2表示3p能級有兩個電子,而不是兩個軌道,p軌道含有三個軌道,故A錯誤;
B.原子晶體中只含有共價鍵,含有離子鍵的晶體為離子晶體,故B錯誤;
C.單原子分子中沒有共價鍵,如稀有氣體,所以分子晶體中不一定存在共價鍵,故C錯誤;
D.sp2雜化軌道是一個s軌道和2個p軌道雜化形成的,sp2雜化軌道保護三個軌道,其模型為 ,故D正確.
,故D正確.
故選D.
點評 本題考查的知識點較綜合,題目涉及電子排布式、晶體和共價鍵、雜化軌道理論及其應用,題目的難點是雜化軌道理論的有關知識,注意歸納整理和理解,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 碳酸鈣難溶于水,所以碳酸鈣屬于非電解質 | |
| B. | 溶于水能電離出氫離子的化合物都是酸 | |
| C. | 稀硝酸與活潑金屬反應主要放出氫氣,而濃硝酸則使金屬鈍化 | |
| D. | 將鋁箔在酒精燈上加熱至熔化,熔化的鋁并不滴下,這是因為鋁表面的氧化膜保護了鋁 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
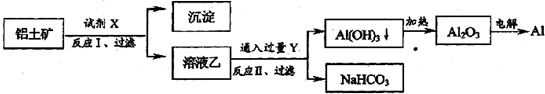
| A. | 試劑X為稀硫酸 | |
| B. | 反應II中生成Al(OH)3的反應為:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- | |
| C. | 結合質子( H+)的能力由強到弱的順序是:OH->HCO3->AlO2- | |
| D. | Al2O3熔點很高,工業上還可采用電解熔融AlCl3冶煉Al |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
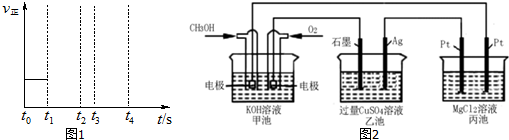
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 摩爾是國際科學界建議采用的一種物理量 | |
| B. | 摩爾是物質的量的單位,簡稱摩,符號為mol | |
| C. | 摩爾可以把物質的宏觀數量與微觀粒子的數量聯系起來 | |
| D. | 國際上規定,12C碳-12原子所含有的碳原子數目的物質的量為1摩 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④⑦ | B. | ②⑤⑦ | C. | ③④⑥ | D. | 全有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba(NO3)2溶液和Na2SO4溶液 | B. | 金屬鈉和MgCl2溶液 | ||
| C. | 金屬鋁和NaOH溶液 | D. | FeCl3溶液和Na2O2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 23gNO2和23gN2O4所含原子數目均為1.5NA | |
| B. | 5.6 g鐵與足量鹽酸反應轉移的電子數為0.3NA | |
| C. | 在常溫常壓下11.2L氯氣所含的原子數目為NA | |
| D. | 高溫下,0.2molFe與足量水蒸氣反應,生成的H2分子數目為0.3NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com