
| A.放出的熱量為(0.4Q1+0.05Q3)KJ | B.放出的熱量為(0.4Q1+0.05Q2)KJ |
| C.△H2 = △H3 | D.△H2 <△H3 |
 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案 沖刺100分單元優化練考卷系列答案
沖刺100分單元優化練考卷系列答案科目:高中化學 來源:不詳 題型:單選題
| A.當溶液中c(CH3COO─)=c(Na+)時,醋酸與氫氧化鈉恰好完全反應 |
| B.當溶液中c(CH3COO─)=c(Na+)時,一定是氫氧化鈉過量 |
| C.當溶液中c(CH3COO─)=c(Na+)>c(H+)=c(OH─)時,一定是醋酸過量 |
| D.當溶液中c(Na+)>c(CH3COO─)>c(OH─)>c(H+)時,一定是氫氧化鈉過量 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2NH3(g) +
2NH3(g) + 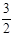 O2(g) ;△H =" a" kJ·mol—1
O2(g) ;△H =" a" kJ·mol—1| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
 2NH3(g) ΔH= -92.4kJ·mol—1
2NH3(g) ΔH= -92.4kJ·mol—1 2H2O(l) ΔH = -571.6kJ·mol—1
2H2O(l) ΔH = -571.6kJ·mol—1查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.酸能電離出H+和酸根離子,故酸為離子化合物 |
| B.共價化合物分子中一定含有共價鍵 |
| C.氫氧化鋇晶體與氯化銨固體的反應是吸收熱量的反應 |
| D.需加熱的反應不一定是吸熱反應 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2NH3(g)能量變化如右圖,回答下列問題:
2NH3(g)能量變化如右圖,回答下列問題:
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.Fe3O4 + 4CO =" 3Fe" + 4CO2△H= -14kJ·mol-1 |
| B.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -22kJ·mol-1 |
| C.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= +14kJ·mol-1 |
| D.Fe3O4(s) + 4CO(g) =" 3Fe(s)" + 4CO2(g)△H= -14kJ·mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com