
分析 (1)依據C=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$計算氯化鈉溶液的物質的量濃度,氯化鈉為強電解質完全電離所以溶液中存在n(Cl-)=n(NaCl),C(Cl-)=C(NaCl);
(2)依據溶液稀釋前后所含溶質的物質的量不變計算需要濃溶液的體積;
(3)溶液中溶質為NaCl、HCl,根據電荷守恒c(Na+)+c(H+)=c(Cl-),據此計算溶液在c(H+),而c(HCl)=c(H+),根據c=nV計算n(HCl),再根據V=nVm計算通入HCl的體積.
解答 解:(1)將117g NaCl溶于水配制成1L溶液,該溶液中NaCl的物質的量濃度為C=$\frac{n}{V}$=$\frac{\frac{m}{M}}{V}$=$\frac{\frac{117g}{58.5g}}{1L}$=2mol/L;氯化鈉為強電解質完全電離所以溶液中存在n(Cl-)=n(NaCl),C(Cl-)=C(NaCl)=2mol/L;
故答案為:2mol/L;2mol/L;
(2)設配制1mol•L-1的NaCl溶液500mL,需要2mol/L氯化鈉溶液體積為V,依據溶液稀釋前后所含溶質的物質的量不變,1mol•L-1×0.5L=2mol/L×V,
解得V=0.25L;
故答案為:0.25L;
(3)溶液中溶質為NaCl、HCl,根據電荷守恒c(Na+)+c(H+)=c(Cl-),溶液中c(Na+)=2mol/L,c(Cl-)=3mol/L,則c(H+)=3mol/L-2mol/L=1mol/L,而c(HCl)=c(H+)=1mol/L,故n(HCl)=1L×1mol/L=1mol,故通入HCl的體積=1mol×22.4L/mol=22.4L.
故答案為:22.4L.
點評 本題考查物質的量濃度有關計算,熟悉溶液中溶質與離子個數之間的關系、溶液中存在的電荷守恒是解題關鍵,題目難度不大.


科目:高中化學 來源: 題型:解答題
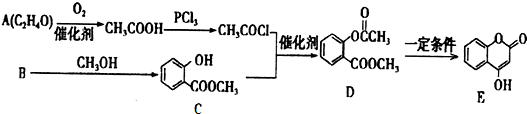
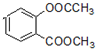 +3NaOH→CH3COONa+CH3OH+
+3NaOH→CH3COONa+CH3OH+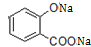 +H2O.
+H2O.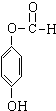
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
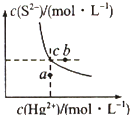 硫化汞(HgS)難溶于水,在自然界中呈紅褐色,常用于油畫顏料、印泥及朱紅雕刻漆器等.某溫度時,HgS在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )
硫化汞(HgS)難溶于水,在自然界中呈紅褐色,常用于油畫顏料、印泥及朱紅雕刻漆器等.某溫度時,HgS在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )| A. | 向硫化汞的濁液中加入硫化鈉溶液,硫化汞的Ksp減小 | |
| B. | 圖中a點對應的是飽和溶液 | |
| C. | 向c點的溶液中加入Hg(NO3)2,則c(S2-)減小 | |
| D. | 升高溫度可以實現c點到b點的轉化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
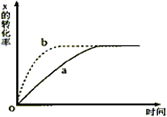 如圖曲線a表示放熱反應2X(g)?Z(g)+M(g)+N(s)進行過程中X的轉化率隨時間變化的關系,若要改變起始條件,使反應過程按b曲線進行,不可采取的措施是( )
如圖曲線a表示放熱反應2X(g)?Z(g)+M(g)+N(s)進行過程中X的轉化率隨時間變化的關系,若要改變起始條件,使反應過程按b曲線進行,不可采取的措施是( )| A. | 升高溫度 | B. | X的投入量增加 | C. | 加催化劑 | D. | 減小容器體積 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | D | |
| 陽極 | 藍 | 白 | 紅 | 藍 |
| 陰極 | 白 | 藍 | 藍 | 藍 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,1mol任何物質的體積都約為22.4L | |
| B. | 1mol任何氣體所含分子數都相同,體積也都約為22.4L | |
| C. | 同溫同壓下,相同體積的任何氣體單質所含原子數目相同 | |
| D. | 常溫常壓下0.3mol H2、0.7mol N2組成的混合氣體共含有NA個分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硝酸和稀硝酸都具有氧化性 | B. | 銅與硝酸的反應屬于置換反應 | ||
| C. | 金屬與硝酸反應不產生氫氣 | D. | 可用鐵或鋁制品盛裝濃硝酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 任何物質燃燒都必須有氧氣參加 | |
| B. | 氫氣在氯氣中燃燒發出淡藍色火焰,并在空氣中產生大量白霧 | |
| C. | 飽和氯水在光照下有氣泡產生,該氣體為氯氣 | |
| D. | 長久放置的氯水將失去漂白性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com