
氧化還原反應在生產、生話中應用廣泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化劑。用所學知識回答問題:
(1)在稀硫酸中,KMnO4能將H2C2O4氧化為CO2。該反應的化學方程式為 ,反應中消耗1mol的MnO4—時轉移電子數為 。
(2)取300mL 0.2mol/L的KI溶液與一定量的酸性KMnO4溶液恰好反應,生成等物質的量的I2和KIO3,則消耗KMnO4的物質的量的是 mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黃色變為淺綠色,過一會又變為棕黃色,溶液先變為淺綠色的離子方程式是 ,又變為棕黃色的原因是 。
(1)2KMnO4+5H2C2O4+ 3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O(2分) 3.01×1024(或答5NA也給分,2分)(2)0.032(2分)
(3)2Fe3+ + SO32-+ H2O = 2Fe2+ + SO42- + 2H+(2分) H+與NO3-組成的硝酸把Fe2+氧化(1分)
解析試題分析:(1)酸性條件下KMnO4與H2C2O4發生氧化還原反應生成MnSO4、K2SO4、CO2和水,反應的化學方程式為2KMnO4+5H2C2O4+3H2SO4=10CO2↑+2MnSO4+K2SO4+8H2O,反應中Mn元素化合價由+7價降低到+2價,反應中消耗1mol的MnO4-時轉移電子5mol,電子數為5NA或3.01×1024;(2)根據題給信息知n(KI)=0.06mol,與一定量的酸性KMnO4溶液恰好反應,生成等物質的量的I2和KIO3,則n(I2)=n(KIO3)=0.02mol,失的物質的量為2×0.02mol+0.02mol×6=0.16mol,1mol的MnO4-時得電子5mol,根據得失電子數目相等知,則消耗KMnO4的物質的量的是0.032mol;(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黃色變為淺綠色,原因是Fe3+與SO32-發生氧化還原反應生成Fe2+和SO42-,反應的離子方程式為2Fe3++SO32-+H2O=2Fe2++SO42-+2H+,反應后溶液呈酸性,則在酸性條件下,H+與NO3-組成的硝酸把Fe2+氧化成Fe3+,過一會又變為棕黃色。
考點:考查氧化還原方程式的書寫及相關計算。


科目:高中化學 來源: 題型:填空題
(10分)為了測定草酸晶體(H2C2O4·xH2O)中的x值,進行如下實驗
(1)稱取Wg草酸晶體,配成100.00mL溶液
(2)取25.00mL所配溶液于錐形瓶內,加入適量稀H2SO4后,用濃度為amol/L的KMnO4溶液滴定至KMnO4不再褪色為止,所發生的反應為: 2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
試回答:
①實驗中,需要的儀器有(填序號) ,還缺少的儀器有(填名稱)
A托盤天平(帶砝碼、鑷子) B滴定管 C 100mL的量筒 D、100mL的容量瓶
E、燒杯 F、漏斗 G、錐形瓶 H、玻璃棒 I、藥匙 J、燒瓶
②實驗中,標準KMnO4溶液應裝在 式滴定管中,因為
③若在接近滴定終點時,用少量蒸餾水將錐形瓶內壁沖洗一下,再繼續滴至終點,則所測得的x的值會 (填偏大、偏小、無影響)。
④在滴定過程中若用去amol/L的KMnO4溶液VmL,則所配制的草酸溶液的物質的量濃度為 mol/L,由此,x= 。
⑤若滴定終點讀數時俯視刻度,則計算的x值會 (填偏大、偏小、無影響)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在50 mL a mol·L-1的硝酸溶液中,加入6.4 g Cu,固體全部溶解,且還原產物只有NO2和NO。將反應后溶液用蒸餾水稀釋至100 mL,測得c(NO3-)=4 mol·L-1。
(1)稀釋后的溶液中c(H+)= mol·L-1
(2)若a=10,則生成的氣體中NO2的物質的量為________mol
(3)治理氮氧化物污染的方法之一是用NaOH溶液進行吸收,反應原理如下:
NO2+NO+2NaOH=2NaNO2+H2O 2NO2+2NaOH=NaNO2+NaNO3+H2O
若上述混合氣體被1 mol·L-1的NaOH溶液恰好吸收,則NaOH溶液的體積為________mL
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
L、M、R、P、Q分別代表五種含不同化合價的氮元素的物質。A、B分別代表兩種含不同化合價的氯元素的物質(每種物質中氮或氯元素的化合價只有一種)。又知物質M中的氮元素化合價要比物質Q中氮元素的化合價低。在一定條件下,它們會發生如下的轉化(關系式未配平):
①P+A―→Q+B ②L+O2―→M+H2O ③L+M―→R+H2O ④B+H2O―→A+O2
(1)若五種含氮元素的物質中,有一種是硝酸,則硝酸是 ,理由是 。
(2)反應②必須在催化劑(鉑、氧化鐵等)作用下,加熱到一定溫度時方能發生,此反應在化工生產上有重要用途,據此推斷在同溫同壓下,若物質R密度比空氣的密度小,則R的化學式為 。
(3)某同學寫出下面三個含氮的物質相互轉換的關系式:
Ⅰ.M+P―→N2O3+H2O
Ⅱ.N2O4+H2O―→P+Q
Ⅲ.M+L―→Q+H2O
其中一定不可能實現的是 ,理由是 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、C、D、F是常見的化合物,其中F在常溫下是一種無色液體,D為強酸,請根據下圖轉化關系(反應條件及部分產物已略去),回答下列問題:
(1)若A、B、C、D均為含硫元素的化合物,A是一種常見的礦石的主要成分,且A的摩爾質量為120 。 反應①的化學方程式為 ;
。 反應①的化學方程式為 ;
(2)若A、B、C、D均為含氮元素的化合物,且A的一個分子中只含有10個電子,則:
①A分子式為__________;
②反應④的離子方程式為________________________________________________
③取Cu和Cu2O的混合物樣品12.0g,加入到足量的D的稀溶液中,用排水法收集產生的氣體,標準狀況下其體積為2.24L,則樣品中Cu2O的質量為__________g。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
硫單質及其化合物在工農業生產中有著重要的應用。
(1)已知25℃時:SO2(g)+2CO(g)=2CO2(g)+1/xSx(s) △H=akJ/mol
2COS(g)+SO2(g)=2CO2(g)+3/xSx(s) △H=bkJ/mol。
則COS(g)生成CO(g)與Sx(s)反應的熱化學方程式是 。
(2)雄黃(As4S4)和雌黃(As2S3)是提取砷的主要礦物原料。已知As2S3和HNO3有如下反應:As2S3+10H++ 10NO3?=2H3AsO4+3S+10NO2↑+ 2H2O,當生成H3AsO4的物質的量為0.6 mol反應中轉移電子的數目為 ,
(3)向等物質的量濃度Na2S、NaOH混合溶液中滴加稀鹽酸至過量。其中H2S、HS?、S2?的分布分數(平衡時某物種的濃度占各物種濃度之和的分數)與滴加鹽酸體積的關系如下圖所示(忽略滴加過程H2S氣體的逸出)。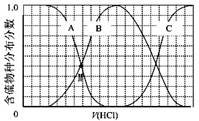
①B表示 。
②滴加過程中,溶液中微粒濃度大小關系正確的是 (填字母)。
a.c(Na+)= c(H2S)+c(HS?)+2c(S2?)
b.2c(Na+)=c(H2S)+c(HS?)+c(S2?)
c.c(Na+)=3[c(H2S)+c(HS?)+c(S2?)]
③NaHS溶液呈堿性,當滴加鹽酸至M點時,溶液中各離子濃度由大到小的順序為 。
(4)工業上用硫碘開路循環聯產氫氣和硫酸的工藝流程如下圖所示: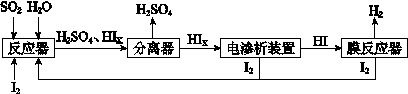
① 寫出反應器中發生反應的化學方程式是 。
② 電滲析裝置如圖所示,寫出陽極的電極反應式 。該裝置中發生的總反應的化學方程式是 。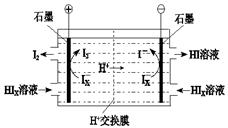
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為證明Fe3+具有較強的氧化性,甲同學做了如下實驗:將Cu片放入0.5mol/L Fe(NO3)3溶液中,觀察到Cu片逐漸溶解,溶液由黃色變為藍綠色,由此甲同學得到Fe3+具有較強氧化性的結論。
乙同學提出了不同的看法:“Fe(NO3)3溶液具有酸性,在此酸性條件下NO3-也能氧化Cu”,并設計實驗進行探究。已知:
| 水解反應 | 平衡常數(K) |
Fe3+ + 3H2O  Fe(OH)3 + 3H+ Fe(OH)3 + 3H+ | 7.9 × 10-4 |
Fe2+ + 2H2O  Fe(OH)2 + 2H+ Fe(OH)2 + 2H+ | 3.2 × 10-10 |
Cu2+ + 2H2O  Cu(OH)2 + 2H+ Cu(OH)2 + 2H+ | 3.2 × 10-7 |
| 實驗內容 | 實驗現象 |
| 甲同學的實驗方案 | 溶液逐漸變成藍綠色, pH略有上升 |
| 乙同學的實驗方案 | 無明顯現象,pH沒有明顯變化。 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(1)向NaBr和KI的混合溶液中,通入足量的Cl2后,將溶液蒸干并灼燒,最后蒸發皿中剩余的物質是________,寫出反應的化學方程式:________________________________。
(2)向KI溶液中滴入淀粉溶液,現象是____________________,再滴入氯水,現象是________,有關反應的離子方程式為______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
已知:2Fe3++2I-=2Fe2++I2,2Fe2++Br2=2Fe3++2Br-。
(1)含有1 mol FeI2和2 mol FeBr2的溶液中通入2 mol Cl2,此時被氧化的離子是________,被氧化的離子的物質的量分別是________________。
(2)如果向原溶液中通入3 mol Cl2,則被氧化的離子是________,其對應氧化產物的物質的量分別是________________。
(3)過二硫酸鉀(K2S2O8)具有強氧化性,可將I-氧化為I2:S2O82—+2I-=2SO42—+I2。通過改變反應途徑,Fe3+、Fe2+均可催化上述反應。試用離子方程式表示Fe3+對上述反應的催化過程:______________________________、____________________________(不必配平)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com