
【題目】用下列實驗裝置進行相應實驗,能達到實驗目的的是
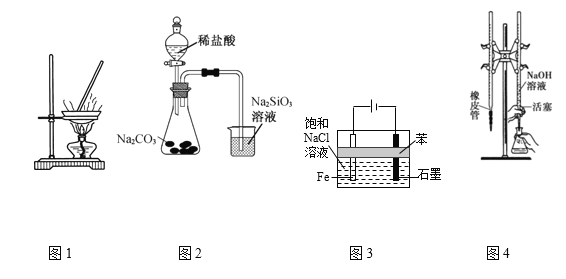
A.用圖1裝置蒸發CuCl2溶液獲得無水CuCl2
B.用圖2裝置可證明非金屬強弱:Cl>C>Si
C.用圖3裝置制備少量白色的Fe(OH)2沉淀
D.用圖4裝置進行已知濃度的NaOH溶液測定未知濃度的鹽酸
科目:高中化學 來源: 題型:
【題目】某地湖鹽中含有Ca2+、Mg2+、Fe3+、SO42-等雜質離子,氨堿廠用該地湖鹽制取燒堿。其中制得精制食鹽水的過程如下:

(1)過程Ⅰ中將粗鹽加水溶解需要適當加熱,其目的是__________。
(2)過程Ⅱ的目的是除去SO42-,加入的X溶液是__________。
(3)下表是過程Ⅱ、Ⅲ中生成的部分沉淀及其在20℃時的溶解度[g/100gH2O]
CaSO4 | Mg2(OH)2CO3 | CaCO3 | BaSO4 | BaCO3 | Fe(OH)3 |
2.6×10-2 | 2.5×10-4 | 7.8×10-4 | 2.4×10-4 | 1.7×10-3 | 4.8×10-9 |
①過程Ⅲ中生成的主要沉淀除CaCO3和Fe(OH)3外還有__________。
②過程Ⅳ中調節pH時發生的主要反應的離子方程式為__________。
(4)上述精制食鹽水中還含有微量的I-、IO3-、NH4+、Ca2+、Mg2+,除去這些離子及進行電解的流程如下:
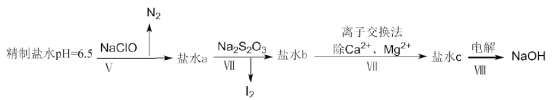
①過程V生成N2的離子方程式為__________。
②過程Ⅳ可以通過控制Na2S2O3的量,將IO3-還原成I2,且鹽水b中含有SO42-,該過程中發生氧化還原反應,其中氧化劑和還原劑的物質的量之比為__________。
③在過程Ⅳ中所用的Na2S2O3俗稱海波,是一種重要的化工原料。商品海波主要成分是Na2S2O3·5H2O。為了測定其含Na2S2O3·5H2O的純度,稱取8.00g樣品,配成250mL溶液,取25.00mL于錐形瓶中,滴加淀粉溶液作指示劑,再用濃度為0.0500mol·L-1的碘水滴定(發生反應2S2O32-+I2=S4O62-+2I-),下表記錄滴定結果:
滴定次數 | 滴定前讀數(mL) | 滴定后讀數(mL) |
第一次 | 0.30 | 29.12 |
第二次 | 0.36 | 30.56 |
第三次 | 1.10 | 29.88 |
計算樣品的純度為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按下圖所示裝置做實驗,若x軸表示流入陰極的電子的物質的量,則y軸可表示( )
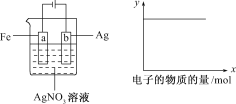
①c(Ag+) ②c(NO3-) ③a棒的質量 ④b棒的質量 ⑤溶液的pH
A.①③B.③④
C.①②④D.①②⑤
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】比較下列各項中的前者和后者,用“>”、 “<”或“=”填空
(1)熔點:NaCl_______CaO
(2)沸點: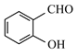 ____
____![]()
(3)在水中的溶解度:SO2_____CO2
(4)酸性:H3PO3_________H3PO4
(5)鍵能:H—O______ H—S
(6)價電子數:O________Cr
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫能被視為21世紀最具發展潛力的清潔能源。根據下列圖示有關說法正確的是
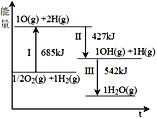
A.斷開非極性鍵和生成極性鍵的能量相同
B.反應II比反應III生成的O-H鍵更牢固
C.1/2O2(g) +H2(g) → OH(g) + H(g) ΔH1>0
D.H2O(g)→ 1/2O2(g) +H2(g) ΔH2<0
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】還原法處理氮的氧化物是環境科學研究的熱點課題。
I.氧氣還原法。H2還原NO發生的反應為:2NO(g)+2H2(g)![]() N2(g)+2H2O(g)。
N2(g)+2H2O(g)。
(1)已知兒種化學鍵的鍵能數據如下:

2NO(g)+2H2(g)![]() N2(g)+2H2O(g) ΔH=___kJ·mol-1。
N2(g)+2H2O(g) ΔH=___kJ·mol-1。
(2)2NO(g)+2H2(g)![]() N2(g)+2H2O(g)的反應速率表達式為v=kc2(NO)·c(H2)(k是速率常數,只與溫度有關)。科學研究發現上述反應分兩步進行:
N2(g)+2H2O(g)的反應速率表達式為v=kc2(NO)·c(H2)(k是速率常數,只與溫度有關)。科學研究發現上述反應分兩步進行:
反應1:2NO(g)+H2(g)![]() N2(g)+H2O2(g);
N2(g)+H2O2(g);
反應2:H2O2(g)+H2(g)![]() 2H2O(g)。
2H2O(g)。
總反應速率由反應較慢的一步決定,由此推知上述兩步反應中,活化能較大的是反應___(填“l”或“2”)。c(NO)對總反應速率的影響程度___c(H2)(填“大于”“小于”或“等于”)。
Ⅱ.NH3還原法。在恒容密閉容器中充入NH3和NO2,在一定溫度下發生反應:8NH3(g)+6NO2(g)![]() 7N2(g)+12H2O(g)。
7N2(g)+12H2O(g)。
(3)下列表明該反應達到平衡狀態的是___(填字母)。
A.混合氣體密度保持不變 B.NO2和N2的消耗速率之比為6:7
C.混合氣體中c(N2)=c(NO2) D.混合氣體壓強保持不變
III.CO還原法。利用高效催化劑處理汽車尾氣中的NO和CO,發生反應:2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH。在2L恒容密閉容器中充人2molCO和2molNO,測得NO的轉化率與溫度、時間的火系如圖所示。
N2(g)+2CO2(g) ΔH。在2L恒容密閉容器中充人2molCO和2molNO,測得NO的轉化率與溫度、時間的火系如圖所示。
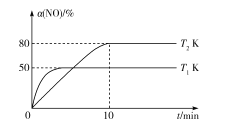
(4)下列說法正確的是___(填字母)。
A.圖像中,T1>T2
B.上述反應在高溫下能自發進行
C.10min時,T2K下正、逆反應速率相等
D.增大NO的濃度,反應物的轉化率增大
(5)T2K溫度下,0-10min內用CO表示的平均反應速率v(CO)=___mol/L-1·min-1;T1K溫度下,上述反應的平衡常數K=___L·mol-1。
(6)T1K溫度下,向平衡后的容器內再加入2molN2和2molNO,則平衡___(填“向右移動”“向左移動”或“不移動”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】a、b、c、d為原子序數依次增大的短周期不同主族元素,其中只有一種為金屬元素,四種元素的單質在通常情況下只有一種不是氣體,b與d的最外層電子數之和為a與c最外層電子數之和的四倍。下列敘述不正確的是
A. 原子半徑:c>d>a
B. d的氧化物對應的水化物酸性均比b的強
C. a、b、d三種元素形成的化合物可能既含離子鍵又含共價鍵
D. 單質的熔點:c>b>a
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將鐵粉和活性炭混合物用NaCl溶液濕潤,進行鐵的電化學腐蝕實驗(裝置如圖所示)。下列有關該實驗的說法正確的是( )
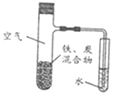
A.負極反應式為Fe-3e-=Fe3+
B.鐵腐蝕過程中化學能全部轉化為電能
C.用水代替NaCl溶液,鐵不能發生吸氧腐蝕
D.用稀醋酸代替NaCl溶液,最終導管中的液面會上升
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)已知短周期元素![]() 、
、![]() ,
,![]() 元素原子的最外層電子數為
元素原子的最外層電子數為![]() ,次外層電子數為
,次外層電子數為![]() ;
;![]() 元素原子的
元素原子的![]() 層(有電子)電子數為
層(有電子)電子數為![]() ,
,![]() 層電子數為
層電子數為![]() ,則
,則![]() 為______(填元素符號,下同),
為______(填元素符號,下同),![]() 為______.
為______.
(2)已知![]() 元素原子的
元素原子的![]() 層比
層比![]() 元素原子的
元素原子的![]() 層少3個電子,
層少3個電子,![]() 元素原子的核外電子總數比
元素原子的核外電子總數比![]() 元素原子的多5,則
元素原子的多5,則![]() 、
、![]() 分別為______、______。
分別為______、______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com