
| 溫度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常數 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
| A. | 該反應的△H<0 | |
| B. | 若反應經過一段時間后,達到平衡時A的轉化率為80% | |
| C. | 如反應初始6s內A的平均反應速率v(A)=0.003mol•L-1•s-1.則6s時 n(A)為0.11 mol | |
| D. | c(A)不隨時間改變或單位時間里生成c和D的物質的量相等均可作為是否達到平衡的依據 |
分析 A、由此表格可知,溫度越高,平衡常數越小,說明此反應為放熱反應;
B、設平衡時A的濃度變化量為x,利用三段式表示平衡時各組分的平衡濃度,代入平衡常數列方程計算x的值,再根據轉化率定義計算;
C、依據v(A)=$\frac{c(A)}{△t}$計算即可;
D、依據此化學反應的特點可知,任何時刻均有生成C和D的物質的量相等.
解答 解:A、700℃時,平衡常數為1.7,1000℃時,平衡常數為0.6,故溫度越高,平衡常數越小,說明此反應為放熱反應,即△H<0,故A正確;
B、設平衡時A的濃度變化量為x,則:
A(g)+B(g)?C(g)+D(g)
開始(mol/L):0.04 0.16 0 0
變化(mol/L):x x x x
平衡(mol/L):0.04-x 0.16-x x x
故$\frac{{x}^{2}}{(0.04-x)(0.16-x)}$=1,解得x=0.032所以平衡時A的轉化率為$\frac{0.032}{0.04}$×100%=80%,故B正確;
C、反應初始6s內A的平均反應速率v(A)=0.003mol•L-1•s-1.則6s時△n(A)=0.003mol•L-1•s-1×6s×5L=0.09 mol,故A剩余為:n(A)=0.2-0.09=0.11mol,故C正確;
D、由于C和D的化學計量數相等,故單位時間里生成c和D的物質的量相等不可作為是否達到平衡的依據,故D錯誤,故選D.
點評 本題考查化學反應速率、化學平衡常數的計算與運用等,難度較大,注意溫度不變時,平衡常數不變,化學方程式相反時,平衡常數互為倒數.


科目:高中化學 來源: 題型:選擇題
| A. | 閃電時,N2變為NO | B. | NO被空氣中O2氧化為NO2 | ||
| C. | 工業上,N2和H2反應生成NH3 | D. | 豆科植物根瘤菌把N2變成NH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 都是無色液體 | B. | 都是易揮發有刺激性氣味的液體 | ||
| C. | 濃溶液在空氣中都有白霧生成 | D. | 都是易溶于水的強酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
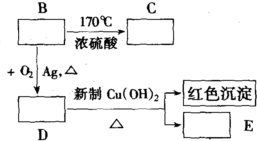
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| 實驗內容 | 實驗目的 | |
| A | 測定同濃度的Na3PO4和Na2SO4水溶液的pH | 探究磷、硫兩種元素非金屬性的強弱 |
| B | 向蔗糖溶液中加入4滴稀硫酸,煮沸幾分鐘,冷卻,再加入銀氨溶液,水溶加熱 | 檢驗蔗糖是否已水解 |
| C | 將乙醇與濃硫酸共熱產生氣體直接通入酸性kMnO4溶液 | 檢驗乙烯的生成 |
| D | 向AgCl沉淀中滴加少量KI溶液,觀察白色沉淀轉化為黃色沉淀 | 驗證Ksρ(AgCl)>Ksρ(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  的名稱為2-甲基-2-丙醇 的名稱為2-甲基-2-丙醇 | |
| B. | 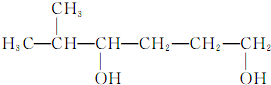 的名稱為2-甲基-3,6-己二醇 的名稱為2-甲基-3,6-己二醇 | |
| C. | 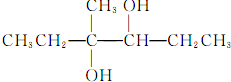 的名稱為4-甲基-2,4己-二醇 的名稱為4-甲基-2,4己-二醇 | |
| D. | 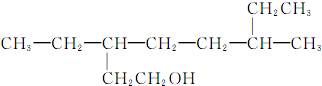 的名稱為3,6-二乙基-1-庚醇 的名稱為3,6-二乙基-1-庚醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入H2O(g),平衡向正反應方向移動,體系壓強減小 | |
| B. | 加入CO,混合氣體的密度增大 | |
| C. | 降低溫度,平衡向正反應方向移動 | |
| D. | 加入少量C,正反應速率增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com