
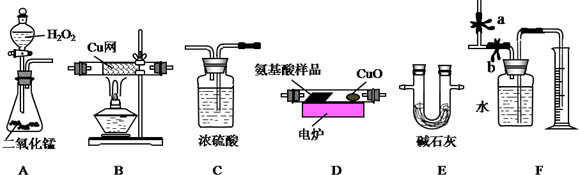
分析 根據(jù)題意可知,用燃燒法測定某種氨基酸(CxHyOzNp)的分子組成,用雙氧水產(chǎn)生氧氣,用純氧氣將CxHyOzNp氧化成二氧化碳、水和氮氣,用氧化銅將未完全氧化的碳元素氧化成二氧化碳,用濃硫酸吸收水,用堿石灰吸收二氧化碳,用銅網(wǎng)吸收未反應的氧氣,用排水量氣法測得氮氣的體積,為了準確測得各成分的質量,實驗開始先用氧氣將裝置中的空氣排盡,同時應按先吸收水,再吸收二氧化碳,再除氧氣,最后測氮氣的體積,根據(jù)元素守恒可計算出CxHyOzNp的組成,據(jù)此答題;
解答 解:根據(jù)題意可知,用燃燒法測定某種氨基酸(CxHyOzNp)的分子組成,用雙氧水產(chǎn)生氧氣,用純氧氣將CxHyOzNp氧化成二氧化碳、水和氮氣,用氧化銅將未完全氧化的碳元素氧化成二氧化碳,用濃硫酸吸收水,用堿石灰吸收二氧化碳,用銅網(wǎng)吸收未反應的氧氣,用排水量氣法測得氮氣的體積,為了準確測得各成分的質量,實驗開始先用氧氣將裝置中的空氣排盡,同時應按先吸收水,再吸收二氧化碳,再除氧氣,最后測氮氣的體積,根據(jù)元素守恒可計算出CxHyOzNp的組成,
(1)根據(jù)上面的分析可知,該實驗裝置的合理連接順序為:A、C、D、C、E、B(或B、E)、F,
故答案為:DCEB或DCBE;
(2)實驗開始時,首先打開止水夾a,關閉止水夾b,通一段時間的純氧,這樣做的目的是將裝置內的N2(或空氣)排除干凈,
故答案為:將裝置內的N2(或空氣)排除干凈;
(3)燃燒管D中放入CuO的作用是將未充分燃燒的產(chǎn)物CO轉化為CO2 (或使氨基酸中的碳完全轉化為CO2),裝置B的作用是 除去多余的O2,保證F裝置最終收集的氣體全為N2,
故答案為:將未充分燃燒的產(chǎn)物CO轉化為CO2 (或使氨基酸中的碳完全轉化為CO2); 除去多余的O2,保證F裝置最終收集的氣體全為N2;
(4)根據(jù)上面的分析可知,為了確定此氨基酸的分子式,除了準確測量N2的體積外,還需得到氨基酸的摩爾質量、生成二氧化碳氣體的質量、生成水的質量,故選ABC;
(5)在讀取F裝置中所排水的體積時,液面左低右高,則所測氣體的壓強大于空氣中的壓強,所以測得的體積偏小,
故答案為:偏小;
(6)根據(jù)分子式為C2H4O2,及氨基酸中的官能團可知,該分子中有羧基,實驗證明該官能團的方法為取該有機物少許于試管中,滴加NaHCO3溶液,有氣泡產(chǎn)生,
故答案為:取該有機物少許于試管中,滴加NaHCO3溶液,有氣泡產(chǎn)生.
點評 本題考查學生利用燃燒法確定有機物分子組成的知識,涉及實驗方案設計、根據(jù)原子守恒法來解答,難度較大,關鍵在于理解實驗原理.


 小學課時作業(yè)全通練案系列答案
小學課時作業(yè)全通練案系列答案 金版課堂課時訓練系列答案
金版課堂課時訓練系列答案 單元全能練考卷系列答案
單元全能練考卷系列答案 新黃岡兵法密卷系列答案
新黃岡兵法密卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4LSO3含有的分子數(shù)NA | |
| B. | 常溫常壓下,4.4gCO2的物質的量一定為0.1mol | |
| C. | 標準狀況下,氧原子總數(shù)為0.2NA的SO2和O2的混合氣體,其體積為2.24L | |
| D. | 7.8gNa2S和7.8gNa2O2中含有的陰離子數(shù)目均為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
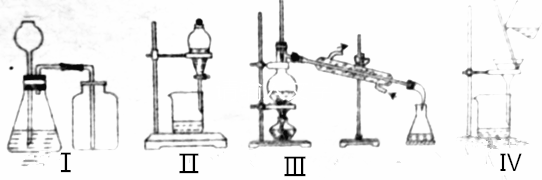
| A. | 選擇裝置Ⅰ用銅與濃硝酸反應制備NO2 | |
| B. | 選擇裝置Ⅱ分離乙酸乙酯和飽和碳酸氫鈉溶液的混合物 | |
| C. | 選擇裝置Ⅲ分離對硝酸甲苯和鄰硝基甲苯 | |
| D. | 選擇裝置Ⅳ分離飽和硫代硫酸鈉溶液和硫代硫酸鈉晶體的混合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 室溫下,12gC60和C70的混合物中含有的碳原子數(shù)為NA | |
| B. | 22.4L SO2氣體中含有的氧原子數(shù)為2NA | |
| C. | 1.0L 1.0mol•L-1CH3COOH溶液中含有的CH3COOH分子數(shù)為NA | |
| D. | 標準狀況下,5.6LCCl4含有的分子數(shù)為0.25NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | υ(A)=0.5mol/(L•min) | B. | υ(B)=1.2mol/(L•s) | C. | υ(C)=1mol/(L•s) | D. | υ(D)=2mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ②③ | C. | ①④ | D. | ③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A. | 反應在前50s的平均速率為v(PCl3)=0.0064mol/(L•s) | |
| B. | 保持其它條件不變,升高溫度,平衡時c(PCl3)=0.11mol/L,則反應的△H<0 | |
| C. | 相同溫度下,起始時向容器中充入4molPCl3、4molCl2,達到平衡時,則此反應的化學平衡常數(shù)為0.025mol/L | |
| D. | 相同溫度下,起始時間向容器中充入2molPCl5、0.40molPCl3和0.40molCl2,達到平衡前v(正)<v(逆) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X為負極、Y為正極 | |
| B. | 工作一段時間后,KOH的物質的量不變 | |
| C. | 在標況下通過5.6 L O2完全反應則有l(wèi).0 mol 電子發(fā)生轉移 | |
| D. | 該電池工作時甲烷一極附近溶液 pH降低 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,其分子的空間構型為三角錐型.
,其分子的空間構型為三角錐型.查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com