
【題目】下列關于40Ar、40K、40Ca說法正確的是
A.具有相同的質子數
B.具有相同的質量數
C.具有相同的中子數
D.互為同位素
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】在兩份相同的Ba(OH)2溶液中,分別滴入H2SO4、NaHSO4溶液,其導電能力隨滴入溶液體積變化的曲線如圖所示。下列分析不正確的是( )

A. ①代表滴加H2SO4溶液的變化曲線
B. b點,溶液中大量存在的離子是Na+、OH–
C. 曲線①的c點和曲線②的c點所代表的溶液酸堿性相同
D. a、d兩點對應的溶液均顯中性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物M是一種食品香料可以C4H10為原料通過如圖所示路線合成:
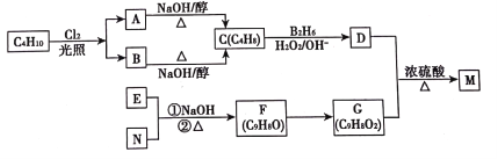
已知:①R—CH==CH2 ![]() R—CH2CH2OH
R—CH2CH2OH
②RCH2CHO+R′CH2CHO ![]()

③C、F分子中的碳鏈上C有支鏈,F沒有支鏈;E為芳香族化合物且E、N都能發生銀鏡反應。請回答下列問題:
(1)A、B均為一氯代烴,寫出其中一種的名稱(系統命名)___________;M中的含氧官能團名稱為___________。
(2)寫出下列反應的反應類型:D+G→M___________。
(3)F與新制Cu(OH)2/NaOH(aq)反應的化學方程式為_______________________________。
(4)M的結構簡式為___________________。
(5)與G具有相同官能團的G的芳香類同分異構體有___________種。
(6)參照上述合成路線,以苯乙烯( )和乙醛為原料(無機試劑任選),設計制備
)和乙醛為原料(無機試劑任選),設計制備![]() —C H2CH== CHCHO的合成路線:____________________________________________。
—C H2CH== CHCHO的合成路線:____________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】標準狀況下VL氨氣溶解在1L水中(水的密度近似為1g/mL),所得溶液的密度為ρg/mL,質量分數為ω,物質濃度為c mol/L,則下列關系中不正確的是
A. ![]()
B. ![]()
C. ![]()
D. ![]() =1000Vρ/(17V+22400)
=1000Vρ/(17V+22400)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究碳氧化合物、氮氧化合物、硫氧化合物等大氣污染物的處理對緩解環境污染、能源危機具有重要意義。工業上處理氮的氧化物途徑有多種:
Ⅰ.堿吸法。
(1)利用純堿溶液吸收NO、NO2,發生的反應共生成兩種鹽,請寫出有關氧化還原方程式:______________________________________、NO+NO2+Na2CO3=2NaNO2+CO2
Ⅱ.催化氧化法:城市中NOx和CO污染主要來源于汽車尾氣,可以利用化學方法將其轉化為無毒無害的物質。
(2)已知:N2(g)+O2(g)![]() 2NO(g) ΔH=+180 kJ·mol-1
2NO(g) ΔH=+180 kJ·mol-1
2CO(g)+O2(g)![]() 2CO2(g) ΔH=-564 kJ·mol-1
2CO2(g) ΔH=-564 kJ·mol-1
請寫出把汽車尾氣轉化為無毒無害的物質的熱化學方程式:__________________________
(3)為研究汽車尾氣轉化為無毒無害的物質有關反應,在密閉容器中充入10molCO和8molNO,發生反應,如圖為平衡時NO的體積分數與溫度、壓強的關系。

①該反應達到平衡后,為在提高反應速率同時提高NO的轉化率,可采取的措施有__________(填字母序號)。
a.改用高效催化劑 b.縮小容器的體積 c.升高溫度 d.增加CO的濃度
②壓強為10 MPa、溫度為T1下,若反應進行到20 min達到平衡狀態,容器的體積為4 L,用CO2的濃度變化表示的平均反應速率v(CO2)=_______,該溫度下平衡常數Kp=______(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數;保留兩位有效數字)。
③若在D點對反應容器降溫的同時縮小體積至體系壓強增大,重新達到的平衡狀態可能是圖中A~G點中的______點。
Ⅲ. 電解硝酸工業的尾氣NO可制備NH4NO3,其工作原理如圖。

(4)N極的電極反應式為________。
(5)在25℃時,將a mol·L-1的氨水與0.1mol·L-1的硝酸等體積混合后溶液顯中性,用含a的代數式表示NH4NO3的水解常數Kh=_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四氯化錫可用作媒染劑。利用如圖所示裝置可以制備四氯化錫(部分夾持裝置已略去);

有關信息如下表:
化學式 | SnCl2 | SnCl4 |
熔點/℃ | 246 | -33 |
沸點/℃ | 652 | 144 |
其他性質 | 無色晶體,易氧化 | 無色液體,易水解 |
回答下列問題:
(1)甲裝置中儀器A的名稱為___________。
(2)用甲裝置制氯氣,MnO4- 被還原為Mn2+,該反應的離子方程式為________________。
(3)將裝置如圖連接好,檢查氣密性,慢慢滴入濃鹽酸,待觀察到__________(填現象)后,開始加熱丁裝置,錫熔化后適當增大氯氣流量,繼續加熱丁裝置,此時繼續加熱丁裝置的目的是:
①促進氯氣與錫反應;
②_______________________________。
(4)如果缺少乙裝置,可能發生的副反應的化學方程式為___________________;己裝置的作用是_________________:
A.除去未反應的氯氣,防止污染空氣
B.防止空氣中CO2氣體進入戊裝置
C.防止水蒸氣進入戊裝置的試管中使產物水解
D.防止空氣中O2進入戊裝置的試管中使產物氧化
(5)某同學認為丁裝置中的反應可能產生SnCl2雜質,以下試劑中可用于檢測是否產生SnCl2 的有_______________(填標號)。
A. H2O2溶液 B. FeCl3溶液(滴有KSCN) C. AgNO3溶液 D. 溴水
(6)反應中用去錫粒1.19g,反應后在戊裝置的試管中收集到2.38gSnCl4,則SnCl4的產率為________。(保留3位有效數字)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖為某二次電池充電時的工作原理示意圖,該過程可實現鹽溶液的淡化。下列說法錯誤的是

A. 充電時,a 為電源正極
B. 充電時,Cl-向Bi 電極移動,Na+向NaTi2(PO4)3 電極移動
C. 放電時,正極的電極反應為BiOCl+2H++3e-=Bi+Cl-+H2O
D. 充電時,新增入電極中的物質:n(Na+):n(Cl-) =1:3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列事實不能用平衡移動原理解釋的是
A. 夏天打開啤酒瓶蓋后產生大量氣泡
B. 濃氨水中加入NaOH 固體產生有刺激性氣味氣體
C. 實驗室用排飽和食鹽水的方法收集氯氣
D. 壓縮H2和I2反應的平衡混合氣體,氣體顏色變深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T時,向2.0L恒容密閉容器中充入1.0 mol PCl5,反應PCl5(g)![]() PCl3(g)+Cl2(g)經一段時間后達到平衡。反應過程中測定的部分數據見下表:下列說法正確的是
PCl3(g)+Cl2(g)經一段時間后達到平衡。反應過程中測定的部分數據見下表:下列說法正確的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反應在前50 s的平均速率為v(PCl3)=0.0032mol·L-1·s-1
B.保持其他條件不變,升高溫度,平衡時c(PCl3)=0.11mol·L-1,則反應的△H<0
C.相同溫度下,起始時向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,達到平衡前v(正)>v(逆)
D.相同溫度下,起始時向容器中充入2.0mol PCl3和2.0molCl2,達到平衡時,PCl3的轉化率小于80%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com