
【題目】隨著現代工業的發展,二氧化碳污染的處理成為科學研究的重點,回答下列問題:
I.有人提出利用H2還原CO2使其轉化為有機化工的主要原料乙烯。
(1)查閱資料:H2的燃燒熱為285.8kJ/mol,C2H4的燃燒熱為l41lkJ/mol,lmolH2O(1)轉化為H2O(g)需吸收44kJ的熱量。則反應6H2(g)+2CO2(g) ![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
△H=___________kJ/mol。
(2)下圖是探究不同溫度對CO2的轉化率和催化劑的催化效率影響的示意圖。

①生產中通常選用的溫度最好是___________,理由是___________。
②圖中表示的化學平衡常數:M___________N(填>、=、<)
③250℃時,在2L密閉容器中分別充入6molH2和2 molCO2,到達平衡時體系中C2H4的體積分數為___________。
Ⅱ.CO在一定條件下,能與H2合成二甲醚:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)。
CH3OCH3(g)+3H2O(g)。
(1)在1L的密閉容器中分別充入2.5molH2與 bmol CO2發生反應,在不同溫度下達到平衡狀態時測得實驗數據如下表:

①到達平衡時若升高溫度,則上述平衡___________方向移動(填“正反應”或“逆反應”)。
②轉化率:x___________y(填>、=、<)
(2)新型高效的二甲醚燃料電池工作時總反應式:CH3OCH3+3O2=2CO2+3H2O。
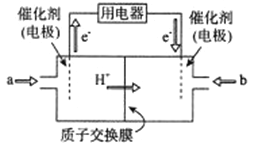
①該電池的負極是___________(填a或b),負極電極反應式為___________;
②利用該電池冶鋁,若制得金屬鋁54g理論上消耗二甲醚___________g。
【答案】-127.8 250℃ 此時催化劑活性最高 > 7.7%或1/13 逆反應 > a CH3OCH3+3H2O-12e-=2CO2↑+12H+ 23
【解析】
I.(1)根據燃燒熱的概念和題意寫出熱化學方程式:H2(g)+0.5O2(g)=H2O(1)△H=-285.8kJ/mol①;C2H4(g)+3O2(g)=2H2O(l)+2CO2(g)△H=-1411.0kJ·mol-1②;H2O(g)=H2O(l)△H=-44kJ·mol-1③;利用蓋斯定律將①×6-②-③×4可得。
(2)①根據圖示催化劑的反應活性和溫度對速率、平衡的影響綜合考慮:此時催化劑活性最高。
②升高溫度二氧化碳的平衡轉化率減低,則升溫平衡逆向移動,所以M點化學平衡常數大于N點;
③根據三段式計算;
Ⅱ.(1)①分析表格數據,根據溫度對CO2的轉化率影響分析;
②由CO2起始物質的量為1.25mol時,溫度越高,CO2的轉化率越小,說明正反應是放熱反應,故結合表格分析。
(2)①根據電子流動方向和氫離子移動方向可知,通入a的電極為負極;電極反應為:CH3OCH3+3H2O-12e-=2CO2↑+12H+
②根據關系式4Al~12e-~CH3OCH3計算。
(1)根據H2(g)的燃燒熱為285.8kJ·mol-1,則其熱化學方程式為:H2(g)+0.5O2(g)=H2O(1)△H=-285.8kJ/mol①;CH2=CH2(g)的燃燒熱為1411.0kJ·mol-1,其熱化學方程式為:C2H4(g)+3O2(g)=2H2O(l)+2CO2(g)△H=-1411.0kJ·mol-1②;H2O(g)=H2O(l)△H=-44kJ·mol-1③;利用蓋斯定律將①×6-②-③×4可得:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)△H=-127.8kJ·mol-1。
CH2=CH2(g)+4H2O(g)△H=-127.8kJ·mol-1。
(2)①如圖所示,化學反應速率隨溫度的升高而加快,催化劑的催化效率隨溫度升高先增大后降低,所以根據催化劑的反應活性和溫度對速率、平衡的綜合影響角度,最好選擇250℃;
②升高溫度二氧化碳的平衡轉化率減小,則升溫平衡逆向移動,所以M點化學平衡常數大于N點;
③在2L密閉容器中分別充入6 mol H2和2 mol CO2,由圖可知250℃時,M點的二氧化碳轉化率50%,由方程式可得
6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g)
CH2=CH2(g)+4H2O(g)
起始量(mol·L-1) 3 1 0 0
變化量(mol·L-1) 1.5 0.5 0.25 1
平衡量(mol·L-1) 1.5 0.5 0.25 1
產物CH2=CH2的體積分數=![]() =7.7%
=7.7%
Ⅱ.(1)①分析表格可知,當CO2起始物質的量為1.25mol時,溫度越低,CO2的轉化率越大,說明降低溫度平衡向正反應方向移動,故升高溫度平衡向逆反應方向移動;
②由CO2起始物質的量為1.25mol時,溫度越高,CO2的轉化率越小,說明正反應是放熱反應,故結合表格可知w<32,x>33;由于CO2(g)、H2(g)按物質的量1:3反應,H2(g)物質的量為2.5mol,CO2的物質的量(b)越大,CO2的轉化率越小,則y<w,綜合上述分析可知x>33>32>w>y;
(2)①根據圖知交換膜是質子交換膜,則電解質溶液呈酸性,根據電子流動方向和氫離子移動方向可知,通入a的電極為負極、通入b的電極為正極,負極上二甲醚失去電子發生氧化反應生成二氧化碳,負極反應式為 CH3OCH3+3H2O-12e-=2CO2↑+12H+;根據電子守恒,可以建立關系式4Al~12e-~CH3OCH3,由此可得若制得金屬鋁54g,理論上消耗甲醇23g。


 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源: 題型:
【題目】把5.1g鎂鋁合金的粉末放入過量的鹽酸中,得到5.6L H2(標準狀況下).試計算:
(1)該合金中鋁的質量分數_______;
(2)該合金中鋁和鎂的物質的量之比_______;
(3)若向反應后的溶液中加入足量的NaOH溶液,最終能產生沉淀_______克?
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機化合物的說法正確的是
A. (CH3)3C-CH=CH2與氫氣完全反應后,生成2,2,3-三甲基戊烷
B. 工業上由乙烯制乙醇、苯制環己烷均屬于加成反應
C. C5H11Cl的同分異構體有3種
D.  分子中所有碳原子一定在同一平面上
分子中所有碳原子一定在同一平面上
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】釩是人體必需的微量元素,能預防突發性心臟病等疾病,常見化合價有+2、+3、+4和+5。實驗室模擬工業生產制備V2(CO3)3的步驟如下:
①取18.20gV2O5放入水中攪拌形成懸濁液,通入二氧化硫充分反應可得V2(SO4)3溶液。
②將V2(SO4)3溶液與足量的碳酸鈉溶液混合,充分反應后過濾洗滌、干燥,得V2(CO3)3固體22.56g。
已知:+5價Ⅴ具有氧化性,+3價V具有還原性,易被氧氣氧化。
回答下列問題:
(1)實驗室用Na2SO3固體和H2SO4(濃)制取SO2,可選用的發生裝置是___________(填A或B),若利用下述裝置制取并收集干燥的SO2,連接順序為a→___________→___________→___________→___________→f。

(2)步驟①實驗裝置如下:
①圖中利用水浴處理的優點是___________,裝置C中長頸漏斗的作用是___________。
②通入二氧化硫前和實驗結束后都要通入N2,目的是___________。
③寫出儀器D中反應的離子方程式___________。

(3)步驟②中洗滌操作后,證明已經洗凈的操作是___________,本實驗中的產率為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將一定質量的鎂鋁混合物投入200 mL硫酸中,固體全部溶解后,向所得溶液中加入5 mol/L的NaOH溶液,生成沉淀的物質的量n與加入NaOH溶液的體積V的變化如圖所示。
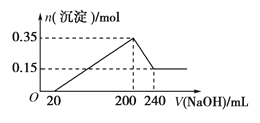
(1)加入NaOH 0~ 20mL 時發生反應離子方程式___________________,
加入NaOH 20~ 200mL 時發生反應離子方程式___________________,
加入NaOH 200~ 240mL 時發生反應離子方程式___________________,
(2)鎂和鋁的總質量為________g
(3)硫酸的物質的量濃度為___________ mol/L
(4)生成的氫氣在標準狀況下的體積為__________L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】簡單原子的原子結構可用下圖形象地表示:

其中●表示質子或電子,○表示中子,則下列有關①②③的敘述正確的組合是( )
a.①②③互為同位素 b.①②③互為同素異形體
c.①②③是三種化學性質不同的粒子 d.①②③具有相同的質量數
e.①②③具有相同的質量 f.①②③是三種不同的原子
A. a、fB. d、eC. b、cD. e、f
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應A (g)+ 3B(g) =2C(g) + 2D(g),下列數據表示反應進行得最快的是( )
A. v(A)=0.7mol/(L·s)B. v (B) =1.8mol/(L· s)
C. v (C)=1mol/(L·s)D. v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫時,改變飽和氯水的pH,得到部分含氯微粒的物質的量分數與pH的關系如圖所示。下列敘述不正確的是

A. 該溫度下,HClO![]() H++ClO-的電離常數Ka的對值lgKa= -7.54
H++ClO-的電離常數Ka的對值lgKa= -7.54
B. 氯水中的Cl2、ClO-、HClO均能與KI發生反應
C. pH=1的氯水中,c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
D. 已知常溫下反應Cl2(aq)+Cl-(aq)![]() Cl3-(aq)的K=0.191,當pH增大時,K減小
Cl3-(aq)的K=0.191,當pH增大時,K減小
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com