
【題目】天津屬于沿海城市,下列與海洋有關說法正確的是( )
A.從海水中提取![]() 單質,最后一步電解
單質,最后一步電解![]() 飽和溶液,就可制得金屬鎂
飽和溶液,就可制得金屬鎂
B.海水經(jīng)過一定生產過程可以制造出殺滅病毒的84消毒液
C.從海帶中提取碘,含![]() 的溶液可以用酒精萃取
的溶液可以用酒精萃取
D.海水中富集的元素氯在目前已知的元素中電負性最強
科目:高中化學 來源: 題型:
【題目】四水合磷酸鋅[Zn3(PO4)2·4H2O],摩爾質量為457g·mol-1,難溶于水]是一種性能優(yōu)良的綠色環(huán)保防銹顏料。實驗室以鋅灰(含ZnO、CuO、FeO、Fe2O3、SiO2等)為原料制備Zn3(PO4)2·4H2O的流程如圖,回答下列問題:
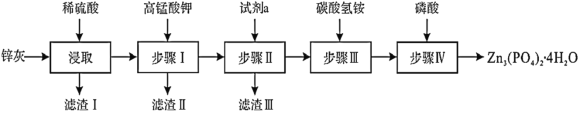
已知:6NH4HCO3+3ZnSO4 ![]() ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑
ZnCO3·2Zn(OH)2·H2O↓+3(NH4)2SO4+5CO2↑
(1)實驗前需要將鋅灰研磨成粉末狀,原因是____。
(2)步驟I中需將溶液pH調至5.1,應選擇的最佳試劑是___。(填字母)
a.NaOH b.ZnO c.Ba(OH)2
(3)步驟I滴加KMnO4溶液的目的是___。
(4)步驟Ⅱ中加入的a是___。
(5)步驟Ⅳ的化學方程式是___。
(6)步驟Ⅳ反應結束后得到Zn3(PO4)2·4H2O的操作包括___和干燥。
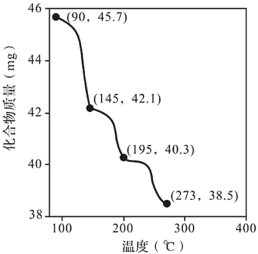
(7)稱取45.7mgZn3(PO4)2·4H2O進行熱重分析,化合物質量隨溫度的變化關系如圖所示,為獲得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合產品,烘干時的溫度范圍為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分別按下圖甲、乙所示裝置進行實驗,圖中兩個燒杯里的溶液為同濃度的稀硫酸,乙中A為電流表。請回答下列問題:
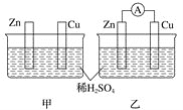
(1)以下敘述中,正確的是_______________(填字母)。
A.甲中鋅片是負極,乙中銅片是正極
B.兩燒杯中銅片表面均有氣泡產生
C.兩燒杯中溶液pH均增大
D.產生氣泡的速度甲中比乙中慢
E.乙的外電路中電流方向Zn→Cu
F.乙溶液中![]() 向銅片方向移動
向銅片方向移動
(2)變化過程中能量轉化的主要形式:甲為___________;乙為______。
(3)在乙實驗中,某同學發(fā)現(xiàn)不僅在銅片上有氣泡產生,而且在鋅片上也產生了氣體,分析原因可能是___。
(4)在乙實驗中,如果把硫酸換成硫酸銅溶液,請寫出銅電極的電極反應方程式及總反應離子方程式:銅電極:____,總反應:___。當電路中轉移0.25 mol電子時,消耗負極材料的質量為_____g(Zn的相對原子質量65)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組要完成中和熱的測定。
(1)實驗桌上備有大、小兩個燒杯、泡沫塑料、泡沫塑料板、膠頭滴管、環(huán)形玻璃攪拌棒、0.5 mol·L-1鹽酸、0.55 mol·L-1 NaOH溶液,實驗尚缺少的玻璃用品是___________、___________。
(2)實驗中能否用環(huán)形銅絲攪拌棒代替環(huán)形玻璃攪拌棒___________(填“能”或“否”),其
原因是 。
(3)他們記錄的實驗數(shù)據(jù)如下:

已知:Q=cm(t2-t1),反應后溶液的比熱容c為4.18 kJ·℃-1·kg-1,各物質的密度均為1 g·cm-3。
①計算完成上表ΔH=_____________。
②根據(jù)實驗結果寫出NaOH溶液與HCl溶液反應的熱化學方程式: 。
(4)若用KOH代替NaOH,對測定結果__________(填“有”或“無”)影響;若用醋酸代替HCl做實驗,對測定結果____________(填“有”或“無”)影響。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在某一恒溫、恒容的密閉容器中發(fā)生反應:3H2(g)+N2(g)![]() 2NH3(g) ΔH<0。t1時刻反應達到平衡,在t2時刻改變某一條件,其反應過程如圖所示。下列說法正確的是
2NH3(g) ΔH<0。t1時刻反應達到平衡,在t2時刻改變某一條件,其反應過程如圖所示。下列說法正確的是

A. Ⅰ、Ⅱ兩過程達到平衡時,平衡常數(shù):KⅠ<KⅡ
B. Ⅰ、Ⅱ兩過程達到平衡時,NH3的體積分數(shù):Ⅰ<Ⅱ
C. Ⅰ、Ⅱ兩過程達到平衡的標志:氣體的平均密度不再發(fā)生變化
D. t2時刻改變的條件可以是向密閉容器中加H2和N2的混合氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對可逆反應4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列敘述正確的是( )
4NO(g)+6H2O(g),下列敘述正確的是( )
A. 達到化學平衡時4v正(O2)=5v逆(NO)
B. 若單位時間內生成x mol NO的同時,消耗x mol NH3,則反應達到平衡狀態(tài)
C. 達到化學平衡時,若增大容器容積,則正反應速率減小,逆反應速率增大
D. 化學反應速率關系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗操作或分析正確的是( )
A.用濕潤的![]() 試紙測鹽酸的
試紙測鹽酸的![]()
B.檢驗淀粉是否水解,可以向淀粉溶液中加入稀![]() ,加熱一段時間,冷卻后加入新制
,加熱一段時間,冷卻后加入新制![]() ,煮沸,觀察是否有紅色沉淀生成
,煮沸,觀察是否有紅色沉淀生成
C.乙醇和乙酸在濃硫酸作用下,酯化制得乙酸乙酯,提純乙酸乙酯需要經(jīng)過水、氫氧化鈉溶液洗滌
D.用鹽酸標準溶液滴定待測的氫氧化鈉溶液時,水洗后的酸式滴定管未經(jīng)標準液潤洗,則測定結果偏高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】甲苯是煤干餾的產物,可用于制備具有止痛退熱效果的冬青油( 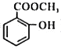 ),合成路線如下:
),合成路線如下:
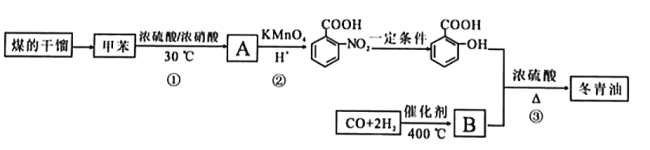
已知: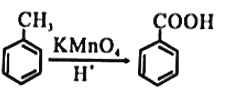
請回答下列問題
(1)煤的干餾是_______________。(填“物理變化”或“化學變化”).
(2)A的結構簡式為_______________。反應①的反應類型是_______________。
(3)反應②的反應類型是_______________。
(4)B的官能團名稱為_______________。
(5)反應③的化學方程式_______________。
(6)C是冬青油的同分異構體,其苯環(huán)上的取代基與冬青油相同,則C的結構簡式可能為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氣是一種清潔能源,氫氣的制取是氫能源利用領域的研究熱點;氫氣也是重要的化工原料。
(1)納米級的Cu2O可作為太陽光分解水的催化劑。一定溫度下,在2L密閉容器中加入納米級Cu2O并通入0.10mol水蒸氣發(fā)生反應:2H2O(g)![]() 2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同時段產生O2的量見表格:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1,不同時段產生O2的量見表格:
時間/min | 20 | 40 | 60 | 80 |
n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
上述反應過程中能量轉化形式為光能轉化為____能,達平衡過程中至少需要吸收光能___kJ(保留三位小數(shù))。
(2)氫氣是合成氨工業(yè)的原料,合成塔中每產生2 molNH3,放出92.2kJ熱量。已知:

則1 molN—H鍵斷裂吸收的能量約等于_____。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com