
 3Fe+4C02,若有1mol Fe34參加反應,轉移電子的物質的量是______mol;
3Fe+4C02,若有1mol Fe34參加反應,轉移電子的物質的量是______mol;

 ,故答案為:
,故答案為: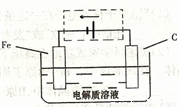 ;
;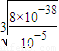 ,
,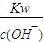 ,lg2=0.3pH=3.3,故答案為:3.3;
,lg2=0.3pH=3.3,故答案為:3.3;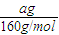 ×2×56g/mol=0.7ag,
×2×56g/mol=0.7ag,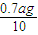 =0.07ag,故答案為:0.07a.
=0.07ag,故答案為:0.07a.

 口算心算速算應用題系列答案
口算心算速算應用題系列答案 同步拓展閱讀系列答案
同步拓展閱讀系列答案科目:高中化學 來源: 題型:閱讀理解
 (2010?臨沂一模)Fe元素是地殼中最豐富的元素之一,在金屬中僅次于鋁,鐵及其化合物在生活、生產中有廣泛應用.請回答下列問題:
(2010?臨沂一模)Fe元素是地殼中最豐富的元素之一,在金屬中僅次于鋁,鐵及其化合物在生活、生產中有廣泛應用.請回答下列問題:
| ||


查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪專題沖刺第9講 金屬及其化合物練習卷(解析版) 題型:填空題
Fe元素是地殼中最豐富的元素之一,在金屬中含量僅次于鋁,鐵及其化合物在生活生產中有廣泛應用。請回答下列問題。
(1)磁鐵礦是工業上冶煉鐵的原料之一,其原理是Fe3O4+4CO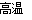 3Fe+4CO2,若有1 mol Fe3O4參加反應,轉移電子的物質的量是________ mol。
3Fe+4CO2,若有1 mol Fe3O4參加反應,轉移電子的物質的量是________ mol。
(2)與明礬相似,硫酸鐵也可用作凈水劑,在使用時發現硫酸鐵并不能使酸性廢水中的懸浮物沉降除去,其原因是___________________________________________________。
(3)某課外活動小組將下圖所示裝置按一定順序連接,在實驗室里制取一定量的FeCl3(所通氣體過量并充分反應)。
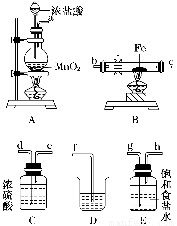
請回答下列問題:
①各裝置的正確連接順序為(填寫裝置代號)
A→________→________→________→D。
②裝置C的作用是_______________________________________________________。
③反應開始后,B中硬質玻璃管內的現象為________;可以檢驗生成物中含有Fe3+的試劑是________(填寫試劑名稱)。
查看答案和解析>>
科目:高中化學 來源: 題型:
Fe元素是地殼中最豐富的元素之一,在金屬中僅次于鋁,鐵及其化合物在生活、生產中有廣泛應用。請回答下列問題:
(1)磁鐵礦是工業上冶煉鐵的原料之一,其原理是Fe304+4CO![]() 3Fe+4C02,若有1mol
3Fe+4C02,若有1mol
Fe304參加反應,轉移電子的物質的量是 mol.
 (2)與明礬相似,硫酸鐵也可用作凈水劑,在使用時發現硫酸鐵并不能使酸性廢水中的懸浮物沉降除去,其原因是
(2)與明礬相似,硫酸鐵也可用作凈水劑,在使用時發現硫酸鐵并不能使酸性廢水中的懸浮物沉降除去,其原因是
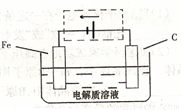
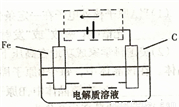
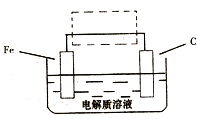
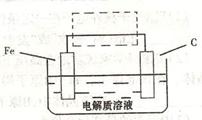
(3)鋼鐵的電化腐蝕簡單示意圖如下,將該圖稍作修
改即可成為鋼鐵電化學防護的簡單示意圖,請在下圖虛
線框內作出修改,并用箭頭標出電子流動方向。
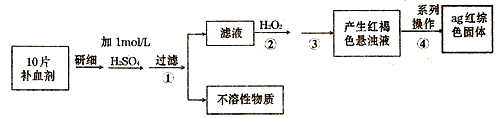
(4)硫酸亞鐵晶體(FeS04·7H20)常作醫藥上的補血劑。課外研究性小組測定該補血劑中鐵元素的含量。實驗步驟如下:

請回答下列問題:
①證明步驟①所得濾液中含有Fe2+的方法是先滴加KSCN溶液,再滴加,此過程的現象為:
②若該實驗溫度下,步驟③中難溶物的溶度積為Ksp=8×l0-38,試計算該物質沉淀完全所需要的pH= (已知溶液中離子濃度小于10-5mol)時,該離子可看做沉淀完全;lg2=0.3)
③步驟④中一系列的操作步驟為:過濾、 、灼燒、冷卻、稱量。
④若實驗過程中無損耗,最后稱量得到a克紅棕色的固體,則每片補血劑中含鐵元素的質
量為 g.(用含a的式子表示)
查看答案和解析>>
科目:高中化學 來源:山東省臨沂市2010屆高三一模(化學) 題型:實驗題
Fe元素是地殼中最豐富的元素之一,在金屬中僅次于鋁,鐵及其化合物在生活、生產中有廣泛應用。請回答下列問題:
(1)磁鐵礦是工業上冶煉鐵的原料之一,其原理是Fe304+4CO 3Fe+4C02,若有1mol
3Fe+4C02,若有1mol
Fe304參加反應,轉移電子的物質的量是 mol.
 (2)與明礬相似,硫酸鐵也可用作凈水劑,在使用時發現硫酸鐵并不能使酸性廢水中的懸浮物沉降除去,其原因是
(2)與明礬相似,硫酸鐵也可用作凈水劑,在使用時發現硫酸鐵并不能使酸性廢水中的懸浮物沉降除去,其原因是
(3)鋼鐵的電化腐蝕簡單示意圖如下,將該圖稍作修
改即可成為鋼鐵電化學防護的簡單示意圖,請在下圖虛
線框內作出修改,并用箭頭標出電子流動方向。
(4)硫酸亞鐵晶體(FeS04·7H20)常作醫藥上的補血劑。課外研究性小組測定該補血劑中鐵元素的含量。實驗步驟如下:
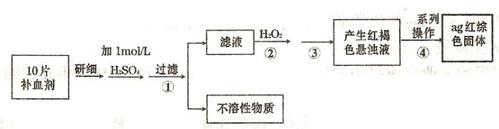
請回答下列問題:
①證明步驟①所得濾液中含有Fe2+的方法是先滴加KSCN溶液,再滴加,此過程的現象為:
②若該實驗溫度下,步驟③中難溶物的溶度積為Ksp=8×l0-38,試計算該物質沉淀完全所需要的pH= (已知溶液中離子濃度小于10-5mol)時,該離子可看做沉淀完全;lg2=0.3)
③步驟④中一系列的操作步驟為:過濾、 、灼燒、冷卻、稱量。
④若實驗過程中無損耗,最后稱量得到a克紅棕色的固體,則每片補血劑中含鐵元素的質
量為 g.(用含a的式子表示)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com