
| KMnO4酸性溶液 的濃度/mol?L-1 |
溶液褪色所需時間 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
| 0.001mol?L-1×0.004L |
| 0.004L+0.002L |
| 6min+7min+7min |
| 3 |
| △c |
| △t |
| 0.00067mol?L-1 |
| 6.7min |


 考前必練系列答案
考前必練系列答案科目:高中化學 來源: 題型:
| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.0 | 3.1 | 8.1 |

查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
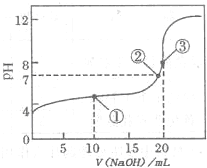 (2011?巢湖二模)滴定法是化學定量分析的一種重要而普遍的方法.
(2011?巢湖二模)滴定法是化學定量分析的一種重要而普遍的方法.| 實驗 | 樣品體積/mL | 高錳酸鉀溶液體積/mL |
| 1 | 10.00 | 8.98 |
| 2 | 10.00 | 8.58 |
| 3 | 10.00 | 9.02 |
| 4 | 10.00 | 9.00 |
查看答案和解析>>
科目:高中化學 來源:2011屆江蘇省姜堰市二中高三上學期學情調查(三)化學試卷 題型:填空題
草酸(H2C2O4)是一種重要的化工原料。已知常溫下0.01 mol·L-l的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示。
| | H2C2O4 | KHC2O4 | K2C2O4 |
| pH | 2.0 | 3.1 | 8.1 、 |
| A.加入適量的H2C2O4 | B.加入適量的KHC2O4 |
| C.加入適量的Na2C2O4 | D.升高溶液的溫度 |
 mol·L-l NaOH溶液至20.00 mL時,溶液由無色變為淺紅色;向第二份溶液中滴加適量3 mol·L-l H2S04溶液酸化后,用0.10 mol·L-l KMnO4溶液滴定,當消耗KMnO4溶液16.00 mL時,溶液由無色變為淺紫紅色。請回答下列問題:
mol·L-l NaOH溶液至20.00 mL時,溶液由無色變為淺紅色;向第二份溶液中滴加適量3 mol·L-l H2S04溶液酸化后,用0.10 mol·L-l KMnO4溶液滴定,當消耗KMnO4溶液16.00 mL時,溶液由無色變為淺紫紅色。請回答下列問題: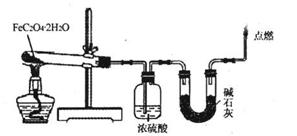
查看答案和解析>>
科目:高中化學 來源:2012-2013學年廣東省清遠市高三上學期期末檢測理綜化學試卷(解析版) 題型:實驗題
不久前,一則“食用撒了魚浮靈的魚蝦可能致癌”的微博在網上熱傳。“魚浮靈”的化學成分實為過碳酸鈉,使用不當會讓魚損傷,過碳酸鈉本身無毒無害,對人體不會有危害。過碳酸鈉,俗稱固體雙氧水,化學式為2Na2CO3·3H2O2,是一種無機鹽,是白色顆粒狀粉末,可以分解為碳酸鈉和過氧化氫。某探究小組制備過碳酸鈉并測定樣品中H2O2的含量,其制備流程和裝置示意圖如下:

已知:50 °C時 2Na2CO3·3H2O2 (s) 開始分解
主反應 2Na2CO3
(aq) + 3H2O2 (aq) 2Na2CO3·3H2O2
(s) ΔH < 0
2Na2CO3·3H2O2
(s) ΔH < 0
副反應 2H2O2 = 2H2O + O2↑
滴定反應 6KMnO4 + 5(2Na2CO3·3H2O2) +19H2SO4 = 3K2SO4 + 6MnSO4+10Na2SO4 + 10CO2 ↑ + 15O2↑ + 34H2O

根據以上信息回答下列問題:
(1)推測圖中支管的作用可能是 。
(2)步驟①的關鍵是控制溫度,結合裝置圖歸納其措施有 、
和 。
(3)在濾液X中加入適量NaCl固體或無水乙醇均可析出過碳酸鈉,原因是 。
(4)步驟③中選用無水乙醇洗滌產品的目的是 。
(5)測定樣品中H2O2的質量分數的方法是:準確稱取0.2000g過碳酸鈉樣品于250 mL 錐形瓶中,加50 mL 蒸餾水溶解,再加50 mL 2.000 mol·L-1 H2SO4 (H2SO4過量),用0.002000mol·L-1 KMnO4 標準溶液滴定至終點時消耗30.00 mL。
①滴定前,滴定管需用KMnO4標準溶液潤洗2~3次,潤洗的操作方法是:關閉酸式滴定管活塞,向滴定管中注入少量KMnO4標準 。
②上述樣品中H2O2的質量分數計算表達式為 (只列出算式,不作任何運算!H2O2的式量為34.00)。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年江蘇省姜堰市高三上學期學情調查(三)化學試卷 題型:填空題
草酸(H2C2O4)是一種重要的化工原料。已知常溫下0.01 mol·L-l的H2C2O4、KHC2O4、K2C2O4溶液的pH如下表所示。
|
|
H2C2O4 |
KHC2O4 |
K2C2O4 |
|
pH |
2.0 |
3.1 |
8.1 、 |
(1)在其它條件不變時,下列措施能使KHC2O4溶液中c(K+):c(HC2O4-)接近1:1的是_________(填字母)。
A.加入適量的H2C2O4 B.加入適量的KHC2O4
C.加入適量的Na2C2O4 D.升高溶液的溫度
(2)取一定質量H2C2O4·2H2O和KHC2O4的混合物,加水溶解,配成250 mL溶液,取兩份此溶液各25 mL,向第一份溶液中先加入幾滴酚酞試液,再滴加0.25 mol·L-l NaOH溶液至20.00 mL時,溶液由無色變為淺紅色;向第二份溶液中滴加適量3 mol·L-l H2S04溶液酸化后,用0.10 mol·L-l KMnO4溶液滴定,當消耗KMnO4溶液16.00 mL時,溶液由無色變為淺紫紅色。請回答下列問題:

①完成離子方程式:5C2O42-+2MnO4-+16H+ =10______+2Mn2++8H2O。
②原混合物中H2C2O4·2H2O和KHC2O4的物質的量之比為__________。
(3)某實驗小組用如圖所示的裝置探究FeC2O4·2H2O在隔絕空氣條件下受熱分解的產物。當36.0g FeC2O4·2H2O充分反應后,殘留固體質量為13.6g,濃硫酸增重7.2g,堿石灰增重11.0g。求殘留固體的成分和物質的量。(已知FeC2O4·2H2O的相對分子質量為180;設反應產生的氣體被充分吸收)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com