
Ⅰ.常溫下,將除去表面氧化膜的Al、Cu片放入U形管作原電池的兩極,測得圖1所示原電池的電流強度(I)隨時間(t)的變化如圖2所示,反應過程中有紅棕色氣體產生。
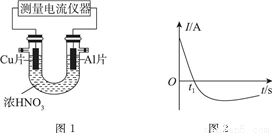
(1)0~t1時,原電池的負極是Al片,此時,正極的電極反應式是________。溶液中的H+向________(填“正”或“負”)極移動。
(2)t1時,原電池中電子流動方向發生改變,其原因是________。
Ⅱ.下圖所示電化學裝置中,a為足量的電解質溶液,X、Y是兩塊電極板。
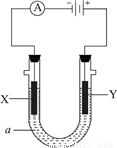
請回答:
(3)若X、Y都是石墨電極,a是含有酚酞的飽和NaCl溶液,則在X電極附近觀察到的現象是________,檢驗Y電極上反應產物的化學方法及實驗現象是________,電解池總反應的離子方程式為________。
 優化作業上海科技文獻出版社系列答案
優化作業上海科技文獻出版社系列答案科目:高中化學 來源:2016~2017學年江蘇省宿遷市高二學業水平測試模擬(二)化學試卷(解析版) 題型:選擇題
下列物質互為同分異構體的一組是
A. 白磷和紅磷 B. H2O和H2O2 C. 1H和2H D. CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年廣東省湛江市高二上學期期末調研考試化學試卷(解析版) 題型:選擇題
下列各組離子能大量共存且溶液顏色為無色的是
A. Na+、MnO4-、K+、NO3-、SO32- B. Na+、S2-、SO32-、H+、、NO3-
C. Na+、S2-、OH-、K+、Cl- D. HCO3-、H+、Na+、Ca2+、SO32-
查看答案和解析>>
科目:高中化學 來源:2016-2017學年福建省漳州市高二上學期期末考試化學試卷(解析版) 題型:選擇題
在恒容密閉容器中,用銅鉻的氧化物作催化劑,用一定量的HCl(g)和O2制取Cl2的原理為:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ΔH<0。下列有關說法不正確的是
2Cl2(g)+2H2O(g) ΔH<0。下列有關說法不正確的是
A. 平衡前,隨著反應的進行,容器內壓強變小
B. 平衡時,其他條件不變,分離出H2O(g),逆反應速率減小
C. 平衡時,其他條件不變,升高溫度平衡常數增大
D. 其他條件不變,使用不同催化劑,HCl(g)的轉化率不變
查看答案和解析>>
科目:高中化學 來源:2016-2017學年福建省漳州市高二上學期期末考試化學試卷(解析版) 題型:選擇題
H2S(g)+ O2(g)===SO2(g)+H2O(g)ΔH1
O2(g)===SO2(g)+H2O(g)ΔH1
2H2S(g)+SO2(g)=== S2(g)+2H2O(g)ΔH2
S2(g)+2H2O(g)ΔH2
H2S(g)+ O2(g)===S(g)+H2O(g)ΔH3 2S(g)===S2(g)ΔH4
O2(g)===S(g)+H2O(g)ΔH3 2S(g)===S2(g)ΔH4
則ΔH4的正確表達式為
A. ΔH4= (ΔH1+ΔH2-3ΔH3) B. ΔH4=
(ΔH1+ΔH2-3ΔH3) B. ΔH4= (3ΔH3-ΔH1-ΔH2)
(3ΔH3-ΔH1-ΔH2)
C. ΔH4= (ΔH1+ΔH2-3ΔH3) D. ΔH4=
(ΔH1+ΔH2-3ΔH3) D. ΔH4= (ΔH1-ΔH2-3ΔH3)
(ΔH1-ΔH2-3ΔH3)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省張家口市高二上學期期末考試化學試卷(解析版) 題型:選擇題
利用三室式電解池(裝置結構如圖所示,電極均為惰性電極)可以實現用硫酸鈉溶液制取硫酸和氫氧化鈉。下列敘述正確的是
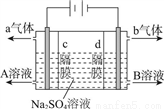
A. a氣體為氫氣,b氣體為氧氣
B. A為氫氧化鈉溶液,B為硫酸溶液
C. 通電后中問隔室的SO42-向陰極遷移,陽極區溶液的pH增大
D. 該電解反應的方程式為2Na2SO4+6H2O 2H2SO4+4NaOH+O2↑+2H2↑
2H2SO4+4NaOH+O2↑+2H2↑
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省張家口市高二上學期期末考試化學試卷(解析版) 題型:選擇題
在一體積可變的密閉容器中,加入一定量的X、Y、Z,發生反應mX(g)+nY(g)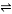 pZ(g)ΔH=QkJ·mol-1。反應達到平衡后,Y的物質的量濃度與溫度、容器體積的關系如下表所示。
pZ(g)ΔH=QkJ·mol-1。反應達到平衡后,Y的物質的量濃度與溫度、容器體積的關系如下表所示。
容器體積/L c(Y)/(mol·L-1) 溫度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
下列說法不正確的是
A. m+n>p
B. Q<0
C. 體積不變,溫度升高,平衡向逆反應方向移動
D. 溫度不變,壓強增大,Y的質量分數增大
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省張家口市高一上學期期末考試化學試卷(解析版) 題型:簡答題
研究或認識物質的化學性質一般可從以下幾個方面入手(以SiO2為例):
(1)從物質類別角度分析可能具有的通性,如酸性、堿性等。
SiO2屬于________氧化物(填“酸性”“堿性”或“兩性”)。盛裝NaOH等堿性溶液的試劑瓶不能用玻璃塞,其原因可用離子方程式表示為________。
(2)從核心元素化合價角度分析可能具有的氧化性、還原性。
據SiO2中Si元素的價態可推知SiO2________(填字母):
A.只有還原性 B.只有氧化性 C.既有還原性又有氧化性。
工業上用石英砂和焦炭混合高溫制取含少量雜質的粗硅,寫出該反應的化學方程式________。
(3)從其他角度認識可能具有的特性。
SiO2能與唯一的酸________(填物質名稱)反應,工藝上常利用該反應________(填一種用途)。
查看答案和解析>>
科目:高中化學 來源:2017屆山西省名校高三下學期聯考理綜化學試卷(解析版) 題型:推斷題
芳香醛廣泛存在于植物中,這類物質性質活潑,是合成染料、香料及藥品的重要中間體,具有較大的工業價值。
已知:①芳香醛在堿作用下,可以發生自身氧化還原反應,生成相應的醇和羧酸。
②不飽和碳碳鍵上連有羥基不穩定。
③化合物A、B、C、D、E、F之間的轉化關系如圖36所示。其中,化合物A含有醛基, E和F是同分異構體,F能與金屬鈉反應放出氫氣。A生成F的過程中,A物質間只有醛基參與反應,經紅外光譜分析,F物質中含有兩種常見的含氧官能團。
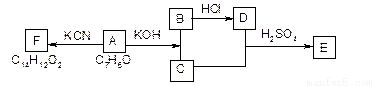
根據題目描述的信息,請你回答下列問題:
(1)寫出C和D生成E的反應方程式:__________________________________________ 。
(2)A生成B和C的反應是_______,C和D生成E的反應是_________。
①.氧化反應 ②.加成反應 ③.消去反應 ④.酯化反應 ⑤.還原反應
(3)F結構簡式是:______________________________________ 。
(4)F不可能發生的反應有_______。
①.氧化反應 .加成反應 ③.消去反應 ④.酯化反應 ⑤.還原反應
(5)G物質是A物質的同系物,分子式是C9H10O。G物質苯環上含有兩個取代基是與A含有相同官能團的同分異構體共用________種,寫出其中一種的結構簡式___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com