
| 實驗方法 | 實驗現象 | 結論 |
| 步驟1:在濾液中加入c(填字母) | 液變成血紅色 | 濾液中有Fe3+ |
| 步驟2:在濾液中加入a(填字母) | 紫紅色褪去 | 濾液中有Fe2+ |
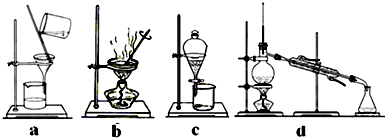
分析 用過量的FeCl3溶液溶解電路板中的銅箔時,會產生大量廢液,則廢液中含FeCl3、FeCl2、CuCl2.
Ⅰ.在廢液中加入過量鐵粉,則會與FeCl3反應生成FeCl2,與CuCl2反應生成FeCl2和Cu,過濾,則濾液中含FeCl2;濾渣中含Cu和過量的Fe粉;
Ⅱ.I的濾渣中含Cu和過量的Fe粉,向I的濾渣中加入過量試劑A,充分反應后,過濾,得到銅,故加入的試劑A只能將鐵反應掉,則A為鹽酸,所得的溶液中含FeCl2;
Ⅲ.I和II中的濾液中均為FeCl2,通入足量氯氣,反應生成FeCl3;
Ⅳ.加熱蒸發、濃縮結晶,得到FeCl3•6H2O晶體.據此分析.
解答 解:用過量的FeCl3溶液溶解電路板中的銅箔時,會產生大量廢液,則廢液中含FeCl3、FeCl2、CuCl2.
Ⅰ.在廢液中加入過量鐵粉,則會與FeCl3反應生成FeCl2,與CuCl2反應生成FeCl2和Cu,過濾,則濾液中含FeCl2;濾渣中含Cu和過量的Fe粉;
Ⅱ.I的濾渣中含Cu和過量的Fe粉,向I的濾渣中加入過量試劑A,充分反應后,過濾,得到銅,故加入的試劑A只能將鐵反應掉,則A為鹽酸,所得的溶液中含FeCl2;
Ⅲ.I和II中的濾液中均為FeCl2,通入足量氯氣,反應生成FeCl3;
Ⅳ.加熱蒸發、濃縮結晶,得到FeCl3•6H2O晶體.
(1)銅與氯化鐵反應生成氯化鐵、氯化亞鐵,化學方程式為:2FeCl3+Cu═2 FeCl2+CuCl2,所以離子方程式是Cu+2Fe3+=Cu2++2Fe2+,故答案為:Cu+2Fe3+=Cu2++2Fe2+;
(2)試劑A只能將鐵反應掉,不反應銅,且不能引入雜質離子,故A為鹽酸,故答案為:鹽酸;
(3)在濾液中加入KSCN溶液,溶液變血紅色,說明濾液中有Fe3+,在濾液中加入酸性KMnO4,如果紫紅色褪去,說明溶液中存在亞鐵離子,故答案為:
| 實驗方法 | 實驗現象 | 結論 |
| 步驟1:在濾液中加入 c(填字母) | 液變成血紅色 | 濾液中有Fe3+ |
| 步驟2:在濾液中加入 a(填字母) | 紫紅色褪去 | 濾液中有Fe2+ |
點評 本題考查了氯化鐵來腐蝕電路銅板的反應和所需試劑的推導,難度不大,應注意的是由溶液獲得帶結晶水的晶體的方法.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
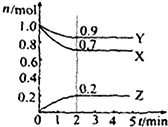 某溫度時在2L容器中X、Y、Z三種物質的物質的量(n)隨時間(t)變化的曲線如圖所示,圖中數據分析:
某溫度時在2L容器中X、Y、Z三種物質的物質的量(n)隨時間(t)變化的曲線如圖所示,圖中數據分析:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色溶液:Na+、K+、SO42-、MnO4- | |
| B. | pH=1的溶液中:Fe2+、SO42-、Cl-、NO3- | |
| C. | 使酚酞變紅的溶液:Na+、Cl-、SO42-、Fe3+、 | |
| D. | 水電離出的c(H+)=1×10-12mol/L的溶液:K+、Cl-、Ba2+、Br- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 陽離子 | Na+、K+、Cu2+ |
| 陰離子 | SO${\;}_{4}^{2-}$、OH- |
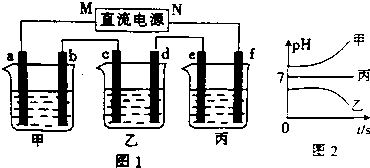
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ||
| 3 | ⑧ | ⑨ | ⑩ |

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲基橙呈黃色的溶液中:K+、Na+、SO42-、S2O32- | |
| B. | 能與Al反應生成H2的溶液:Na+、Ba2+、NO3-、I- | |
| C. | 常溫下水電離出的OH-為1×10-7mol/L的溶液中:K+、Na+、SO42-、AlO2- | |
| D. | 常溫下pH=7的溶液中:NH4+、K+、CH3COO-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl-、NO3-、Fe3+、Na+ | B. | Ag+、NO3-、Cl-、K+ | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向以上平衡體系中加入足量濃NaOH溶液,兩平衡都向右移動,Al(OH)3的質量增加 | |
| B. | 向以上平衡體系中加入足量濃鹽酸,Al3+的物質的量增加 | |
| C. | 在同一溶液中,Al3+與OH-能大量共存 | |
| D. | 在同一溶液中,AlO2-與H+能大量共存 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com