
【題目】N,P,As等元素的化合物在生產和研究中有許多重要用途。請回答下列問題:
(1)意大利羅馬大學的FuNvio Cacace等人獲得了極具理論研究意義的N4分子,該分子的空間構型與P4類似,其中氮原子的軌道雜化方式為_______,N—N鍵的鍵角為____。
(2)基態砷原子的價電子排布圖為_______,砷與同周期相鄰元素的第一電離能由大到小的順序為______。
(3)配位原子對孤對電子的吸引力越弱,配體越容易與過渡金屬形成配合物。![]() 與
與![]() 的結構相似,和過渡金屬更容易形成配合物的是__________
的結構相似,和過渡金屬更容易形成配合物的是__________![]() 填PH4”或“
填PH4”或“![]() ”
”![]() 。
。
(4)SCl3+和![]() 是等電子體,
是等電子體,![]() 的空間構型是_________。
的空間構型是_________。![]() 鍵鍵長____
鍵鍵長____![]() 鍵鍵長
鍵鍵長![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ,原因是____________。
,原因是____________。
【答案】sp3 60° ![]() As>Se>Ge PH3 三角錐形 < S 原子半徑小于P原子半徑,故 S-Cl 鍵要比 P-Cl 鍵短
As>Se>Ge PH3 三角錐形 < S 原子半徑小于P原子半徑,故 S-Cl 鍵要比 P-Cl 鍵短
【解析】
(1)N4分子的空間構型與P4類似,4個N原子形成正四面體構型,每個N原子形成3個N-N鍵,還含有1對孤對電子;
(2)As元素處于第四周期VA族,價電子排布式為4s24p3,結合泡利原理、洪特規則畫出價電子排布圖;As原子4p軌道為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素的;
(3)元素的電負性越小,對孤電子對吸引越弱,越容易形成配位鍵;
(4)PCl3中P原子形成3個P-Cl鍵,含有1對孤對電子,其空間結構三角錐形,而等電子體的結構相似;原子半徑越小,原子之間形成的共價鍵越短。
(1)N4分子的空間構型與P4類似,4個N原子形成正四面體構型,每個N原子形成3個N-N鍵,還含有1對孤對電子,雜化軌道數目為4,故N原子采取sp3雜化,每個面均為正三角形,故N-N鍵的鍵角為60°;
(2)As元素處于第四周期VA族,價電子排布式為4s24p3,價電子排布圖為:![]() ,As原子4p軌道為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素的,故第一電離能:As>Se>Ge;
,As原子4p軌道為半滿穩定狀態,能量較低,第一電離能高于同周期相鄰元素的,故第一電離能:As>Se>Ge;
(3)P元素的電負性比N元素的小,P原子對孤電子對吸引更弱,容易給出孤對電子形成配位鍵;
(4)PCl3中P原子形成3個P-Cl鍵,含有1對孤對電子,其空間結構三角錐形,而等電子體的結構相似,SCl3+的空間構型是三角錐形, S 原子半徑小于P原子半徑,故 S-Cl 鍵要比 P-Cl 鍵短。


 活力試卷系列答案
活力試卷系列答案 課課優能力培優100分系列答案
課課優能力培優100分系列答案科目:高中化學 來源: 題型:
【題目】在相同溫度下(T=500K),有相同體積的甲、乙兩容器,且保持體積不變,甲容器中充入1gSO2和1gO2,乙容器中充入2gSO2和2gO2。下列敘述中錯誤的是( )
A.化學反應速率:乙>甲B.平衡時O2的濃度:乙>甲
C.平衡時SO2的轉化率:乙>甲D.平衡時SO2的體積分數:乙>甲
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列生產生活等實際應用中,不能用勒夏特列原理解釋的是( )
A. 新制氯水中存在平衡Cl2+H2O ![]() HCl+ HClO,當加入AgNO3溶液后溶液顏色變淺
HCl+ HClO,當加入AgNO3溶液后溶液顏色變淺
B. 使用更有效的催化劑,提高可逆反應的轉化率
C. 工業合成NH3是放熱反應,為提高NH3的產率,理論上應采取低溫的措施
D. 工業生產硫酸的過程中使用過量的空氣以提高二氧化硫的利用率(2SO2+O2![]() 2SO3)
2SO3)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列現象或事實可用同一原理解釋的是![]()
A.濃硫酸和濃鹽酸長期暴露在空氣中濃度降低
B.![]() 和
和![]() 溶液使酸性高錳酸鉀的紫色褪去
溶液使酸性高錳酸鉀的紫色褪去
C.漂白粉和水玻璃長期暴露在空氣中變質
D.亞硫酸鈉溶液和氯化鋁溶液在空氣中蒸干不能得到對應的溶質
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學在生產和日常生活中有著重要的應用。下列說法正確的是![]()
![]()
A.明礬、鐵鹽均可以對水起凈化作用
B.向煤中加入適量石灰石,使煤燃燒產生的![]() 最終生成
最終生成![]() ,以減少對大氣的污染
,以減少對大氣的污染
C.高純度的硅單質廣泛用于制作光導纖維
D.如果得了胃潰瘍,可服用小蘇打得以緩解
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)Al2(SO4)3溶液加熱蒸干并灼燒最終得到物質是________________(填化學式),將NaHCO3與Al2(SO4)3兩者溶液混合后可做泡沫滅火劑,其原理是_____________________(用離子方程式表示)
(2)實驗室溶液中常用NaOH來進行洗氣和提純。當100mL 1mol·L-1的NaOH溶液吸收標準狀況下2.24LSO2時,所得溶液中各離子濃度由大到小的順序為____________________________
(3)25℃時,幾種離子開始沉淀時的pH如下表:
離子 | Fe2+ | Cu2+ | Mg2+ |
pH | 7.6 | 5.2 | 10.4 |
當向含相同濃度Cu2+、Mg2+、Fe2+的溶液中滴加NaOH溶液時,_____先沉淀(填離子符號),要使0.3mol·L-1硫酸銅溶液中Cu2+沉淀較為完全(當Cu2+濃度降至10-5 mol·L-1時),則應向溶液里加入氫氧化鈉溶液使溶液pH為____(KspCu(OH)2=1×10-20)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】pH=2的A、B兩種一元酸溶液各1mL, 分別加水稀釋到1000mL,其溶液的pH與溶液體積(V)的關系如圖所示, 則下列說法正確的是
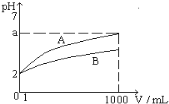
A. A、B兩種酸溶液物質的量濃度一定相等
B. 稀釋后A酸溶液的酸性比B酸溶液強
C. a = 5時, A是弱酸, B是強酸
D. 若A、B都是弱酸, 則5 > a > 2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗現象或圖像信息不能充分說明相應的化學反應是放熱反應的是
A | B | C | D | |
圖示 |
|
|
|
|
相關 信息 | 溫度計的水銀柱不斷上升 | 反應物總能量大于生成物總能量 | 反應開始后,甲處液面低于乙處液面 | 反應開始后,針筒活塞向右移動 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,濃度都是1mol·L-1的兩種氣體X2和Y2在密閉容器中反應,經過tmin后,測得物質的濃度分別為:c(X2)=0.4mol·L-1,c(Y2)=0.8mol·L-1,則該反應的方程式可表示為()
A. X2+2Y2![]() 2XY2B. 2X2+Y2
2XY2B. 2X2+Y2![]() 2X2Y
2X2Y
C. X2+3Y2![]() 2XY3D. 3X2+Y2
2XY3D. 3X2+Y2![]() 2X3Y
2X3Y
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com