
下列關于有機物的敘述正確的是
A. 石油干餾可得到汽油、煤油等
B. 乙酸乙酯、油脂與NaOH溶液反應均有醇生成
C. 淀粉、蛋白質完全水解的產物互為同分異構體
D. 苯不能使酸性KMnO4溶液褪色,因此苯不能發生氧化反應
科目:高中化學 來源:2017屆山東省淄博市高三第一次模擬考試化學試卷(解析版) 題型:填空題
硼及其化合物在工農業生產中應用廣泛。
(1)基態硼原子的核外電子排布式為__________,有_______種不同能量的電子。
(2)BF3溶于水后.在一定條件下可轉化為H3O+·[B(OH)F3]-,該物質中陽離子的空間構型為_____________,陰離子的中心原子軌道采用________雜化。
(3)與BH4-互為等電子休的分子是_______________(寫化學式)。
(4)EminBF4的熔點為12 ℃,在常溫下為液體,由有機物陽離子[Emin]+和[BF4]-構成。該物質的晶體屬于_________晶體。
(5)一種由硼和釤(Sm)形成的晶體的晶胞結構如圖所示,已知晶胞常數a=n pm,則晶體的密度為_____________g·cm-3(設NA為阿伏伽德羅常數的值)。
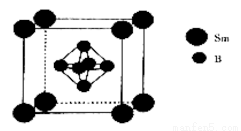
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省黃岡市高三第三次聯考理綜化學試卷(解析版) 題型:實驗題
亞氯酸鈉(NaClO2)和ClO2都是重要的漂白劑。通常情況下,ClO2是一種具有強氧化性的黃色氣體,常用于水的凈化和紙漿、紡織品的漂白。ClO2易發生爆炸,在生產、使用時可用其它氣體進行稀釋。ClO2易與堿反應生成亞氯酸鹽和氯酸鹽。
(1)草酸(H2C2O4)是一種弱酸,利用硫酸酸化的草酸還原氯酸鈉,可較安全地生成ClO2,反應的離子方程式為___________。
(2)自來水用ClO2處理后,有少量ClO2殘留在水中,可用碘量法作如下檢測(已知ClO2存在于pH為4~6的溶液中,ClO2-存在于中性溶液中):
①取0.50L水樣,加入一定量的碘化鉀,用氫氧化鈉溶液調至中性,再加入淀粉溶液,溶液變藍。寫出ClO2與碘化鉀反應的化學方程式_____________。
②已知:2Na2S2O3+I2=Na2S4O6+2NaI,向①所得溶液中滴加5.00×10-4mol·L-1的Na2S2O3溶液至恰好反應,消耗Na2S2O3溶液20.00ml,判斷達到滴定終點的方法是_________。該水樣中ClO2的濃度是___mg/L。
(3)某學習小組設計如下裝置進行制取亞氯酸鈉(NaClO2)。
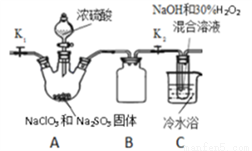
①裝置A中產生的ClO2氣體,在裝置C中反應生成NaClO2,寫出生成NaClO2的化學方程式為_______。將NaClO2溶液在一定條件下處理即可得到NaClO2晶體。
②裝置B的作用是____________。
③某同學認為上述裝置并不完整,請畫出需補充的裝置圖____________。
查看答案和解析>>
科目:高中化學 來源:2017屆河南省南陽、信陽等六市高三第一次聯考理綜化學試卷(解析版) 題型:選擇題
下列有關性質的比較,不能用元素周期律解釋的是
A. 堿性:KOH>NaOH B. 金屬性:Na>Al
C. 穩定性:HF>CH4 D. 酸性:HClO<HClO4
查看答案和解析>>
科目:高中化學 來源:2017屆安徽省淮南市高三第一次模擬考試理綜化學試卷(解析版) 題型:實驗題
在實驗室中模擬工業制取NaHCO3的實驗步驟如下:
第一步:連接好裝置,檢驗氣密性,在儀器內裝入藥品。
第二步:先讓某一裝置發生反應,直到產生的氣體不能再在C中溶解,再通入另一裝置中產生的氣體,片刻后,C中出現固體。繼續向C中通入兩種氣體,直到不再有固體產生。
第三步:分離C中所得的混合物,得到NaHCO3固體。
第四步:向濾液中加入適量的某固體粉末,有NH4Cl晶體析出。
(1)下圖所示裝置的連接順序是:a接________;________接_______;b接_________(填接口編號)。
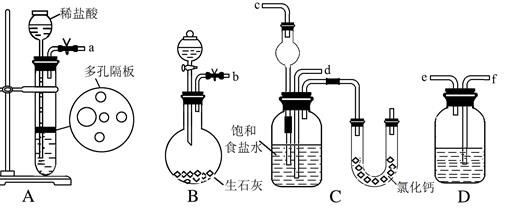
(2)A中常選用的固體反應物為_______________;D中應選用的液體為________________。
(3)第二步中讓___________裝置先發生反應。
(4)C中用球形干燥管而不用直導管,其作用是______________________;裝有無水CaCl2的U形管的作用是_________________________。
(5)第三步分離出NaHCO3固體的操作是________________。
(6)第四步中所加固體粉末化學式為 。所得的晶體中常含有少量的NaCl和NaHCO3(約占5%~8%),請設計一個簡單的實驗,不使用其他任何試劑,證明所得晶體大部分是NH4C1。簡要寫出操作和現象_____________________。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省常州市高三第一次模擬考試化學試卷(解析版) 題型:實驗題
過硫酸鉀(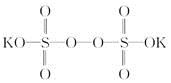 )具有強氧化性(常被還原為硫酸鉀),80℃以上易發生分解。實驗室模擬工業合成過硫酸鉀的流程如下:
)具有強氧化性(常被還原為硫酸鉀),80℃以上易發生分解。實驗室模擬工業合成過硫酸鉀的流程如下:
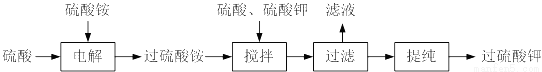
(1)硫酸銨和硫酸配制成電解液,以鉑作電極進行電解,生成過硫酸銨溶液。寫出電解時發生反應的離子方程式___________________。
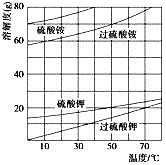
(2)已知相關物質的溶解度曲線如下圖所示。在實驗室中提純過硫酸鉀粗產品的實驗具體操作依次為:將過硫酸鉀粗產品溶于適量水中,___________,干燥。
(3)樣品中過硫酸鉀的含量可用碘量法進行測定。實驗步驟如下:
步驟1:稱取過硫酸鉀樣品0.3000g于碘量瓶中,加入30 mL水溶解。
步驟2:向溶液中加入4.000g KI固體(略過量),搖勻,在暗處放置30 min。
步驟3:在碘量瓶中加入適量醋酸溶液酸化,以淀粉溶液作指示劑,用0.1000mol·L-1Na2S2O3標準溶液滴定至終點,共消耗Na2S2O3標準溶液21.00mL。
(已知反應:I2+2S2O32-=2I-+S4O62-)
①若步驟2中未將碘量瓶“在暗處放置30 min”,立即進行步驟3,則測定的結果可能__________(選填“偏大”、“偏小”、“無影響”);上述步驟3中滴定終點的現象是__________。
②根據上述步驟可計算出該樣品中過硫酸鉀的質量分數為__________。
③為確保實驗結果的準確性,你認為還需要____________________。
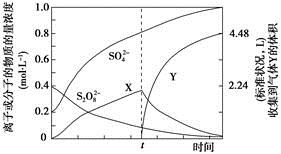
(4)將0.40mol過硫酸鉀與0.20mol硫酸配制成1 L溶液,在80℃條件下加熱并在t時刻向溶液中滴加入少量FeCl3溶液,測定溶液中各成分的濃度如圖所示(H+濃度未畫出)。圖中物質X的化學式為
__________。
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省常州市高三第一次模擬考試化學試卷(解析版) 題型:選擇題
我國科學家屠喲喲因創制新型抗瘧藥——青篙素和雙氫青篙素而分享了2015 年諾貝爾生理學或醫學獎。青篙素和雙氫青篙素的結構如下,下列說法正確的是( )
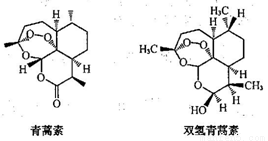
A. 青篙素的分子式為C16H24O5
B. 兩種分子中所含的手性碳原子數目相同
C. 雙氫青篙素在一定條件下可發生消去反應
D. 兩種分子中均含有過氧鍵(-O-O-),一定條件下均可能具有較強的氧化性
查看答案和解析>>
科目:高中化學 來源:2017屆山東省臨沂市高三上學期期末考試化學試卷(解析版) 題型:選擇題
25℃時,向盛有50mL pH=2的HA溶液的絕熱容器中加入pH=13的NaOH溶液,加入NaOH溶液的體積(V)與所得混合溶液的溫度(T)的關系如圖所示。下列敘述正確的是( )

A. HA溶液的物質的量濃度為0.0l mol·L—1
B. b→c的過程中,溫度降低的原因是溶液中發生了吸熱反應
C. a→b的過程中,混合溶液中可能存在:c(A-)=c(Na+)
D. 25℃時,HA的電離平衡常數K約為1.43×10—2
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省濟南市高一下學期開學考試化學試卷(解析版) 題型:選擇題
下列有關廚房鋁制品的使用中,你認為合理的是( )
A. 盛放食醋 B. 用堿液洗滌
C. 燒制開水 D. 用金屬絲擦洗表面污垢
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com