
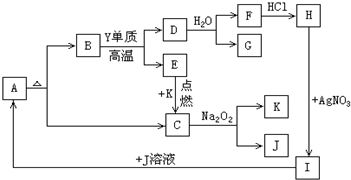
分析 C是氣體,能與過氧化鈉反應生成氣體K和物質J,則可知C為CO2,K為O2,J為Na2CO3,氣體E在氧氣中點燃生成CO2,所以E為CO,非金屬單質Y與B在高溫下反應生成D和E,則Y應為C,B為應為二價金屬元素X的化合物,根據A受熱分解生成B和二氧化碳,可知A為CaCO3,B為CaO,CaO與碳反應生成D為CaC2,CaC2與水反應生成F為Ca(OH)2,氣體G為C2H2,F與氯化氫反應生成H為CaCl2,CaCl2與硝酸銀反應生成I為Ca(NO3)2,I與Na2CO3反應生成碳酸鈣,符合各物質的轉化關系,據此答題;
解答 解:C是氣體,能與過氧化鈉反應生成氣體K和物質J,則可知C為CO2,K為O2,J為Na2CO3,氣體E在氧氣中點燃生成CO2,所以E為CO,非金屬單質Y與B在高溫下反應生成D和E,則Y應為C,B為應為二價金屬元素X的化合物,根據A受熱分解生成B和二氧化碳,可知A為CaCO3,B為CaO,CaO與碳反應生成D為CaC2,CaC2與水反應生成F為Ca(OH)2,氣體G為C2H2,F與氯化氫反應生成H為CaCl2,CaCl2與硝酸銀反應生成I為Ca(NO3)2,I與Na2CO3反應生成碳酸鈣,符合各物質的轉化關系,
(1)根據上面的分析可知,元素X為Ca,元素Y的名稱為碳,
故答案為:Ca;碳;
(2)CaC2與水反應生成Ca(OH)2和C2H2,反應的化學方程式為CaC2+2H2O→C2H2↑+Ca(OH)2,
故答案為:CaC2+2H2O→C2H2↑+Ca(OH)2;
(3)反應C→K+J為二氧化碳與過氧化鈉反應生成氧氣和碳酸鈉,反應的化學方程式為2CO2+2Na2O2=2Na2CO3+O2,
故答案為:2CO2+2Na2O2=2Na2CO3+O2;
(4)J為Na2CO3,能與CaO、Ca(OH)2、CaCl2等反應生成CaCO3,
故答案為:B、F、H;
點評 本題考查無機物推斷,涉及C、Na元素化合物性質,物質的性質及相互轉化關系是推斷突破口,題目綜合性較強,難度中等,需要學生熟練掌握元素化合物知識,對學生綜合思維能力要求較高.


 全程金卷系列答案
全程金卷系列答案 快樂5加2金卷系列答案
快樂5加2金卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | Mg2+的結構示意圖: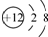 | |
| B. | 葡萄糖的結構簡式:C6H12O6 | |
| C. | H2O2的電子式: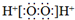 | |
| D. | 硫酸的電離方程式:H2SO4═H22++SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
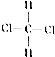 和
和 ⑧乙烷和戊烷
⑧乙烷和戊烷查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1種 | B. | 2種 | C. | 3種 | D. | 4種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 有5.6 g金屬被腐蝕 | B. | 有6.5 g金屬被氧化 | ||
| C. | 有0.15 mol金屬失去電子 | D. | 標準狀況下有4.48 L H2逸出 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
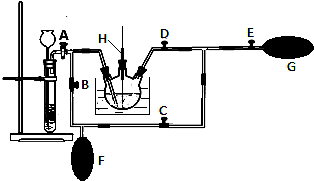
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 實驗編號 | 試管a中試劑 | 試管b中試劑 | 測得有機層的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL18mol•L-1 濃硫酸 | 飽和Na2CO3溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol•L-1 H2SO4 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、鹽酸 | 1.2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
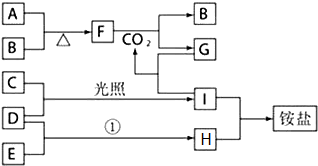 某興趣小組的同學發現《高中化學(必修1)》中學習的單質及其化合物(或其溶液)存在如圖的轉化關系,已知B、C、D、E是非金屬單質,且在常溫常壓下都是氣體;F為淡黃色粉末,化合物H和I通常狀況下呈氣體;反應①是化工生產中的一種重要固氮反應.
某興趣小組的同學發現《高中化學(必修1)》中學習的單質及其化合物(或其溶液)存在如圖的轉化關系,已知B、C、D、E是非金屬單質,且在常溫常壓下都是氣體;F為淡黃色粉末,化合物H和I通常狀況下呈氣體;反應①是化工生產中的一種重要固氮反應.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 降低溫度 | B. | 增大壓強 | C. | 充入一定量CO2 | D. | 再加入一些鐵粉 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com