
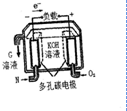
 已知短周期主族元素A、B、C、D、E的原子序數依次增大,A、C、D原子的最外層電子數之和為12,C、D、E位于同一周期,B、D同主族.D原子的最外層電子數既是A原子內層電子數的3倍又是C原子最外層電子數的3倍.請回答下列問題:
已知短周期主族元素A、B、C、D、E的原子序數依次增大,A、C、D原子的最外層電子數之和為12,C、D、E位于同一周期,B、D同主族.D原子的最外層電子數既是A原子內層電子數的3倍又是C原子最外層電子數的3倍.請回答下列問題: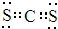 ,故答案為:第三周期ⅦA族;
,故答案為:第三周期ⅦA族;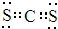 ;
;
| ||


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:
| A、用H2O2酸性溶液,將海帶灰中的I-轉變為I2:H2O2+2I-═I2+2OH- |
| B、高錳酸鉀與足量濃鹽酸反應制氯氣:2MnO4-+16H++10Cl-═2Mn2++5Cl2↑+8H2O |
| C、AlCl3溶液中滴加過量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| D、漂白粉溶液中,通入過量的二氧化碳:Ca2++2ClO-+CO2+H2O═CaCO3↓+2HClO |
查看答案和解析>>
科目:高中化學 來源: 題型:
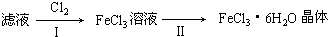
查看答案和解析>>
科目:高中化學 來源: 題型:
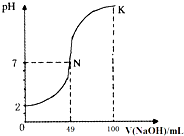 常溫下,向100mL0.1mol?L-1H2A(二元酸)溶液中逐滴加入0.2mol?L-1NaOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).下列有關說法正確的是( )
常溫下,向100mL0.1mol?L-1H2A(二元酸)溶液中逐滴加入0.2mol?L-1NaOH溶液,圖中所示曲線表示混合溶液的pH變化情況(體積變化忽略不計).下列有關說法正確的是( )| A、H2A為二元強酸 |
| B、K點時加水稀釋溶液,c(H+)增大 |
| C、N點對應溶液有:c(Na+)=c(A2-)+c(HA-) |
| D、K點對應溶液中離子濃度由大到小的順序為:c(A2-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:
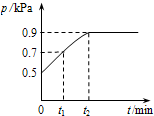 在1.0L密閉容器中放入0.10 mol X,在一定溫度下發生反應:X(g)?Y(g)+Z(g)△H<0容器內氣體總壓強p隨反應時間t的變化關系如圖所示.以下分析正確的是( )
在1.0L密閉容器中放入0.10 mol X,在一定溫度下發生反應:X(g)?Y(g)+Z(g)△H<0容器內氣體總壓強p隨反應時間t的變化關系如圖所示.以下分析正確的是( )A、從反應開始到t1時的平均反應速率v(X)=
| ||
| B、該溫度下此反應的平衡常數K=0.32 | ||
| C、欲提高平衡體系中Y的含量,可升高體系溫度或減少Z的量 | ||
| D、其他條件不變,再充入0.1 mol 氣體X,平衡正向移動,X的轉化率增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

| ||
 為碳原子,
為碳原子, 為硅原子).每個碳原子周圍與其距離最近的硅原子有
為硅原子).每個碳原子周圍與其距離最近的硅原子有查看答案和解析>>
科目:高中化學 來源: 題型:
| A、3:1 | B、2:5 |
| C、11:3 | D、4:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com