
一個電池的總反應:Zn+Cu2+=Zn2++Cu,該反應的原電池的正確組成是( )
|
科目:高中化學 來源: 題型:



查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
A、B、C、D、E、F、G、H八種元素分布在三個不同的短周期,它們的原子序數依次增大,其中B、C、D為同一周期,A與E,B與G,D與H分別為同一主族,C和D的最外層電子數之和為11,C、D、F三種元素的原子序數之和為28。請回答下列問題:
(1)B與D可形成非極性分子X,過量的X與F D2-溶液反應的離子方程式為____________________________。
(2)E、F、H所形成的簡單離子的半徑由大到小的順序為(用離子符號表示) 。
(3)G的最高價氧化物與B的單質在高溫下能發生置換反應,其化學反應方程式為:
。
(4)鹽Y由B、D、E組成。以熔融鹽Y為電解質構成的燃料電池如右圖所示。寫出石墨(I)電極上發生的電極反應式: 。

(5)用熔融鹽Y的燃料電池作電源,以石墨為電極,電解一定濃度的CuSO4溶液至無色后繼續電解一段時間。斷開電路,向溶液中加入0.1 mol Cu(OH)2,溶液恢復到電解之前的體積和濃度,則電解過程中轉移電子的物質的量為______。
(6)由A、C、D、E四種元素中任意三種構成的強電解質Z和W,溶于水時都能促進水的電離,測得Z的水溶液pH>7,W的水溶液pH<7,則Z為 、W為 。
(7)在一個裝有可移動活塞的容器中進行如下反應:C2(g)+3A2(g)![]() 2CA3(g),反應達到平衡后,測得容器中含有C2 0.5mol,A20.2mol,CA30.2mol,總容積為1.0L。
2CA3(g),反應達到平衡后,測得容器中含有C2 0.5mol,A20.2mol,CA30.2mol,總容積為1.0L。
①如果達成此平衡前各物質起始的量有以下幾種可能,其中不合理的是________:
A.C2 0.6mol, A2 0.5mol, CA30mol
B.C2 0mol, A2 0mol, CA3 1.2mol
C.C2 0.6mol/L,A2 0.5mol/L, CA3 0.1mol/L
②求算此平衡體系的平衡常數K=________;
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
A、B、C、D、E、F、G、H八種元素分布在三個不同的短周期,它們的原子序數依次增大,其中B、C、D為同一周期,A與E,B與G,D與H分別為同一主族,C和D的最外層電子數之和為11,C、D、F三種元素的原子序數之和為28。請回答下列問題:
(1)B與D可形成非極性分子X,過量的X與F D2-溶液反應的離子方程式為____________________________。
(2)E、F、H所形成的簡單離子的半徑由大到小的順序為(用離子符號表示) 。
(3)G的最高價氧化物與B的單質在高溫下能發生置換反應,其化學反應方程式為:
。
(4)鹽Y由B、D、E組成。以熔融鹽Y為電解質構成的燃料電池如右圖所示。寫出石墨(I)電極上發生的電極反應式: 。
(5)用熔融鹽Y的燃料電池作電源,以石墨為電極,電解一定濃度的CuSO4溶液至無色后繼續電解一段時間。斷開電路,向溶液中加入0.1mol Cu(OH)2,溶液恢復到電解之前的體積和濃度,則電解過程中轉移電子的物質的量為______。
(6)由A、C、D、E四種元素中任意三種構成的強電解質Z和W,溶于水時都能促進水的電離,測得Z的水溶液pH>7,W的水溶液pH<7,則Z為 、W為 。
(7)在一個裝有可移動活塞的容器中進行如下反應:C2(g)+3A2(g)![]() 2CA3(g),反應達到平衡后,測得容器中含有C2 0.5mol,A20.2mol,CA30.2mol,總容積為1.0L。
2CA3(g),反應達到平衡后,測得容器中含有C2 0.5mol,A20.2mol,CA30.2mol,總容積為1.0L。
①如果達成此平衡前各物質起始的量有以下幾種可能,其中不合理的是________:
A.C2 0.6mol, A2 0.5mol, CA30mol
B.C2 0mol, A2 0mol, CA3 1.2mol
C.C2 0.6mol/L,A2 0.5mol/L, CA3 0.1mol/L
②求算此平衡體系的平衡常數K=________;
查看答案和解析>>
科目:高中化學 來源:2013屆山東省高二下學期第一次月考化學試卷 題型:填空題
(16分)下圖是一個化學過程的示意圖。已知甲池的總反應式為:2CH3OH+3O2+4KOH
2K2CO3+6H2O
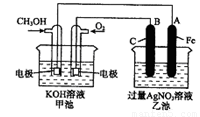
(1)請回答圖中甲、乙兩池的名稱。甲電池是 裝置,乙池是 裝置。
(2)請回答下列電極的名稱:通入CH3OH的電極名稱是 ,B(石墨)電極的名稱是 。
(3)寫出電極反應式:
通入O2的電極的電極反應式是 。
A(Fe)電極的電極反應式為 ,
(4)乙池中反應的化學方程式為 。[來源:Z&xx&k.Com]
(5)當乙池中A(Fe)極的質量增加5.40g時,甲池中理論上消耗O2 mL(標準狀況下)
查看答案和解析>>
科目:高中化學 來源: 題型:
I.光伏組件采用高效率單晶硅或多晶硅光伏電池、高透光率鋼化玻璃、抗腐蝕鋁合多邊框等材料,使用先進的真空層壓工藝及脈沖焊接工藝制造。
 (1)下圖是太陽能電池板經太陽光照射前后內部電子的變化情況,圖乙中燈泡變亮,其中____(填寫“N”或“P”)是正極。
(1)下圖是太陽能電池板經太陽光照射前后內部電子的變化情況,圖乙中燈泡變亮,其中____(填寫“N”或“P”)是正極。
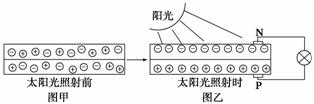
![]() (2)右上圖是一個太陽能路燈,圖中的④是蓄電池。鎳氫電池就是這樣一種與太陽能電池配套使用的蓄電池,白天用于充電,夜間供電。這種蓄電池容量大,充電放電循環壽命也較長。該蓄電池的總反應為Ni(OH)2 NiOOH+1/2H2↑。鎳氫電池的電解液采用30%的KOH溶液,白天充電反應時的陽極反應式為 ,夜間放電時,負極附近溶液的pH________(填“增大”、“減小”或“不變”)。
(2)右上圖是一個太陽能路燈,圖中的④是蓄電池。鎳氫電池就是這樣一種與太陽能電池配套使用的蓄電池,白天用于充電,夜間供電。這種蓄電池容量大,充電放電循環壽命也較長。該蓄電池的總反應為Ni(OH)2 NiOOH+1/2H2↑。鎳氫電池的電解液采用30%的KOH溶液,白天充電反應時的陽極反應式為 ,夜間放電時,負極附近溶液的pH________(填“增大”、“減小”或“不變”)。
 II.X、Y、Z、Q、R5種短周期元素原子序數依次增大。化合物甲由X、Z、Q3種元素組成,常溫下,0.1mol·L-l甲溶液的pH =13。工業上常用電解QR飽和溶液生產甲
II.X、Y、Z、Q、R5種短周期元素原子序數依次增大。化合物甲由X、Z、Q3種元素組成,常溫下,0.1mol·L-l甲溶液的pH =13。工業上常用電解QR飽和溶液生產甲
(3)Q的原子結構示意圖為
(4)常溫下將R的單質通人甲溶液中,發生反應的離子方程式為
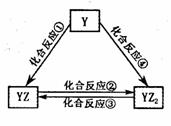
(5)若Y元素的單質能發生如右圖所示轉化,則Y元素是 。
已知:298K時,反應②生成1mol YZ2(g)時放出熱量283.O kJ·mol-1,
反應④生成1mol YZ2(g)時放出熱量393.5 kJ·mol-1,反應③的熱化學方程式為
。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com