
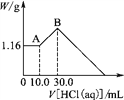
【題目】將NaOH、MgCl2、AlCl3三種固體組成的混合物溶于足量水后,產生1.16 g白色沉淀,再向所得濁液中逐漸加入1.00 mol/L HCl溶液,加入HCl溶液的體積與生成沉淀的關系如下圖所示。
試回答:
(1)A點的沉淀的化學式為________,理由是_______________________________________;
(2)寫出A點至B點發生反應的離子方程式: _____________________________________;
(3)原混合物中AlCl3的質量是________g,NaOH的物質的量是________ mol。
【答案】 Mg(OH)2 NaOH、MgCl2、AlCl3反應后有NaOH剩余,過量的NaOH與AlCl3反應生成NaAlO2 AlO![]() +H++H2O===Al(OH)3↓ 2.67 0.13
+H++H2O===Al(OH)3↓ 2.67 0.13
【解析】試題分析:由題意知,向所得濁液中逐漸加入1.00 mol/L HCl溶液,加入HCl溶液的體積在0~10.0mL之間時,發生了OH-+H+=H2O,說明濁液中不溶物只有氫氧化鎂,其物質的量為![]() ,所以n(MgCl2)=0.02mol;在10.0~30.0mL之間時,沉淀的質量逐漸增加,說明發生了AlO2-+H++H2O=Al(OH)3↓,n[Al(OH)3]=n(H+)=20.0
,所以n(MgCl2)=0.02mol;在10.0~30.0mL之間時,沉淀的質量逐漸增加,說明發生了AlO2-+H++H2O=Al(OH)3↓,n[Al(OH)3]=n(H+)=20.0![]() L
L![]() 1.00 mol/L=0.02mol;在30.0mL之后,氫氧化鋁和氫氧化鎂逐漸溶解于鹽酸。
1.00 mol/L=0.02mol;在30.0mL之后,氫氧化鋁和氫氧化鎂逐漸溶解于鹽酸。
(1)A點的沉淀的化學式為Mg(OH)2,理由是NaOH、MgCl2、AlCl3反應后有NaOH剩余,過量的NaOH與AlCl3反應生成NaAlO2;
(2)A點至B點發生反應的離子方程式為 AlO![]() +H++H2O===Al(OH)3↓ ;
+H++H2O===Al(OH)3↓ ;
(3)原混合物中n(AlCl3)= n[Al(OH)3] =0.02mol,質量是m(AlCl3)= 0.02mol![]() 133.5g/mol=2.67g;在圖像中B點,沉淀達到最大量,此時溶液中的溶質為氯化鈉,n(NaCl)=c(HCl)+2n(MgCl2)+3n(AlCl3)=30.0
133.5g/mol=2.67g;在圖像中B點,沉淀達到最大量,此時溶液中的溶質為氯化鈉,n(NaCl)=c(HCl)+2n(MgCl2)+3n(AlCl3)=30.0![]() L
L![]() 1mol/L+2
1mol/L+2![]() 0.02mol+3
0.02mol+3![]() 0.02mol=0.13mol,即NaOH的物質的量是0.13 mol。
0.02mol=0.13mol,即NaOH的物質的量是0.13 mol。


科目:高中化學 來源: 題型:
【題目】由二氧化硅制高純硅的流程如圖,下列判斷中錯誤的是( ) 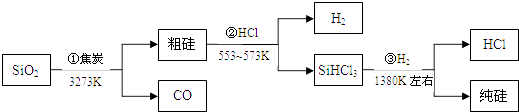
A.①②③均屬于氧化還原反應
B.H2和HCl均可循環利用
C.SiO2是一種堅硬難熔的固體
D.SiHCl3摩爾質量為135.5g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生活密切相關,下列過程沒有發生氧化還原反應的是
A.酸性重鉻酸鉀檢測酒精含量
B.內服小蘇打藥片治療胃酸過多
C.植物油開封久置變質
D.即熱飯盒自熱包中的鎂粉、鐵粉遇食鹽水迅速放熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于實驗室用二氧化錳制取氯氣的敘述不正確的是
A. 二氧化錳與濃鹽酸共熱B. 緩慢加熱反應
C. 用向下排空氣法收集氯氣D. 多余氯氣常用較濃的堿液吸收
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列溶液的PH值不隨溫度的變化而改變的是( )
A.0.01mol/L的氨水
B.0.01mol/L的NaOH
C.0.01mol/L的CH3COOH
D.0.01mol/L的HCl
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法中錯誤的是( )
A. 從1L 1mol·L-1的NaCl溶液中取出10mL,其濃度仍是1mol·L-1
B. 制成0.5L 10mol·L-1的鹽酸,需要氯化氫氣體112L(標準狀況)
C. 0.5L 2mol·L-1 BaCl2溶液中,Ba2+和Cl-總數為3×6.02×1023
D. 10g 98%硫酸(密度為1.84g·cm-3)與10mL 18.4mol·L-1硫酸的濃度是不同的
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com