
| A. | Cu2+ Cl- K+ SO42- | B. | Na+ NO3 - OH - CO3 2- | ||
| C. | Ba2+ Cl- NO3 - SO4 2- | D. | K+ Na+ Cl- SO4 2- |
分析 溶液中加入金屬鋅有H2放出,為非氧化性酸或強堿溶液,根據離子之間不能結合生成沉淀、氣體、水等,不能發生氧化還原反應等,則離子大量共存,并結合離子的顏色來解答.
解答 解:溶液中加入金屬鋅有H2放出,為非氧化性酸或強堿溶液,
A.Cu2+為藍色,與無色不符,且堿溶液中不能大量存在Cu2+,故A不選;
B.酸溶液中不能大量存在OH -、CO3 2-,故B不選;
C.Ba2+、SO4 2-結合生成沉淀,不能共存,故C不選;
D.酸、堿溶液中該組離子之間不反應,可大量共存,且離子均為無色,故D選;
故選D.
點評 本題考查離子的共存,為高頻考點,把握習題中的信息及常見離子的反應為解答的關鍵,側重分析與應用能力的考查,注意復分解反應的判斷,題目難度不大.


科目:高中化學 來源: 題型:解答題
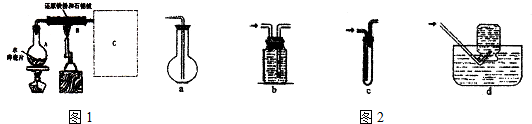
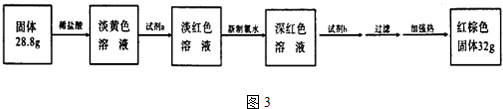
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
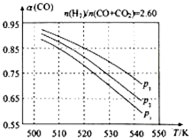 甲醇是重要的化工原料,又可做為燃料.利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:
甲醇是重要的化工原料,又可做為燃料.利用合成氣(主要成分為CO、CO2和H2)在催化劑的作用下合成甲醇,發生的主反應如下:| 物質 | CO | CO2 | H2 | CH3OH(g) |
| 標準生成熱(kJ/mol) | -110.52 | -393.51 | 0 | -201.25 |
| 容器編號 | 溫度(℃) | 起始物質的量(mol) | 平衡物質的量(mol) | |||
| CH3OH(g) | CH3OCH3(g) | H2O(g) | CH3OCH3(g) | H2O(g) | ||
| a | 387 | 0.20 | 0 | 0 | 0.080 | 0.080 |
| b | 387 | 0.40 | 0 | 0 | ||
| c | 207 | 0.20 | 0 | 0 | 0.090 | 0.090 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | v(CO)=1.2 mol/(L•s) | B. | v(NO2)=0.3 mol/(L•min) | ||
| C. | v(N2)=0.6 mol/(L•min) | D. | v(CO2)=1.2 mol/(L•min) |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
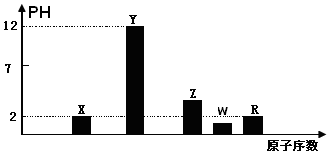


查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱的反應發生時不必加熱 | |
| B. | 反應是放熱還是吸熱必須看反應物和生成物所具有的總能量的相對大小 | |
| C. | 需要加熱才能發生的反應一定是吸熱反應 | |
| D. | 放熱反應在常溫下一定很容易發生 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com