
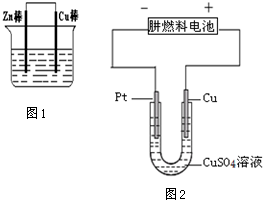
分析 (1)①銅鋅原電池中,活潑金屬作負極,在正極上有氣體生成;
②若電解質為硫酸銅溶液,則在正極上析出銅;
③根據原電池兩極上得失電子數目相等計算;
(2)電解硫酸銅溶液,陰極上銅離子放電,陽極上銅失電子發生氧化反應;根據串聯電路中轉移電子相等計算.
解答 解:(1)①將Zn棒和Cu棒用導線連接后,若電解質溶液為稀硫酸,則鋅為負極,銅為正極,負極反應為:Zn-2e-=Zn2+,正極反應為:2H++2e-=H2↑,在正極上有氣體生成,
故答案為:負;有氣體析出;2H++2e-=H2↑;
②將Zn棒和Cu棒用導線連接后,若電解質為硫酸銅溶液,則在正極上析出銅,鋅為負極,負極反應為Zn-2e-=Zn2+,正極反應為:Cu2++2e-=Cu,
故答案為:還原;Zn-2e-=Zn2+;
③設上述兩個過程中都消耗1molZn,則:Cu棒上(1)所析出物質的質量為:1mol×2g/mol=2g,(2)所析出物質的質量為:1mol×64g/mol=64g,Cu棒上(1)和(2)所析出物質的質量之比為2g:64g=1:32,故答案為:1:32;
(2)①電解硫酸銅溶液,陰極鉑上銅離子放電生成銅單質,電極反應式為Cu2++2e-═Cu,
故答案為:Cu2++2e-═Cu;
②陽極上銅失電子發生氧化反應,消耗128g銅轉移電子的物質的量=$\frac{128g}{64g/mol}$×2=4mol,
根據串聯電路中轉移電子相等得消耗標準狀況下的氧氣體積=$\frac{4mol}{4}$×22.4L/mol=22.4L,
氧氣的體積占空氣的20%,
所以空氣體積=22.4÷20%=112L,
故答案為:112.
點評 本題以聯氨為背景考查了原電池及電解池,據電解原理的電極反應特點寫出鉑極上的電極反應式,并結合質量變化進行相關計算,根據已知化學電源的書寫方法,難度不大.


 優百分課時互動系列答案
優百分課時互動系列答案科目:高中化學 來源: 題型:選擇題
| A. | 在常溫下可用鋁制容器貯藏運輸濃硫酸 | |
| B. | Al(OH)3可作治療胃酸過多的一種藥劑 | |
| C. | Na2O2可用作呼吸面具中的供氧劑 | |
| D. | 四氧化三鐵俗稱鐵紅,可用于作油漆、紅色涂料 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | BrCl+H2O═HCl+HBrO | D. | 2Na2O2+2H2O═4NaOH+O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量與滴入NaOH溶液的體積關系如圖所示,則原混合液中Al2(SO4)3與MgSO4的物質的量濃度之比為( )
在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量與滴入NaOH溶液的體積關系如圖所示,則原混合液中Al2(SO4)3與MgSO4的物質的量濃度之比為( )| A. | 6:1 | B. | 1:2 | C. | 2:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | M的氫化物的水溶液呈酸性 | B. | M2在常溫常壓下一定是氣體 | ||
| C. | MO3-中的M元素只能被還原 | D. | M位于元素周期表的第VA族 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com