
(14分)己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序數依次增大。X與N同主族,且與W都能形成A2B、A2B2型化合物;Z、W的單質常溫下均為無色氣體;Y原子的L層電子數是K層電子數的2倍;U原子的最外層電子數是其電子層數的2倍,試回答下列問題:
(1)YW2的電子式 ;V原子的結構示意圖 ;
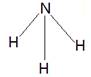
Z的氫化物結構式為 ;寫出U元素在周期表中的位置
N2W2中含有的化學鍵的種類
(2)X、Y、Z、W四種元素(按順序)可組成原子個數比為5:1:1:3的化合物,該化合物的稀溶液與足量澄清石灰水反應的離子方程式為 。
(3)從化合價升降的角度推測UW2與V元素的單質在水溶液中反應的化學方程式是 。
(1)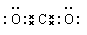 ;
;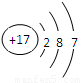 ,
,
第3周期第VIA族, 離子鍵和共價鍵 (各2分)
(2)NH4++HCO3-+Ca2++2OH-=NH3·H2O+CaCO3↓+H2O (2分)
(3)SO2+Cl2+2H2O=2HCl+H2SO4 (2分)
【解析】考查原子核外電子的排布規律及元素周期表的結構。Y原子的L層電子數是K層電子數的2倍,所以Y是碳元素。U原子的最外層電子數是其電子層數的2倍,且U的原子序數大于Y的,所以U是硫元素。常見A2B、A2B2型化合物是氧化鈉、過氧化鈉和水、雙氧水。所以X是氫元素,W是氧元素,N是鈉元素。Z的原子序數介于碳和氧之間,所以Z是氮元素。
(1)CO2是由極性鍵形成的共價化合物,電子式為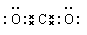 。氨氣分子中含有3個極性鍵,結構式為
。氨氣分子中含有3個極性鍵,結構式為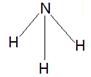 。
。
(2)X、Y、Z、W四種元素(按順序)可組成原子個數比為5:1:1:3的化合物是NH4HCO3,
和澄清的石灰水反應生成碳酸鈣和氨水,方程式NH4++HCO3-+Ca2++2OH-=NH3·H2O+CaCO3↓+H2O
(3)SO2中的硫元素是+4價,具有還原性。氯氣具有氧化性,所以能把SO2氧化生成硫酸,方
程式為SO2+Cl2+2H2O=2HCl+H2SO4。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:2011-2012學年浙江省浙東北三校高一下學期期中聯考化學試卷(帶解析) 題型:填空題
(14分)己知X、Y、Z、W、N、U、V是短周期的主族元素,原子序數依次增大。X與N同主族,且與W都能形成A2B、A2B2型化合物;Z、W的單質常溫下均為無色氣體;Y原子的L層電子數是K層電子數的2倍;U原子的最外層電子數是其電子層數的2倍,試回答下列問題:
(1)YW2的電子式 ;V原子的結構示意圖 ;
Z的氫化物結構式為 ;寫出U元素在周期表中的位置
N2W2中含有的化學鍵的種類
(2)X、Y、Z、W四種元素(按順序)可組成原子個數比為5:1:1:3的化合物,該化合物的稀溶液與足量澄清石灰水反應的離子方程式為 。
(3)從化合價升降的角度推測UW2與V元素的單質在水溶液中反應的化學方程式是 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com