
| A. | 原子半徑C>D>E | |
| B. | A2E6分子中各原子均滿足8電子結構 | |
| C. | 氣態(tài)氫化物的穩(wěn)定性HmE>HnD | |
| D. | B、C形成的化合物中只可能存在離子鍵 |
分析 A、B、C、D、E是元素周期表中前18號元素,原子序數(shù)依次增大,已知B、D同主族,形成共價化合物DB3,則B為O元素、D為S元素,C、D、E同周期,可組成離子化合物C2B,則C為Na,E的原子序數(shù)最大,則E為Cl,元素形成共價化合物AE4,A的原子序數(shù)小于氧,則A為碳元素,據(jù)此解答.
解答 解:A、B、C、D、E是元素周期表中前18號元素,原子序數(shù)依次增大,已知B、D同主族,形成共價化合物DB3,則B為O元素、D為S元素,C、D、E同周期,可組成離子化合物C2B,則C為Na,E的原子序數(shù)最大,則E為Cl,元素形成共價化合物AE4,A的原子序數(shù)小于氧,則A為碳元素.
A.同周期自左而右原子半徑減小,故原子半徑Na>S>Cl,故A正確;
B.C2Cl6分子中各原子均滿足8電子結構,故B正確;
C.非金屬性Cl>S,故氫化物穩(wěn)定性HCl>H2S,故C正確;
D.鈉與氧形成的過氧化鈉中既存在離子鍵又存在共價鍵,故D錯誤,
故選:D.
點評 本題考查結構性質(zhì)位置關系應用,推斷元素是解題關鍵,注意掌握常見元素化合物組成.


 培優(yōu)口算題卡系列答案
培優(yōu)口算題卡系列答案 開心口算題卡系列答案
開心口算題卡系列答案 口算題卡河北少年兒童出版社系列答案
口算題卡河北少年兒童出版社系列答案科目:高中化學 來源: 題型:解答題
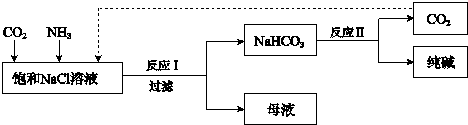
 2NH3.
2NH3.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2mol | B. | 0.6mol | C. | 0.8mol | D. | l.0mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
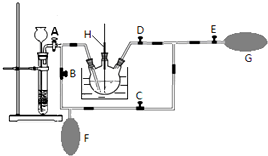
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
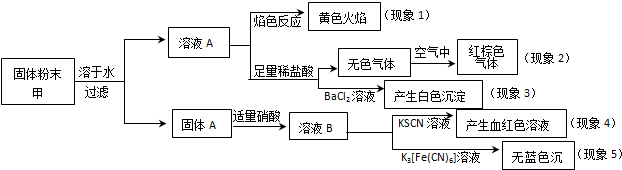
| A. | 根據(jù)現(xiàn)象1可推出該固體粉末中含有鈉元素,但一定不含鉀元素 | |
| B. | 根據(jù)現(xiàn)象2可推出該固體粉末中一定不含有NaNO2 | |
| C. | 根據(jù)現(xiàn)象3可推出該固體粉末中一定含有Na2SO4 | |
| D. | 根據(jù)現(xiàn)象4和現(xiàn)象5可推出該固體粉末中一定不含F(xiàn)eO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
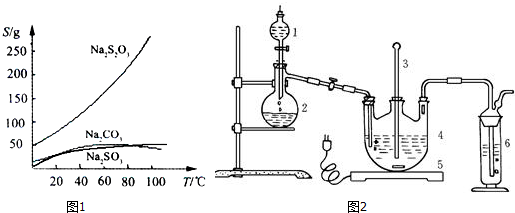

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 反應物的鍵能總和比生成物的鍵能總和高 | |
| B. | E1為反應物的平均能量與過渡態(tài)的能量差,稱為正反應的活化能 | |
| C. | 正反應的熱效應為△H=E1-E2,且E2>E1,所以正反應為放熱反應 | |
| D. | 使用合適的催化劑能同時降低E1和E2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
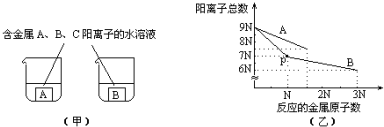
| A. | ① | B. | ② | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
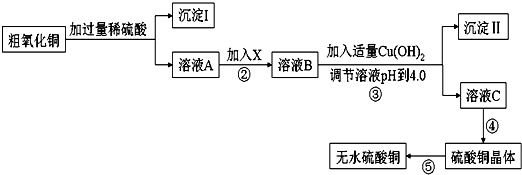
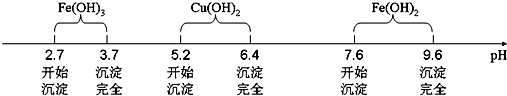
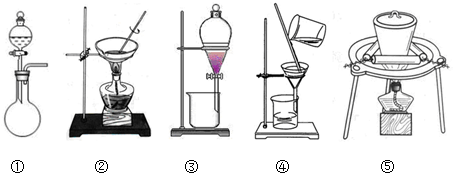
| 滴定次數(shù) | 第一次 | 第二次 | 第三次 |
| 滴定前讀數(shù)(mL) | 0.10 | 0.36 | 1.10 |
| 滴定滴定后讀數(shù)(mL) | 20.12 | 20.34 | 22.12 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com