
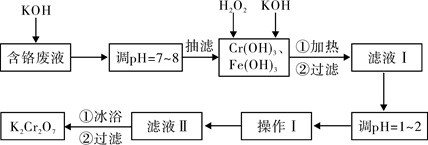
| 物質 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
| KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |


 云南師大附小一線名師提優作業系列答案
云南師大附小一線名師提優作業系列答案 沖刺100分單元優化練考卷系列答案
沖刺100分單元優化練考卷系列答案科目:高中化學 來源:不詳 題型:填空題
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題

| A.此法的優點之一是原料來源豐富 |
| B.該提取鎂的過程中涉及置換、分解、復分解和氧化還原反應 |
| C.步驟①②③的目的是從海水中提取無水MgCl2 |
| D.步驟②中加鹽酸的離子方程式為Mg(OH)2+2H+=Mg2++2H2O |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 3K2MnO4+KCl+3H2O
3K2MnO4+KCl+3H2O| | K2CO3 | KHCO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 33.7 | 11.1 | 6.34 |
 2KMnO4+2KOH+H2↑。與原方法相比,電解法的優勢為 。
2KMnO4+2KOH+H2↑。與原方法相比,電解法的優勢為 。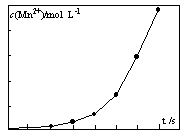
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| A.萃取分液法 | B.加熱法 | C.結晶法 | D.分液法 E.過濾法 F.蒸餾法 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

| 物質 | 熔點/℃ | 沸點/℃ | 密度/g·cm-3 | 在水中溶解性 |
| 甲苯 | -95 | 110.6 | 0.8669 | 難溶 |
| 苯甲酸鉀 | 121.5~123.5 |  |  | 易溶 |
| 苯甲酸 | 122.4 | 248 | 1.2659 | 微溶 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題


查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| 選項 | 物質(括號內為雜質) | 試劑 | 方法 |
| A | Cl2(HCl ) | NaOH溶液 | 洗氣 |
| B | Fe(Al) | NaOH溶液 | 過濾 |
| C | CO2(CO) | O2 | 點燃 |
| D | KNO3(KOH) | FeCl3溶液 | 過濾 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

| 物質名稱 | 溶度積(Ksp) | pH值 | |
| 開始沉淀 | 完全沉淀 | ||
| Mg(OH)2 | 5.6×10-12 | 9.3 | 10.8 |
| Fe(OH)3 | 2.8×10-16 | 2.7 | 3.7 |
| Al(OH)3 | 1.3×10-33 | 3.7 | 4.7 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com