
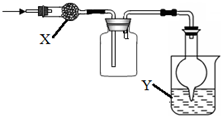
 如圖是用于干燥、收集并吸收多余氣體的裝置,下列方案正確的是( )
如圖是用于干燥、收集并吸收多余氣體的裝置,下列方案正確的是( ) | 選項 | X | 收集氣體 | Y |
| A | 堿石灰 | 氯氣 | 水 |
| B | 堿石灰 | 氨氣 | 水 |
| C | 氯化鈣 | 二氧化硫 | 氫氧化鈉 |
| D | 氯化鈣 | 一氧化氮 | 氫氧化鈉 |
| A. | A | B. | B | C. | C | D. | D |
分析 該裝置中采用向上排空氣法收集,說明該氣體密度大于空氣,且該氣體和空氣中成分不反應,用固體干燥劑干燥,則該氣體和干燥劑不反應,據此結合選項進行判斷.
解答 解:A.堿石灰呈堿性,能與氯氣反應,所以氯氣不能用堿石灰干燥,且氯氣吸收多余的氯氣應該用堿液,故A錯誤;
B.氨氣密度小于空氣,應該采用向下排空氣法收集,故B錯誤;
C.二氧化硫密度大于空氣且常溫下和空氣中成分不反應,氯化鈣和二氧化硫不反應,所以能用氯化鈣干燥,故C正確;
D.常溫下NO和氧氣反應生成紅棕色氣體二氧化氮,所以得不到NO,NO采用排水法收集,故D錯誤;
故選C.
點評 本題考查了氣體的干燥、收集和尾氣處理,題目難度不大,根據氣體的性質確定干燥劑、尾氣處理試劑,根據氣體的溶解性及密度確定收集方法,注意氨氣不能用氯化鈣干燥,為易錯點.


 鷹派教輔銜接教材河北教育出版社系列答案
鷹派教輔銜接教材河北教育出版社系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬氧化物一定是堿性氧化物,非金屬氧化物不一定是酸性氧化物 | |
| B. | 有單質參加或生成的化學反應一定是氧化還原反應 | |
| C. | 金屬陽離子被還原一定得到相應的金屬單質 | |
| D. | 在氧化還原反應中金屬單質只能作還原劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | SO2+2NaOH═Na2SO3+H2O | B. | SO2+H2O+(NH4)2SO3═2NH4HSO3 | ||
| C. | SO2+N02═SO3+NO | D. | SO2+H2O+Br2═H2SO4+2HBr |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1,3-丁二烯的實驗式:C4H6 | B. | 乙醇的分子式:C2H5OH | ||
| C. | 甲醛的結構式: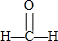 | D. | 聚丙烯的結構簡式: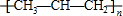 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加入鹽酸 | B. | 通入CO2 | ||
| C. | 加熱至固體質量不再減少為止 | D. | 加入NaOH溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com