
高氯酸、硫酸、硝酸和鹽酸都是強酸,其酸性在水溶液中差別不大。四種物質在冰醋酸中的電離
常數如表。從表格中判斷以下說法中不正確的是( )
HClO4 | H2SO4 | HCl | HNO3 | |
Ka | 1.6×10﹣5 | 6.3×10﹣9 | 1.6×10﹣9 | 4.2×10﹣10 |
A. 在冰醋酸中高氯酸是這四種酸中最強的酸
B. 在冰醋酸中這四種酸都沒有完全電離
C. 在冰醋酸中硫酸的電離方程式為H2SO4=2H++SO42﹣
D. 酸的強弱與其本身的結構和溶劑的性質有關
科目:高中化學 來源:2016-2017學年北京市懷柔區高一上學期期末考試化學試卷(解析版) 題型:選擇題
將0.4g NaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol•L﹣1稀鹽酸.下列圖象能正確表示加入鹽酸的體積和生成CO2的物質的量的關系的是
A.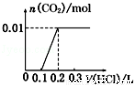 B.
B.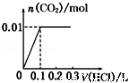 C.
C.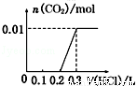 D.
D.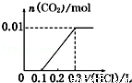
查看答案和解析>>
科目:高中化學 來源:北京市懷柔區2016-2017學年度第一學期期末考試高二化學試卷 題型:選擇題
近年來流行喝蘋果醋.蘋果醋是一種由蘋果發酵而成的具有解毒、降脂、減肥和止瀉等明顯藥效的健康食品.蘋果酸(α﹣羥基丁二酸)是這種飲料的主要酸性物質,蘋果酸的結構如圖所示,下列相關說法不正確的是
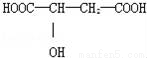
A. 蘋果酸在一定條件下能發生酯化反應
B. 蘋果酸在一定條件下能發生催化氧化反應
C. 蘋果酸在一定條件下能發生消去反應
D. 蘋果酸不能發生縮聚反應
查看答案和解析>>
科目:高中化學 來源:湖北省沙市2016-2017學年高二下學期第三次雙周考化學試卷(A卷) 題型:簡答題
X、Y、Z、W為短周期的主族元素,其原子序數依次增大。X元素形成的單質是自然界中含量最多的氣體,Y是電負性最大的元素,W的原子最外層電子數與核外電子總數之比為3︰8,X的原子序數是Z的原子序數的一半,U是第四周期11列元素。
(1)U基態原子的價電子排布式__________________,Z在周期表中位置為___________________。
(2)在OY2中,氧原子的雜化軌道類型是____________。
(3)Z、W的最高價氧化物的水化物,酸性較強的是______。(填最高價氧化物的水化物的化學式)
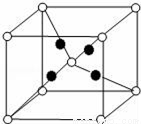
(4)U的含氧化合物M晶胞如圖所示(“○”表示氧原子),則M的化學式為________。
(5)已知:[Cu(NH3)4]2+具有對稱的空間構型,且當[Cu(NH3)4]2+中的兩個NH3被兩個Cl﹣取代時,能得到兩種不同結構的產物,則[Cu(NH3)4]2+的空間構型為_____________。
查看答案和解析>>
科目:高中化學 來源:湖北省沙市2016-2017學年高二下學期第三次雙周考化學試卷(A卷) 題型:選擇題
2 mol A與2 mol B混合于2 L的密閉容器中,發生如下反應:2A(g)+3B(g) 2C(g)+zD(g),2 s后A的轉化率為50%,測得υ(D)=0.25 mol·L﹣1·s﹣1,下列推斷不正確的是( )
2C(g)+zD(g),2 s后A的轉化率為50%,測得υ(D)=0.25 mol·L﹣1·s﹣1,下列推斷不正確的是( )
A. z=2 B. 2 s后,容器內的壓強是初始的7/8倍
C. 2 s后,B的濃度為0.5 mol/L D. 2 s時C的體積分數為2/7
查看答案和解析>>
科目:高中化學 來源:湖北省沙市2016-2017學年高二下學期第三次雙周考化學試卷(A卷) 題型:選擇題
X、Y、Z、W是原子序數依次增大的短周期元素,X的一種原子沒有中子,Y、Z易形成質量比為3︰4和3︰8的兩種常見化合物,W所在的周期數和族序數相同。下列說法正確的是( )
A. W的最高價氧化物對應水化物是強堿 B. 原子最外層電子數:W>Z>Y
C. 原子半徑:Y<Z<W D. X、Y可以形成既有極性鍵也有非極性鍵的化合物
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省、襄陽五中、襄陽四中等)高三下學期第二次聯考理綜化學試卷(解析版) 題型:簡答題
I、煤制天然氣的工藝流程簡圖如下:
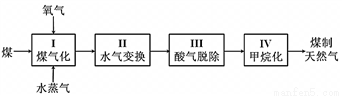
⑴反應I:C(s) + H2O(g) CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
CO(g) + H2(g) ΔH = +135 kJ·mol-1,通入的氧氣會與部分碳發生燃燒反應。請利用能量轉化及平衡移動原理說明通入氧氣的作用:___________________________。
⑵反應II:CO(g) + H2O(g)  CO2(g) + H2(g) ΔH = ?41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。
CO2(g) + H2(g) ΔH = ?41 kJ·mol-1。如圖表示不同溫度條件下,煤氣化反應I發生后的汽氣比(水蒸氣與CO物質的量之比)與CO平衡轉化率的變化關系。
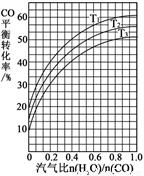
① 判斷T1、T2和T3的大小關系:______________。(從小到大的順序)
② 若煤氣化反應I發生后的汽氣比為0.8,經煤氣化反應I和水氣變換反應II后,得到CO與H2的物質的量之比為1:3,則反應II應選擇的溫度是_______(填“T1”或“T2”或“T3”)。
⑶① 甲烷化反應IV發生之前需要進行脫酸反應III。煤經反應I和II后的氣體中含有兩種酸性氣體,分別是H2S和_______。
② 工業上常用熱碳酸鉀溶液脫除H2S氣體得到兩種酸式鹽,該反應的離子方程式是_______。
II、利用甲烷超干重整CO2技術可得到富含CO的氣體,將甲烷和二氧化碳轉化為可利用的化學品,其能源和環境上的雙重意義重大。該技術中的化學反應為:
CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0
H>0
CH4超干重整CO2的催化轉化原理示意如圖:
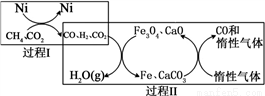
⑷過程II,實現了含氫物種與含碳物種的分離。生成H2O(g)的化學方程式是______________。
⑸假設過程I和過程II中的各步均轉化完全,下列說法正確的是_______。((填序號)
a.過程I和過程II中均含有氧化還原反應
b.過程II中使用的催化劑為Fe3O4 和CaCO3
c.若過程I投料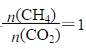 ,可導致過程II中催化劑失效
,可導致過程II中催化劑失效
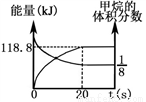
(6)一定條件下,向體積為2L的恒容密閉容器中充入1.2 mol CH4(g)和4.8 mol CO2(g),發生反應CH4 (g)+3CO2 (g) 2H2O(g)+4CO(g)
2H2O(g)+4CO(g)  H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的
H>0,實驗測得,反應吸收的能量和甲烷的體積分數隨時間變化的曲線圖像如圖。計算該條件下,此反應的 H=________________。
H=________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省達州市年高二上學期期末檢測化學試卷(解析版) 題型:選擇題
向恒溫恒容的密閉容器中充入amolX和bmolY,發生反應X(g)+3Y(g) 2Z(g)達到平衡時,測得X和Y的轉化率分別為25%和37.5%。則a:b為
2Z(g)達到平衡時,測得X和Y的轉化率分別為25%和37.5%。則a:b為
A. 1 3 B. 3
3 B. 3 1 C. 3
1 C. 3 2 D. 1
2 D. 1 2
2
查看答案和解析>>
科目:高中化學 來源:2017屆浙江省教育綠色評價聯盟高三3月適應性考試(選考)化學試卷(解析版) 題型:選擇題
下列說法正確的是( )
A. 鎂帶燃燒可以用CO2滅火
B. 單晶硅是重要的半導體材料,常用于制造光導纖維
C. Cl2能使濕潤的有色布條褪色,是因為Cl2的氧化性
D. 金屬鈉可保存在煤油中
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com