
【題目】下列物質中,不屬于合金的是( )
A. 硬鋁 B. 黃銅 C. 水銀 D. 鋼鐵
科目:高中化學 來源: 題型:
【題目】(1)反應Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常數為K1
FeO(s)+CO(g) ΔH1,平衡常數為K1
反應Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常數為K2
FeO(s)+H2(g) ΔH2,平衡常數為K2
在不同溫度時K1、K2的值如下表:
700℃ | 900℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反應CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH,平衡常數為K,則ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述計算可知,反應CO2(g)+H2(g)
CO(g)+H2O(g) ΔH,平衡常數為K,則ΔH=_______(用ΔH1和ΔH2表示),K=________(用K1和K2表示),且由上述計算可知,反應CO2(g)+H2(g) ![]() CO(g)+H2O(g)是_________反應(填“吸熱”或“放熱”)。
CO(g)+H2O(g)是_________反應(填“吸熱”或“放熱”)。
(2)一定溫度下,向某密閉容器中加入足量鐵粉并充入一定量的CO2氣體,發生反應Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的濃度與時間的關系如圖1所示:
FeO(s)+CO(g) ΔH>0,CO2的濃度與時間的關系如圖1所示:

①該條件下反應的平衡常數為___________;若鐵粉足量,CO2的起始濃度為2.0 mol/L,則平衡時CO2的濃度為________mol/L。
②下列措施中能使平衡時CO物質的量百分數增大的是________(填序號)。
A.升高溫度 B.增大壓強
C.再充入一定量的CO2 D.再加入一定量鐵粉
(3)對于可逆反應Fe(s)+CO2(g)![]() FeO(s)+CO(g),該反應的逆反應速率隨時間變化的關系如圖2。
FeO(s)+CO(g),該反應的逆反應速率隨時間變化的關系如圖2。
①從圖中看到,反應在t2時達平衡,在t1時改變了某種條件,改變的條件可能是______。
A.升溫 B.增大CO2濃度 C.使用催化劑
②如果在t3時從混合物中分離出部分CO,t4~t5時間段反應處于新平衡狀態,請在圖上畫出t3~t5的v逆變化曲線_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】四種短周期元素在周期表中的位置如圖,其中只有M為金屬元素.下列說法不正確的是( ) 
A.原子半徑Z<M
B.Y的最高價氧化物對應水化物的酸性比X的弱
C.X的最簡單氣態氫化物的熱穩定性比Z的小
D.Z位于元素周期表中第2周期第ⅥA族
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮化硅(Si3N4)是一種新型陶瓷材料,它可由石英與焦炭在高溫的氮氣流中反應制得:①3SiO2+6C+2N2![]() Si3N4+6CO;也可由SiCl4的蒸汽和NH3反應制取:②3SiCl4+4NH3
Si3N4+6CO;也可由SiCl4的蒸汽和NH3反應制取:②3SiCl4+4NH3![]() Si3N4+12HCl。則下列敘述正確的是
Si3N4+12HCl。則下列敘述正確的是
A. 反應②屬于離子反應
B. 若制取等量的Si3N4,則反應①②轉移電子數目必然相等
C. 反應①的氧化劑是N2
D. 反應①中氧化產物與還原產物物質的量之比為1∶6
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有關合理用藥的下列說法中,錯誤的是( )
A. 對癥下藥是合理用藥的首要原則
B. 能被充分、快速吸收而無刺激性的藥物,可在飯前口服
C. 一種藥物的用量,是經過嚴格的科學實驗和大量的臨床研究確定的
D. 因為青霉素能夠殺菌,所以過期的青霉素仍然能夠使用
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于反應2NO2(g)![]() N2O4(g)達到平衡后,在溫度不變時欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
N2O4(g)達到平衡后,在溫度不變時欲使c(NO2)/c(N2O4)比值增大,可以采取的措施是
A. 體積不變,增加NO2的量 B. 體積不變,增加N2O4的量
C. 體積不變,充入N2 D. 體積擴大到原來的2倍
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在2L密閉容器內,800℃時反應2NO(g)+O2(g)=2NO2(g)體系中,n(NO)隨時間的變化如下表:
時間(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
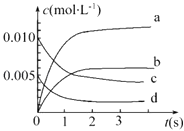
(1)上述反應在第5s時,NO的轉化率為 .
(2)如圖中表示NO2變化曲線的是 . 用O2表示0~2s內該反應的平均速率v= .
(3)能說明該反應已達到平衡狀態的是 .
a.v(NO2)=2v (O2) b.容器內壓強保持不變
c.v逆(NO)=2v正(O2) d.容器內密度保持不變.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)氮是地球上含量豐富的一種元素,氮及其化合物在工農業生產、生活中有著重要作用,下圖是N2(g)和H2(g)反應生成lmol NH3(g)過程中能量變化示意圖,

請寫出N2和H2反應的熱化學方程式:______________________________________________;
(2)若已知下列數據:
化學鍵 | H-H | N≡N |
鍵能/kJ mol-1 | 435 | 943 |
試根據表中及圖中數據計算N-H的鍵能____________kJ mol-1
(3)合成氨反應通常用鐵觸媒作催化劑。使用鐵觸媒后的變化是:E1_______,△H________ (填“增大”、“減小、” “不變”)。
(4)用NH3催化還原NO2還可以消除氮氧化物的污染。例如
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H1=akJ·mol-1
N2(g)+O2(g)=2NO(g) △H2=bkJ·mol-1
若1mol NH3還原NO至N2,則該反應過程中的反應熱△H3=_________kJ/mol (用含a、b的式子表示)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com