
【題目】在-50℃時,液氨的電離跟水的電離相似,存在平衡:2NH3(l)![]() NH4++NH2-,NH4+的平衡濃度為1×10-15mol·L-1,下列說法錯誤的是
NH4++NH2-,NH4+的平衡濃度為1×10-15mol·L-1,下列說法錯誤的是
A. 在液氨中加入NaNH2,可使液氨的離子積變大
B. 此溫度下液氨的離子積K為1×10-30
C. 在液氨中加入NH4Cl,液氨的離子積不變
D. 改變溫度,液氨中c(NH4+)=c(NH2-)
【答案】A
【解析】仔細觀察液氨的電離方程式,不難發現液氨的電離類似于水的電離,均屬于“質子(H+)轉移自偶電離”, 其中NH4+和NH2-分別相當于純水中水電離出的H3O+和OH-。由此類比推出,液氨的性質應類似于水,如液氨可以與金屬鈉反應生成H2和NaNH2;影響液氨電離平衡的因素也類似于水。液氨的離子積(也應該只是溫度的函數)為常數,此溫度下會恒等于1×10-30。故A、液氨的離子積為常數,只與溫度有關,溫度不變,常數不變,選項A錯誤;B、此溫度下液氨的離子積K為1×10-15mol·L-1×1×10-15mol·L-1=1×10-30 mol2·L-2,選項B正確;C、液氨的離子積為常數,只與溫度有關,與濃度無關,溫度不變,常數不變,選項C正確;D、改變溫度,液氨中c(NH4+)、c(NH2-)同時改變,但c(NH4+)=c(NH2-),選項D正確。答案選A。


科目:高中化學 來源: 題型:
【題目】想一想:Ba(OH)2(固體)、CuSO4(固體)、CH3COOH(液態)這些物質為什么歸為一類,下列哪些物質還可以和它們歸為一類
A、75%的酒精溶液 B、硝酸鈉
C、Fe(OH)3膠體 D、豆漿
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】根據所學知識填空:
(1)實驗室中可用KClO3和濃HCl反應制取氯氣,寫出該反應的化學方程式,并用雙線橋法標出電子轉移的方向和數目;該反應中,氧化產物是 , 還原產物是 , 氧化產物與還原產物的物質的量之比是 .
(2)化學鍍鎳的溶液中含有Ni2+和H2PO2﹣在酸性條件下發生如下反應,請配平該反應.
Ni2++H2PO2﹣+→ Ni++H2PO3﹣+
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】【化學——選修3:物質結構與性質】
Q、R、X、Y、Z為周期表前四周期元素,原子序數依次遞增。已知:
①Q為元素周期表中原子半徑最小的元素;
②R的基態原子中電子占據三種能量不同的原子軌道,且每種軌道中的電子總數相同;
③Y的基態原子的核外成對電子數是未成對電子數的3倍;
④Q、R、Y三種元素組成的一種化合物M是新裝修居室中常含有的一種有害氣體,Q、R兩種元素組成的原子個數比為1:1的化合物N是中學化學中常見的有機溶劑;
⑤Z有“生物金屬”之稱,Z4+離子和氬原子的核外電子排布相同。
請回答下列問題(答題時,Q、R、X、Y、Z用所對應的元素符號表示)
(1)化合物M的空間構型為______________ ,其中心原子采取_________雜化;化合物N在固態時的晶體類型為_______________。
(2)R、X、Y三種元素的第一電離能由小到大的順序為___________。
(3)由上述一種或多種元素組成的與RY2互為等電子體的分子為__________(寫分子式)。
(4)由R、X、Y三種元素組成的RXY-離子在酸性條件下可與NaClO溶液反應,生成X2、RY2等物質。該反應的離子方程式為______________________________。
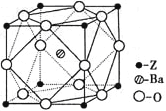
(5)Z原子基態時的外圍電子排布式為_________________;Z的一種含氧酸鋇鹽的晶胞結構如圖所示,晶體內與每個Z原子等距離且最近的氧原子數為____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】t℃時,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12。
(1)該溫度下,水的離子積常數Kw=________________。
(2)在該溫度下,將100mL0.1mol/L的稀硫酸與100mL0.4mol/L的NaOH溶液混合后,溶液的pH=_________,此時該溶液中由水電離的c(OH-)=____________。
(3)該溫度下,若100體積pH1=a的某強酸溶液與1體積pH2=b的某強堿溶液混合后溶液呈中性,則混合前,該強酸的pH1與強堿的pH2之間應滿足的關系是______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】
釩及其化合物在科學研究中和工業生產中具有許多用途。
(1)基態釩原子的核外價電子排布式為________。
(2)釩有+2、+3、+4、+5等幾種化合價。這幾種價態中,最穩定的是______。
(3)V2O5溶解在NaOH溶液中,可得到釩酸鈉(Na3VO4)。例舉與VO43-空間構型相同的一種陽離子__________(填化學式)。
(4)釩(Ⅱ)的配離子有[V(CN)6]4-、[V(H2O)6]2+等。
①CN-與N2互為等電子體,CN-中σ鍵和Π鍵數目比為________。
②對H2O與V2+形成[V(H2O)6]2+過程的描述不合理的是______________。
a.氧原子的雜化類型發生了變化
b.微粒的化學性質發生了改變
c.微粒中氫氧鍵(H-O)的夾角發生了改變。
d.H2O與V2+之間通過范德華力相結合。
③在[V(H2O)6]2+中存在的化學鍵有___________。
a.金屬鍵 b.配位鍵 c. σ鍵 d.Π鍵 f. 氫鍵
(5)已知單質釩的晶胞如圖,則V原子的配位數是_______,假設晶胞的邊長為d nm,密度ρ g·cm-3,則釩的相對原子質量為_______________。(設阿伏伽德羅常數為NA)

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】80 ℃時,2 L 密閉容器中充入0.40 mol N2O4,發生反應N2O4![]() 2NO2 △H =+Q kJ/mol(Q>0),獲得如下數據:下列判斷正確的是
2NO2 △H =+Q kJ/mol(Q>0),獲得如下數據:下列判斷正確的是
時間/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol·L-1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
A. 升高溫度該反應的平衡常數K減小
B. 20~40 s 內,v(N2O4)=0.002 mol/( Ls)
C. 反應達平衡時,吸收的熱量為0.30 Q kJ/mol
D. 100s 時再通入0.40 mol N2O4,達新平衡時N2O4的轉化率增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列反應中,生成的有機物只有一種的是
A. 異戊二烯(![]() )與等物質的量的Br2發生加成反應
)與等物質的量的Br2發生加成反應
B. 2-氯丁烷(![]() )與NaOH乙醇溶液共熱發生消去HCl分子的反應
)與NaOH乙醇溶液共熱發生消去HCl分子的反應
C. 甲苯在一定條件下發生硝化反應生成一硝基甲苯的反應
D. 新戊烷和氯氣發生取代反應生成一氯取代物的反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向 50mL 稀 H2SO4 與稀 HNO3 的混合溶液中逐漸加入鐵粉,假設加入鐵粉的質量與產生氣體的體積(標 準狀況下)之間的關系如圖所示,且每一段只對應一個反應。下列說法正確的是( )

A. 參加反應鐵粉的總質量 m2=5.6 g
B. 所用混合溶液中 c(HNO3)=0.5 molL-1
C. 開始時產生的氣體為 H2
D. AB 段產生的反應為置換反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com