
下圖表示在催化劑作用下將X和Y合成具有生物活性的物質Z,W是中間產物(R1、R2均為烴基)。則下列有關敘述一定正確的是
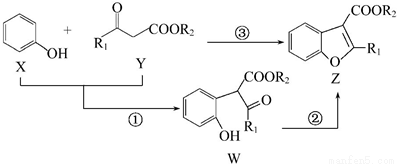
A.反應①屬于加成反應
B.1molZ完全加成需要3molH2
C.X與W屬于同系物
D.X、Y、Z、W都能與NaOH溶液反應
 通城學典默寫能手系列答案
通城學典默寫能手系列答案科目:高中化學 來源:2016-2017學年山西省高二上開學考化學試卷(解析版) 題型:選擇題
W、X、Y、Z均為短周期元素,W的最外層電子數與核外電子數之比為7:17;X與W同主族;Y的原子序數是W和X的原子序數之和的一半:含Z元素物質的焰色反應為黃色。下列判斷正確的是
A. 金屬性:Y>Z B. 氫化物的沸點:X>W
C. 離子的還原性:X>W D. 原子及離子半徑:Z>Y>X
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上學期周考(8.28)化學試卷(解析版) 題型:填空題
磷有三種同素異形體,分別為白磷(P4)、紅磷和黑磷。
(1)白磷常溫為白色或淡黃色固體,在40℃左右自燃,實驗室保存少量白磷的方法是__________;
(2)白磷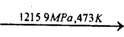 黑磷,黑磷比白磷穩定。結構與石墨相似,下列敘述正確的是_______
黑磷,黑磷比白磷穩定。結構與石墨相似,下列敘述正確的是_______
A.黑磷與白磷互為同分異構體 B.黑磷能導電
C.白磷轉化為黑磷為氧化還原反應 D.白磷轉化為黑磷為放熱反應
(3)紅磷在氯氣中燃燒生成兩種氯化物,其中一種氯化物分子是每個原子最外層都滿足8個電子的結構,則該氯化物的空間構型與下列_______分子最相似(填字母)
A.H2O B.CCl4 C.NH3 D.CS2
(4)己知白磷、紅磷燃燒的熱化學方程式分別為
① P4(s,白磷)+5O2(g)=P4O10(s) △H=-2986kJ/mol
② P(s,紅磷)+ O2(g)=
O2(g)=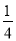 P4O10(s) △H=-739kJ/mol
P4O10(s) △H=-739kJ/mol
寫出紅磷轉化為白磷的熱化學方程式:________________________。
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上學期周考(8.28)化學試卷(解析版) 題型:選擇題
t℃,將一定質量的某物質的不飽和溶液均分為三份,分別加熱蒸發溶液,然后把溫度降至t℃,已知從三份溶液中蒸發的溶劑質量分別為10g、20g、30g,析出晶體(不含結晶水)質量分別為a、b、c(單位g,且a、b、c均大于零),則a、b、c三者的關系為()
A.c=2b-a B.c=a+b C.c=a+2b D.c=2a+b
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市高三上學期開學考試化學試卷(解析版) 題型:填空題
W、X、Y、Z(W、X、Y、Z分別代表元素符號)均為元素周期表中前四周期的元素,其原子序數依次增大,其中W、X、Y、Z為短周期元素,它們的單質在通常情況下均為無色氣體。X元素的基態原子在同周期元素基態原子中含有的未成對電子數最多,Y元素的基態原子中s能級上的電子數等于p能級上的電子數,Z為金屬元素,其基態原子是具有4s1結構的基態原子中質子數最多的原子,試回答下列問題:
(1)寫出X的基態原子的價電子排布式_________________;
(2)比較X、Y兩元素基態原子的第一電離能大小:X__________Y(填“>”、“<”或“=”),理由是________;
(3)W、X兩元素能寫出一種常見氣體M,每個M分子中含有10個電子,M分子中心原子的雜化方式為_________;WX兩種元素還能寫出一種常見陽離子N,每個N中也含有10個電子,但在N與M中所含化學鍵的鍵角大小不同,其原因是__________;
(4)Z2+可與M分子在誰溶液中形成[Z(M)4]2+,其中M分子和Z2+通過__________-結合;
(5)單質Z的警報結構如圖所示,已知兩個最近的Z原子距離為a,Z的相對原子質量用Mr表示,則該晶體密度為_______________(只列計算式)。
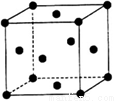
查看答案和解析>>
科目:高中化學 來源:2017屆重慶市高三上學期開學考試化學試卷(解析版) 題型:選擇題
短周期元素W、X、Y、Z在元素周期表中的位置如圖所示,下列說法中正確的是
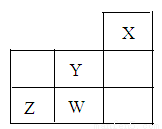
A. W的最高價氧化物對應的水化物是強酸
B. Y的一種半徑在同周期主族元素中最大
C. W的非金屬性比Z的弱
D. Z的氣態氫化物的穩定性在同主族元素中最強
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河南省高二上入學考試化學試卷(解析版) 題型:選擇題
實驗室里可按下圖所示的裝置干燥、儲存氣體 R,多余的氣體可用水吸收,則 R是( )
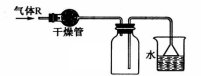
A.NO2 B.HCl C.CH4 D.NH3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年貴州省高一上入學考試化學卷(解析版) 題型:選擇題
用氯酸鉀和二氧化錳混合物加熱制取氧氣,將制得的氣體通入蒸餾水中,再向水中滴入含稀硝酸和硝酸銀的溶液,有白色沉淀產生,根據以上事實,某同學得出如下結論:①制得的氧氣不是純凈物 ②制得的氧氣中混有含氯的物質 ③制得的氣體中含氯元素 ④在發生氯酸鉀分解反應的同時,還發生了其它反應。以上結論中正確的是
A.只有①③ B.只有①② C.①②③ D.全部
查看答案和解析>>
科目:高中化學 來源:2017屆河南省高三第一次月考理綜化學試卷(解析版) 題型:填空題
【化學——選修3:物質結構與性質】
鹵族元素的單質和化合物很多,我們可以利用所學物質結構與性質的相關知識去認識和理解它們。
(1)鹵族元素位于元素周期表的_________區;溴的價電子排布式為________________。
(2)在一定濃度的溶液中,氫氟酸是以二分子締合(HF)2形式存在的。使氫氟酸分子締合的作用力是________。
(3)請根據下表提供的第一電離能數據判斷,最有可能生成較穩定的單核陽離子的鹵素原子是_________(寫出名稱)。
氟 | 氯 | 溴 | 碘 | |
第一電離能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的結構分別如圖I、II所示:
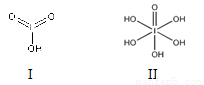
請比較二者酸性強弱:HIO3________H5IO6(填“>”、 “<”或“=”)。
(5)已知ClO2-為角型,中心氯原子周圍有四對價層電子。ClO2-中心氯原子的雜化軌道類型為___________,寫出一個ClO2-的等電子體__________。
(6)右圖為碘晶體晶胞結構。有關說法中正確的是_________。
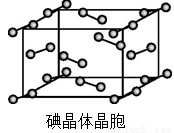
A.碘分子的排列有2種不同的取向,2種取向不同的碘分子以4配位數交替配位形成層結構
B.用均攤法可知平均每個晶胞中有4個碘原子
C.碘晶體為無限延伸的空間結構,是原子晶體
D.碘晶體中存在的相互作用有非極性鍵和范德華力
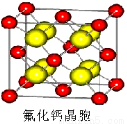
(7)已知CaF2晶體(見右圖)的密度為ρg/cm3,NA為阿伏加德羅常數,棱上相鄰的兩個Ca2+的核間距為a cm,則CaF2的相對分子質量可以表示為___________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com