
【題目】在一定溫度下,將一定量的氣體通入體積為2L的密閉容器中,使其發生反應,有關物質X、Y、Z的物質的量的變化如圖所示。則下列有關推斷正確的是

A.t時,X、Y、Z的質量不再改變
B.該反應的化學方程式為:3Z=3X+2Y
C.t時,Z的濃度為1.2mol/L
D.t時,反應停止,反應速率為0
【答案】A
【解析】
根據圖象,Z的物質的量逐漸減少,X、Y的物質的量逐漸增大,說明Z為反應物,X、Y為生成物,最終達到平衡狀態,說明為可逆反應,結合物質的量的變化關系判斷反應的方程式,再結合化學反應速率和平衡狀態的特征分析判斷。
A.根據圖象,t時為平衡狀態,化學平衡時各組分的濃度不再隨時間變化而變化,故X、Y、Z的質量也不再改變,故A正確;
B.由圖可知,X、Y的物質的量增大,為生成物,Z物質的量減小,為反應物,到達平衡后,X生成1.8mol,Y生成1.2mol,Z反應1.8mol,X、Y、Z的化學計量數之比=1.8∶1.2∶1.8=3∶2∶3,則反應的化學方程式為:3Z3X+2Y,故B錯誤;
C.根據圖象可知,平衡時Z的濃度為![]() =0.6mol/L,故C錯誤;
=0.6mol/L,故C錯誤;
D.t時為平衡狀態,反應處于平衡時正、逆反應速率相等,但不等于零,故D錯誤;
故選A。


 100分闖關期末沖刺系列答案
100分闖關期末沖刺系列答案 名校聯盟快樂課堂系列答案
名校聯盟快樂課堂系列答案科目:高中化學 來源: 題型:
【題目】甲醇是重要的綠色能源之一,目前科學家用水煤氣(CO+H2)合成甲醇,其反應為:CO(g)+2H2(g) ![]() CH3OH(g)△H=-128.1kJ·mol-1
CH3OH(g)△H=-128.1kJ·mol-1
回答下列問題:
(1)該反應是可逆反應,為使化學反應速率和CO的轉化率都同時提高的措施有_____。
A、升高溫度 B、增大壓強 C、充入氫氣 D、分離出甲醇
(2)恒溫恒容條件能說明該可逆反應達平衡的是_________;
A.2v正(H2)=v逆(CH3OH)
B.n(CO):n(H2):n(CH3OH)=1:2:1
C.混合氣體的密度不變
D.混合氣體的平均相對分子質量不變
(3)若上述可逆反應在恒溫恒容的密閉容器進行,起始時間向該容器中充入1molCO(g)和2molH2(g)。實驗測得H2的平衡轉化率隨溫度(T)、壓強(P)的變化如圖所示。
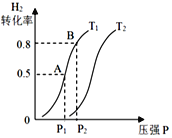
①該反應的△S____0,圖中的T1___T2(填“<”“>”或“=”)
②T1下到達平衡狀態A時,容器的體積為2L,此時該反應的平衡常數為______,若達到平衡狀態B時,則容器的體積V(B)=______L。
(4) CO燃燒的熱化學方程式:CO(g)+ 1/2 O2(g)═CO2(g)△H= —283.0kJmol-1
H2(g)+1/2 O2(g)═H2O(l)△H= —285.8 kJmol-1
CO(g)+2H2(g)═CH3OH(l)△H= —128.1KJmol-1
則CH3OH(g)燃燒熱的熱化學方程式是為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘在醫藥衛生、高純度金屬提煉、光學儀器等領域起著至關重要的作用。從含碘化鉀廢液(可能還含有I2、IO3-)中回收I2,實驗過程如下:
(1)確定碘的存在形式
①I2的確定:取含碘廢液放入試管,加入CCl4,振蕩靜置,現象為_____,確定含有I2。
②IO3-的確定:取①中上層溶液,加入少量新配制的0.1mo/LFeSO4溶液,它的作用是____。振蕩使之充分反應,再加入少量CCl4,CCl4層無紫色出現,說明該含碘廢液中無IO3-。
(2)碘的回收
在含碘廢液中加入適量的K2Cr2O7溶液和稀H2SO4,充分反應后經減壓過濾得到粗碘,由粗碘提純精制碘的裝置如圖:
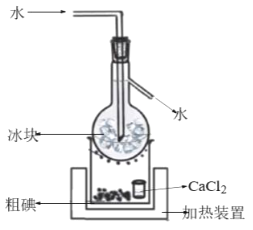
①補全得到粗碘的離子方程式:______。
□Cr2O72-+□I-+□ =□ +□Cr3++□ 。
②CaCl2的作用是__。
(3)碘的純度分析(已知:2S2O32-+I2=2I-+S4O62-)
精確量取0.1136g精制后的碘置于250mL碘量瓶中,加入0.5gKI和30mL水,振蕩至完全溶解(KI僅用于溶解)。以0.0513mol·L-1的Na2S2O3溶液快速滴定至淡黃色,加入1mL左右淀粉溶液,緩慢滴定至____,消耗Na2S2O3溶液17.26mL。碘的純度的計算表達式為____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在電解煉鋁過程中加入冰晶石(用“A”代替),可起到降低Al2O3熔點的作用。冰晶石的生產原理為2Al(OH)3+12HF+3Na2CO3═2A+3CO2↑+9H2O。根據題意完成下列填空:
(1)冰晶石的化學式為________,含有的化學鍵類型為_________________。
(2)生成物中含有一個10個電子的分子,該分子的空間構型為________,中心原子的雜化方式為________。
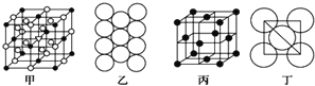
(3)冰晶石由兩種微粒構成,冰晶石的晶胞結構如圖甲所示,●位于大立方體的頂點和面心,○位于大立方體的12條棱的中點和8個小立方體的體心,那么大立方體的體心處所代表的微粒是________(填微粒符號)。
(4)Al單質的晶體中原子的堆積方式如圖乙所示,其晶胞特征如圖丙所示,原子之間相互位置關系的平面圖如圖丁所示。則一個晶胞中Al原子的數目為________個。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】漢黃芩素是傳統中草藥黃芩的有效成分之一,對腫瘤細胞的殺傷有獨特作用。下列有關漢黃芩素的敘述正確的是( )

A. 漢黃芩素的分子式為C16H13O5
B. 該物質遇FeCl3溶液不顯色
C. 1 mol該物質與溴水反應,最多消耗2 mol Br2
D. 與足量H2發生加成反應后,該分子中官能團的種類減少1種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列實驗對應的離子方程式正確的是( )
A.鋁溶解在NaOH溶液中:2Al+2OH-=2AlO2-+3H2↑
B.向溴水中通入SO2后褪色:SO2+Br2+2H2O=SO42-+2Br-+4H+
C.白醋與84消毒液混合產生黃綠色氣體:Cl-+ClO-+2H+=Cl2↑+H2O
D.少量鐵溶于過量稀硝酸中:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以下是化學反應中的能量變化圖,該反應方程式為A2+B2==2AB,回答下列問題

(1)該反應中,反應物斷鍵吸收的能量為_______________kJ/mol,生成物成鍵釋放的能量為_______________kJ/mol屬于_______________(填“放熱”“吸熱”)反應,該反應的該反應的△H=_______________(用字母寫出表達式)
(2)已知反應有下列反應
①Fe+2HCl=FeCl2+H2↑ ②H2SO4+2NaOH=Na2SO4+2H2O
③CO+CuO=Cu+CO2↑ ④Ba(OH)2·8H2O+2NH4Cl=BaCl2+2NH3↑+10H2O
與圖片所示化學反應熱效應相同的是_______________(填序號)
(3)以下說法正確的是_______________
A.中和反應是吸熱反應
B.鋁熱反應需要在高溫條件下進行,鋁熱反應屬于吸熱反應
C.放熱反應發生時有可能需要加熱
D.凡是放出熱量的化學反應均可用來造福人類
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列操作中,完全正確的一組是
①用試管夾夾持試管時,試管夾從試管底部往上套,夾在試管的中上部
②給盛有液體的體積超過![]() 容積的試管加熱
容積的試管加熱
③把鼻孔靠近容器口去聞氣體的氣味
④將試管平放,用紙槽往試管里送入固體粉末后,然后豎立試管
⑤加熱坩堝要墊上石棉網
⑥將燒瓶放在桌上,用力塞緊塞子
⑦用坩堝鉗夾取加熱后的蒸發皿
⑧將滴管豎直伸入試管內滴加液體
⑨稀釋濃硫酸時,應沿器壁緩緩地將水加入濃硫酸中
⑩用鑷子從煤油中取出金屬鈉,再用小刀切一小塊,然后將剩下的鈉放回原瓶
A.①④⑦⑩B.①④⑤⑦⑩C.①④⑤⑦⑧⑩D.④⑤⑦⑩
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最早的麻醉藥是從南美洲生長的古柯植物提取的可卡因,目前人們已實驗并合成了數百種局部麻醉劑,多為羧酸酯類。F是一種局部麻醉劑,其合成路線:
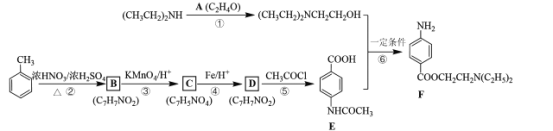
回答下列問題:
(1)已知A的核磁共振氫譜只有一個吸收峰,寫出A的結構簡式____。
(2)B的化學名稱為________。
(3)D中的官能團名稱為____,④和⑤的反應類型分別為________、____。
(4)寫出⑥的化學方程式____。
(5)C的同分異構體有多種,其中-NO2直接連在苯環上且能發生銀鏡反應的有_____種,寫出其中苯環上一氯代物有兩種的同分異構體的結構簡式____________。
(6)參照上述流程,設計以對硝基苯酚鈉、乙醇和乙酰氯(CH3COCl)為原料合成解熱鎮痛藥非那西丁(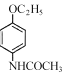 )的合成路線(無機試劑任選)。已知:
)的合成路線(無機試劑任選)。已知: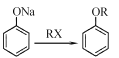 __________
__________
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com