
(18分)實驗一:某化學(xué)小組為比較鹽酸和醋酸的酸性,設(shè)計了如下實驗方案。裝置如圖:
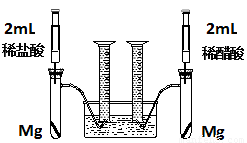
實驗方案:在兩試管中分別加入過量鎂條,同時將兩注射器中的溶液注入相應(yīng)試管中,觀察產(chǎn)生氫氣的速率和體積。
(1)鹽酸與鎂反應(yīng)的離子方程式為 。
(2)在上述實驗方案中有一明顯欠缺,該欠缺是 。
(3)在欠缺已經(jīng)改正的方案下,反應(yīng)起始時,產(chǎn)生氫氣的速率關(guān)系應(yīng)是 ;最終產(chǎn)生氫氣的體積關(guān)系應(yīng)是 。
(4)實驗中產(chǎn)生的氫氣體積比理論值高,可能原因是 。
(5)通過比較起始反應(yīng)的速率可以得出的結(jié)論是 。
(6)除上述方法外,還可以通過其他方法比較鹽酸和醋酸的酸性,請寫出其中一種更簡單的方法
。
實驗二:某二元酸(H2B)在水中的電離方程式是: H2B=H++HB-
HB- H++B2-
H++B2-
回答下列問題:
(1)請判斷H2B是強電解質(zhì)還是弱電解質(zhì)?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,則0.1mol·L-1 H2B溶液中氫離子的物質(zhì)的量濃度應(yīng) 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列離子濃度關(guān)系式正確的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各種離子濃度由大到小的順序是_______________________。
科目:高中化學(xué) 來源: 題型:
| 428c |
| a |
| 428c |
| a |
| ||
| ||
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
(18分)實驗一:某化學(xué)小組為比較鹽酸和醋酸的酸性,設(shè)計了如下實驗方案。裝置如圖:
實驗方案:在兩試管中分別加入過量鎂條,同時將兩注射器中的溶液注入相應(yīng)試管中,觀察產(chǎn)生氫氣的速率和體積。
(1)鹽酸與鎂反應(yīng)的離子方程式為 。
(2)在上述實驗方案中有一明顯欠缺,該欠缺是 。
(3)在欠缺已經(jīng)改正的方案下,反應(yīng)起始時,產(chǎn)生氫氣的速率關(guān)系應(yīng)是 ;最終產(chǎn)生氫氣的體積關(guān)系應(yīng)是 。
(4)實驗中產(chǎn)生的氫氣體積比理論值高,可能原因是 。
(5)通過比較起始反應(yīng)的速率可以得出的結(jié)論是 。
(6)除上述方法外,還可以通過其他方法比較鹽酸和醋酸的酸性,請寫出其中一種更簡單的方法
。
實驗二:某二元酸(H2B)在水中的電離方程式是: H2B=H++HB- HB- H++B2-
回答下列問題:
(1)請判斷H2B是強電解質(zhì)還是弱電解質(zhì)?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,則0.1mol·L-1 H2B溶液中氫離子的物質(zhì)的量濃度應(yīng) 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列離子濃度關(guān)系式正確的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)=c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各種離子濃度由大到小的順序是_______________________。
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:
實驗一:某化學(xué)小組為比較鹽酸和醋酸的酸性,設(shè)計了如下實驗方案。裝置如圖:
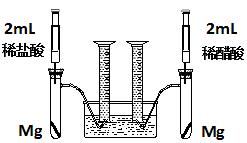
實驗方案:在兩試管中分別加入過量鎂條,同時將兩注射器中的溶液注入相應(yīng)試管中,觀察產(chǎn)生氫氣的速率和體積。
(1)鹽酸與鎂反應(yīng)的離子方程式為 。
(2)在上述實驗方案中有一明顯欠缺,該欠缺是 。
(3)在欠缺已經(jīng)改正的方案下,反應(yīng)起始時,產(chǎn)生氫氣的速率關(guān)系應(yīng)是 ;最終產(chǎn)生氫氣的體積關(guān)系應(yīng)是 。
(4)實驗中產(chǎn)生的氫氣體積比理論值高,可能原因是 。
(5)通過比較起始反應(yīng)的速率可以得出的結(jié)論是 。
(6)除上述方法外,還可以通過其他方法比較鹽酸和醋酸的酸性,請寫出其中一種更簡單的方法
。
實驗二:某二元酸(H2B)在水中的電離方程式是: H2B=H++HB- HB-![]() H++B2-
H++B2-
回答下列問題:
(1)請判斷H2B是強電解質(zhì)還是弱電解質(zhì)?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,則0.1mol·L-1 H2B溶液中氫離子的物質(zhì)的量濃度應(yīng) 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列離子濃度關(guān)系式正確的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各種離子濃度由大到小的順序是_______________________。
查看答案和解析>>
科目:高中化學(xué) 來源:廣西柳鐵一中2010-2011學(xué)年高三第二次月考 題型:實驗題
實驗一:某化學(xué)小組為比較鹽酸和醋酸的酸性,設(shè)計了如下實驗方案。裝置如圖:
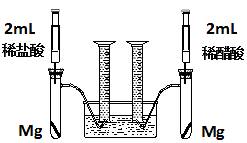 實驗方案:在兩試管中分別加入過量鎂條,同時將兩注射器中的溶液注入相應(yīng)試管中,觀察產(chǎn)生氫氣的速率和體積。
實驗方案:在兩試管中分別加入過量鎂條,同時將兩注射器中的溶液注入相應(yīng)試管中,觀察產(chǎn)生氫氣的速率和體積。
(1)鹽酸與鎂反應(yīng)的離子方程式為 。
(2)在上述實驗方案中有一明顯欠缺,該欠缺是
。
(3)在欠缺已經(jīng)改正的方案下,反應(yīng)起始時,產(chǎn)生氫氣的速率關(guān)系應(yīng)是 ;最終產(chǎn)生氫氣的體積關(guān)系應(yīng)是 。
(4)實驗中產(chǎn)生的氫氣體積比理論值高,可能原因是 。
(5)通過比較起始反應(yīng)的速率可以得出的結(jié)論是 。
(6)除上述方法外,還可以通過其他方法比較鹽酸和醋酸的酸性,請寫出其中一種更簡單的方法
。
實驗二:某二元酸(H2B)在水中的電離方程式是: H2B=H++HB- HB- H++B2-
H++B2-
回答下列問題:
(1)請判斷H2B是強電解質(zhì)還是弱電解質(zhì)?
(2)已知0.1mol·L-1 NaHB溶液的pH=2,則0.1mol·L-1 H2B溶液中氫離子的物質(zhì)的量濃度應(yīng) 0.11 mol·L-1(填“<”,“>”或“=”)
(3)在0.1mol/L的Na2B溶液中,下列離子濃度關(guān)系式正確的是_______。
A.c(H+)+c(HB-)+c(H2B)=0.1mol/L B.c(Na+)+c(OH-)=c(H+)+ c(HB-)
C.c(Na+)+ c(H+)= c(OH-)+ c(HB-)+2c(B2-) D.c(Na+)=2c(B2-)+2 c(HB-)
(4)0.1mol/LNaHB溶液中各種離子濃度由大到小的順序是_______________________。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com