
【題目】現有下列物質:①高錳酸鉀 ②鎂 ③氧氣 ④氫氧化鈉 ⑤硫酸 ⑥甲烷 ⑦![]() 膠體 ⑧硫酸銅
膠體 ⑧硫酸銅
(1)以上物質屬于電解質的是_________,屬于非電解質的是_______。(填序號)
(2)屬于有機物的是__________。(填序號)
(3)鑒別膠體和溶液最簡單有效的物理方法是_____;分離膠體和溶液常用的物理方法是_____。
(4)從上述物質中選出一種或兩種為反應物,按下列反應類型各寫一個反應化學方程式:
①化合反應:______;
②分解反應:______;
③置換反應:______;
④復分解反應:________。
【答案】①④⑤⑧ ⑥ ⑥ 丁達爾效應 滲析 ![]() (答案合理即可)
(答案合理即可) ![]() (答案合理即可)
(答案合理即可) ![]() (答案合理即可)
(答案合理即可) ![]() (答案合理即可)
(答案合理即可)
【解析】
(1)在水溶液中或熔融狀態下能導電的化合物為電解質,在水溶液中和熔融狀態下均不能導電的化合物為非電解質,單質和混合物,既不屬于電解質,也不屬于非電解質;
(2)含碳元素的化合物為有機物;
(3)丁達爾效應是膠體特有的性質,可用以鑒別膠體和溶液,根據膠體和溶液分散質粒子的大小選擇分離方法;
(4)①兩種或兩種以上的物質反應生成一種物質的反應為化合反應;
②一種物質反應生成兩種或兩種以上物質的反應為分解反應;
③一種單質和一種化合物反應生成另一種單質和另一種化合物的反應為置換反應;
④兩種化合物相互交換成分生成另外兩種化合物的反應為復分解反應。
(1)在水溶液中或熔融狀態下能導電的化合物為電解質,在水溶液中和熔融狀態下均不能導電的化合物為非電解質,
①高錳酸鉀在水溶液中和熔融狀態下均能導電,屬于電解質;
②鎂是單質,既不屬于電解質,也不屬于非電解質;
③氧氣是單質,既不屬于電解質,也不屬于非電解質;
④氫氧化鈉在水溶液中和熔融狀態下均能導電,屬于電解質;
⑤硫酸在水溶液中能導電,屬于電解質;
⑥甲烷在水溶液中和熔融狀態下均不能導電,屬于非電解質;
⑦![]() 膠體是混合物,既不屬于電解質,也不屬于非電解質;
膠體是混合物,既不屬于電解質,也不屬于非電解質;
⑧硫酸銅在水溶液中和熔融狀態下均能導電,屬于電解質;
綜上所述,以上物質中,屬于電解質的是①④⑤⑧,屬于非電解質的是⑥,故答案為:①④⑤⑧;⑥;
(2)含碳元素的化合物為有機物,故⑥甲烷是有機物,故答案為:⑥;
(3)丁達爾效應是膠體特有的性質,則鑒別膠體和溶液最簡單有效的物理方法是丁達爾效應,膠體不能透過半透膜,溶液可以透過半透膜,利用半透膜可以分離膠體和溶液,操作為滲析,故答案為:丁達爾效應;滲析;
(4)①兩種或兩種以上的物質反應生成一種物質的反應為化合反應,Mg在O2中燃燒為化合反應,化學方程式為![]() ,故答案為:
,故答案為:![]() (答案合理即可);
(答案合理即可);
②一種物質反應生成兩種或兩種以上物質的反應為分解反應,故KMnO4分解生成K2MnO4、MnO2和O2為分解反應,化學方程式為![]() ,故答案為:
,故答案為:![]() (答案合理即可);
(答案合理即可);
③一種單質和一種化合物反應生成另一種單質和另一種化合物的反應為置換反應,故Mg和硫酸反應生成MgSO4和氫氣的反應為置換反應,化學方程式![]() ,故答案為:
,故答案為:![]() (答案合理即可);
(答案合理即可);
④兩種化合物相互交換成分生成另外兩種化合物的反應為復分解反應,NaOH和CuSO4反應生成Cu(OH)2沉淀和Na2SO4的反應為復分解反應,化學方程式為![]() ,故答案為:
,故答案為:![]() (答案合理即可)。
(答案合理即可)。


 提分百分百檢測卷單元期末測試卷系列答案
提分百分百檢測卷單元期末測試卷系列答案科目:高中化學 來源: 題型:
【題目】科學家預測第114號元素具有良好的力學、光學、電學等性質。下列對114號元素的敘述錯誤的是( )
A.該元素的位于第7周期第Ⅳ![]() 族,是金屬元素
族,是金屬元素
B.該元素的主要化合價為+2、+4
C.該元素的最高價氧化物有較強的氧化性
D.該元素的原子半徑小于同主族其他元素的原子半徑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】練江整治已刻不容緩,其中以印染工業造成的污染最為嚴重。某工廠擬綜合處理含NH4+ 廢水和工業廢氣(主要含N2、CO2、SO2、NO、CO),設計了如下工業流程:
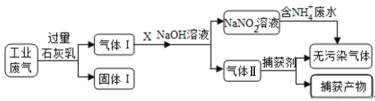
下列說法錯誤的是
A. 氣體I中主要含有的氣體有N2、NO、CO
B. X在反應中作氧化劑,可通入過量的空氣
C. 處理含NH4+廢水時,發生離子方程式是:NH4++NO2-=N2↑+2H2O
D. 捕獲劑所捕獲的氣體主要是CO
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氨是一種重要的化工原料,可以用來制備氮化硅(Si3N4)肼(N2H4)、氫氰酸(HCN)。
(1)已知:Si(s)+2Cl2(g)====SiCl4(g) △H1=akJ·mol-1
N2(g)+3H2(g) ![]() 2NH3(g) △H2=bkJ·mol-1
2NH3(g) △H2=bkJ·mol-1
3Si(s)+2N2(g)====Si3N4(s) △H3=ckJ·mol-1
H2(g)+Cl2(g)====2HCl(g) △H4=dkJ·mol-1
則反應3SiCl4(g)+4NH3(g)====Si3N4(s)+12HCl(g)的△H=________________kJ·mol-1(用a、b、c、d表示)。
(2)肼的制備方法是用次氯酸鈉氧化過量的氨。
已知ClO-水解的方程式為:ClO-+H2 O=HClO+OH-。常溫下,該水解反應的平衡常數為K=1.0×10-6mol·L-1,則1.0mol· L -1NaCIO溶液的pH=________。
(3)工業上利用氨氣生產氫氰酸(HCN)的反應為:CH4(g)+NH3(g) ![]() HCN(g)+3H2 (g) △H>O
HCN(g)+3H2 (g) △H>O
①其他條件一定,達到平衡時NH3轉化率隨外界條件X變化的關系如圖所示。X代表的是________(填“溫度”或“壓強”)。

②其他條件一定,向2L密閉容器中加人 n mol CH4和2 mol NH3,平衡時NH3體積分數隨n變化的關系如圖所示。若反應從開始到a點所用時間為10min,該時間段內用CH4的濃度變化表示的反應速率為________mol·L-1·min-1;平衡常數:K(a) ________K(b)(填“>”“=”或“<”)
③工業上用電解法處理含氰電鍍廢水(pH=10)的裝置如圖所示。

陽極產生的氯氣與堿性溶液反應生成ClO-,ClO-將CN-氧化的離子方程式為:_____CN-+ _____ClO-+ ________====_____CO32-+_____N2↑+________+________若電解處理2 mol CN-,則陰極產生氣體的體積(標準狀況下)為________L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2019年諾貝爾化學獎授予在鋰電池發展上做出貢獻的三位科學家。某可連續工作的液流鋰離子儲能電池放電時工作原理如圖所示,下列說法正確的是
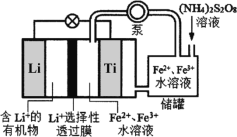
A.放電時,儲罐中發生反應:S2O82-+2Fe2+=2Fe3++2SO42-
B.放電時,Li電極發生了還原反應
C.放電時,Ti電極發生的電極方程式為:Fe2+-e=Fe3+
D.Li+選擇性透過膜可以通過Li+和H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室回收廢水中苯酚的過程如圖所示。下列分析錯誤的是
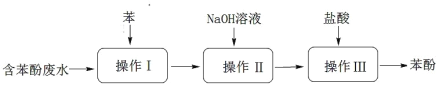
A.操作Ⅰ為萃取、分液,萃取劑也可以用選用 CCl4
B.苯酚鈉是離子化合物,在苯中的溶解度比在水中的小
C.通過操作Ⅱ,苯可循環使用,三步操作均需要分液漏斗
D.苯酚沾到皮膚上,需用 NaOH 溶液清洗后,再用大量水不斷沖洗
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】依據氧化還原反應:2Ag++Cu=Cu2++2Ag,設計的原電池如圖所示。
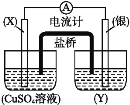
請回答下列問題:
(1)電極X的材料是___;電極X是原電池的___極;
(2)銀電極發生的電極反應為___;
(3)今有2H2+O2![]() 2H2O反應構成燃料電池,則正極通的應是___;負極的電極反應式為___。
2H2O反應構成燃料電池,則正極通的應是___;負極的電極反應式為___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸四氨合銅晶體![]() 常用作殺蟲劑,媒染劑,在堿性鍍銅中也常用作電鍍液的主要成分,在工業上用途廣泛。常溫下該物質溶于水,不溶于乙醇、乙醚,在空氣中不穩定,受熱時易發生分解。某化學興趣小組以Cu粉、3mol/L的硫酸、濃氨水、10% NaOH溶液、95%的乙醇溶液、0.500 mol/L稀鹽酸、0.500 mol/L的NaOH溶液來合成硫酸四氨合銅晶體并測定其純度。
常用作殺蟲劑,媒染劑,在堿性鍍銅中也常用作電鍍液的主要成分,在工業上用途廣泛。常溫下該物質溶于水,不溶于乙醇、乙醚,在空氣中不穩定,受熱時易發生分解。某化學興趣小組以Cu粉、3mol/L的硫酸、濃氨水、10% NaOH溶液、95%的乙醇溶液、0.500 mol/L稀鹽酸、0.500 mol/L的NaOH溶液來合成硫酸四氨合銅晶體并測定其純度。
I.CuSO4溶液的制備
①稱取4g銅粉,在A儀器中灼燒10分鐘并不斷攪拌,放置冷卻。
②在蒸發皿中加入30mL 3mol/L的硫酸,將A中固體慢慢放入其中,加熱并不斷攪拌。
③趁熱過濾得藍色溶液。
(1)A儀器的名稱為____。
(2)某同學在實驗中有1.5g的銅粉剩余,該同學將制得的CuSO4溶液倒入另一蒸發皿中加熱濃縮至有晶膜出現,冷卻析出的晶體中含有白色粉末,試解釋其原因_____
II.晶體的制備
將上述制備的CuSO4溶液按如圖所示進行操作
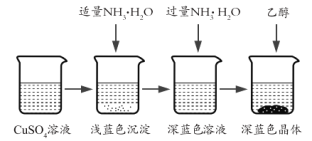
(3)已知淺藍色沉淀的成分為![]() ,試寫出生成此沉淀的離子反應方程式_________。
,試寫出生成此沉淀的離子反應方程式_________。
(4)析出晶體時采用加入乙醇的方法,而不是濃縮結晶的原因是__。
III.氨含量的測定
精確稱取mg晶體,加適量水溶解,注入如圖所示的三頸瓶中,然后逐滴加入VmL10%NaOH溶液,通入水蒸氣,將樣品液中的氨全部蒸出,并用蒸餾水沖洗導管內壁,用V1mL C1mol/L的鹽酸標準溶液完全吸收。取下接收瓶,用C2mol/L NaOH標準溶液滴定過剩的HCl(選用甲基橙作指示劑),到終點時消耗V2mLNaOH溶液。
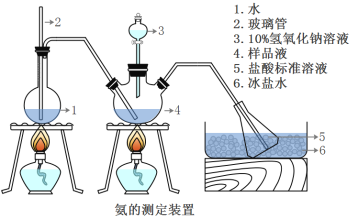
(5)A裝置中長玻璃管的作用_____,樣品中氨的質量分數的表達式_______。
(6)下列實驗操作可能使氨含量測定結果偏低的原因是_______。
A.滴定時未用NaOH標準溶液潤洗滴定管
B.讀數時,滴定前平視,滴定后俯視
C.滴定過程中選用酚酞作指示劑
D.取下接收瓶前,未用蒸餾水沖洗插入接收瓶中的導管外壁。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物R的結構簡式如圖所示。下列有關R的性質敘述正確的是( )
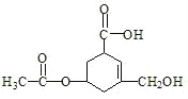
A.R的所有原子一定在同一平面上
B.在Ni催化和加熱條件下,lmolR能與3molH2發生加成反應
C.R既能與羧酸、醇反應,還能發生水解、加成和氧化反應
D.1molR與足量碳酸氫鈉溶液反應,生成CO2的物質的量為2mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com