
| A. | 酸堿鹽都是電解質 | |
| B. | 弱堿分解均生成對應的氧化物和水 | |
| C. | 酸酐不 一定是氧化物 | |
| D. | 電解原理精煉銅的過程中兩電極質量變化相同 |
分析 A、電解質是指:在水溶液中或熔融狀態下能夠導電的化合物,非電解質是在水溶液中和熔融狀態下都不能夠導電的化合物;
B、弱堿一般都不穩定,受熱易分解.一些金屬氫氧化物受熱會分解成金屬氧化物和水.但不是所有的弱堿都會分解為水和氧化物;
C、酸酐中大多數是氧化物,但是醋酸酐(C4H6O3)就不是氧化物;
D、電解過程中,陽極上不僅有銅還有其它金屬失電子;
解答 解:A.酸堿鹽在水溶液中或熔融狀態下能電離出自由移動的離子而導電,屬于化合物,是電解質,故A正確;
B、弱堿一般都不穩定,受熱易分解.一些金屬氫氧化物受熱會分解成金屬氧化物和水.但不是所有的弱堿都會分解為水和氧化物,如:NH3•H2O=NH3↑+H2O,故B錯誤;
C、酸酐中大多數是氧化物,但是醋酸酐(C4H6O3)就不是氧化物,酸酐不一定是氧化物,故C正確;
D、電解過程中,陽極上不僅有銅還有其它金屬失電子,陰極上只有銅離子得電子,所以陽極減少的質量不等于陰極增加的質量,故D錯誤;
故選AC.
點評 本題考查了電解質的概念分析和物質分類,弱堿分解特征,電解精煉的原理應用,注意有些化學概念極易混淆,比如氧化物和含氧化合物就不完全相同:氧化物由兩種元素組成其中一種是氧元素,而含氧化合物只要組成中有氧元素即可,像醋酸酐是含氧化合物就不是氧化物,題目較簡單.


科目:高中化學 來源: 題型:選擇題
| A. | 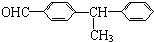 | B. | 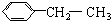 | ||
| C. | CH2=CHCH=CHCH=CH2 | D. | (CH3)2CH-C≡C-CH=CHCH3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金剛石為網狀結構,由共價鍵形成的碳原子環中,最小的環上有6個碳原子 | |
| B. | 氯化鈉晶體中,每個Na+周圍距離相等的Na+共有12個 | |
| C. | 干冰晶體中,每個CO2分子周圍緊鄰12個CO2分子 | |
| D. | 金屬銅屬于六方最密堆積結構,金屬鎂屬于面心立方最密堆積結構 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.2mol/L的AlCl3溶液中,陽離子總數大于0.2NA | |
| B. | 工業制取漂白粉時,理論上每制得25.4g產品,反應中轉移電子數為0.2NA | |
| C. | 30g甲酸甲酯與30g葡萄糖中含C-H鍵個數均為2NA | |
| D. | 將2.7g鋁粉投入足量的熱的濃硝酸中充分反應,可收集到標況下氣體6.72 L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子中三個碳原子可能處于同一直線上 | |
| B. | 全氟丙烷的電子式為: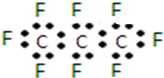 | |
| C. | 相同壓強下,沸點:C3F8<C3H8 | |
| D. | 全氟丙烷分子是既有極性鍵又有非極性鍵的極性分子 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱反應比吸熱反應更容易發生 | |
| B. | 凡是在加熱或點燃條件下進行的反應都是吸熱反應 | |
| C. | 向1L 1 mol/L NaOH溶液中加入一定量濃H2SO4溶液至恰好反應完全時,共放出65 kJ的熱量.則表示該反應的中和熱的熱化學方程式為:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-65kJ•mol-1 | |
| D. | 已知:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1,由此可知CO的燃燒熱為283 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ③ | B. | ②③ | C. | ①②③ | D. | ①③ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com