
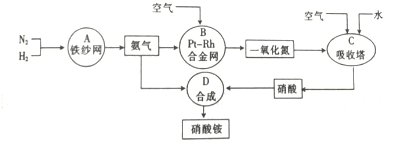
分析 (1)工業制氮氣的原理是分離液態空氣,其方法是將空氣加壓降溫成液態空氣,然后略微升溫,沸點低的先逸出;
(2)①NH3與NaClO反應可得到肼(N2H4),N元素的化合價升高,Cl元素的化合價降低;
②肼和亞硝酸(HNO2)反應時發生歸中反應生成氫疊氮酸(HN3),H和O元素未發生氧化還原反應,據此書寫化學方程式;
(3)氫疊氮酸(HN3)只由兩種元素構成,故受撞擊時爆炸分解成常見的兩種單質為氫氣和氮氣,據此書寫反應;
(4)根據反應中各物質的組成元素的化合價是否發生變化來判斷是否發生氧化還原反應.
解答 解:(1)氧氣的沸點是-183℃,氮氣的沸點是-196℃,工業制氮氣的原理是分離液態空氣,其方法是將空氣加壓降溫成液態空氣,然后略微升溫,沸點低的氮氣先逸出,此方法為液態空氣的分餾,
故答案為:分餾;
(2)①NH3與NaClO反應可得到肼(N2H4),N元素的化合價升高,Cl元素的化合價降低,則NaClO氧化劑;
故答案為:NaClO;
②肼和亞硝酸(HNO2)反應時發生歸中反應生成氫疊氮酸(HN3),H和O元素未發生氧化還原反應,故化學方程式為N2H4+HNO2═HN3+2H2O,
故答案為:N2H4+HNO2═HN3+2H2O;
(3)氫疊氮酸(HN3)只由兩種元素構成,故受撞擊時爆炸分解成常見的兩種單質為氫氣和氮氣,故化學方程式為:2HN3=H2↑+3N2↑,
故答案為:2HN3=H2↑+3N2↑;
(4)題中涉及的化學反應有:A、N2+3H2?2NH3,B、4NH3+5O2 $\frac{\underline{催化劑}}{△}$4NO+6H2O,C、2NO+O2═2NO2、3NO2+H2O═2HNO3+NO、4NO2+O2+H2O═4HNO3,D、NH3+HNO3═NH4NO3,其中A、B、C屬于氧化還原反應,
故答案為:ABC.
點評 本題考查了氧化還原反應的判斷、化學方程式的書寫等知識,題目難度稍大,試題題量較大,涉及的知識點較多,充分考查了學生的分析、理解能力及靈活應用所學知識的能力.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
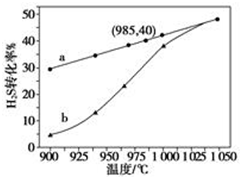 在恒容密閉容器中,控制不同溫度進行H2S分解實驗:2H2S(g)?2H2(g)+S2(g),以H2S起始濃度均為c mol•L-1測定H2S的轉化率,結果見圖.圖中a為H2S的平衡轉化率與溫度關系曲線,b曲線表示不同溫度下反應經過相同時間且未達到化學平衡時H2S的轉化率.據圖計算985℃時H2S按上述反應分解的平衡常數K=$\frac{0.8c}{9}$;說明隨溫度的升高,曲線b向曲線a逼近的原因:溫度升高,反應速率加快,達到平衡所需的時間縮短.
在恒容密閉容器中,控制不同溫度進行H2S分解實驗:2H2S(g)?2H2(g)+S2(g),以H2S起始濃度均為c mol•L-1測定H2S的轉化率,結果見圖.圖中a為H2S的平衡轉化率與溫度關系曲線,b曲線表示不同溫度下反應經過相同時間且未達到化學平衡時H2S的轉化率.據圖計算985℃時H2S按上述反應分解的平衡常數K=$\frac{0.8c}{9}$;說明隨溫度的升高,曲線b向曲線a逼近的原因:溫度升高,反應速率加快,達到平衡所需的時間縮短.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
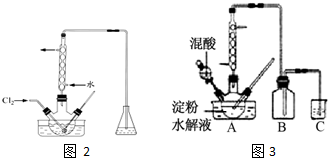
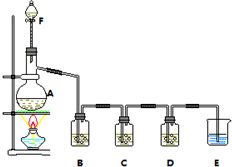 某小組欲探究Cl2與KI溶液的反應,設計實驗裝置如下圖.
某小組欲探究Cl2與KI溶液的反應,設計實驗裝置如下圖.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
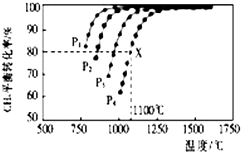 在密閉容器中通入物質的量濃度均為0.1的CH4與CO2,在一定條件下發生反應CH4(g)+CO2(g)?2CO(g)+2H2(g),測得CH4的平衡轉化率與溫度、壓強的關系如圖所示.
在密閉容器中通入物質的量濃度均為0.1的CH4與CO2,在一定條件下發生反應CH4(g)+CO2(g)?2CO(g)+2H2(g),測得CH4的平衡轉化率與溫度、壓強的關系如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
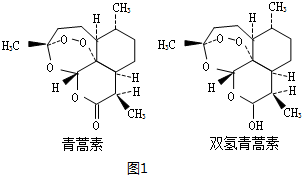
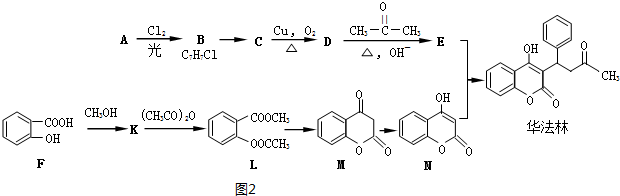
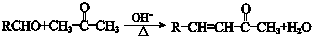
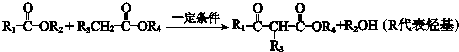
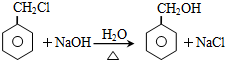 ;
;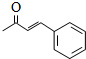 .L→M的轉化中,會產生少量鏈狀高分子聚合物,該聚合物的結構簡式為
.L→M的轉化中,會產生少量鏈狀高分子聚合物,該聚合物的結構簡式為 .
.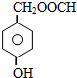 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com