
(12分)堿式碳酸銅[Cu2(OH)2C03]是一種用途廣泛的化工原料。工業上可用電子工業中刻蝕線路板的酸性廢液(主要成分有FeCl3、CuCl2、FeCl2)制備,其制備過程如下:
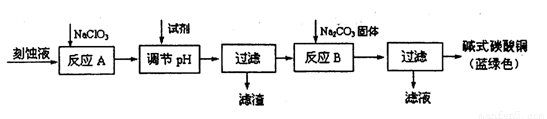
查閱資料知,通過調節溶液的酸堿性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
|
物質 |
Cu(OH)2 |
Fe(OH)2 |
Fe(OH)3 |
|
開始沉淀pH |
6.0 |
7.5 |
1,4 |
|
沉淀完全pH |
13 |
14 |
3.7 |
(1)氯酸鈉的作用是 ;
(2)調節溶液A的pH范圍為 ,可以選擇的試劑是 .(填序號)。
a.氨水 b.硫酸銅 c.氫氧化銅 d.碳酸銅
(3)反應B的溫度要控制在60℃左右,且保持恒溫,可采用的加熱方法是 ;若溫度過高,所得藍綠色沉淀中會有黑色固體出現,黑色固體可能是 。
(4)已知濾液中含有碳酸氫鈉,寫出生成堿式碳酸銅的離子方程式: 。
(5)過濾得到的產品洗滌時,如何判斷產品已經洗凈 。
(1)將Fe2+氧化成Fe3+ (2)3.7~6.0 cd (3)水浴加熱 CuO
(4)2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-
(5)取最后一次洗滌液,加入硝酸銀、硝酸溶液,無沉淀生成則表明已洗凈
【解析】(1)由于沉淀氫氧化亞鐵的pH大于沉淀氫氧化鐵的pH,所以應該把亞鐵離子氧化生成鐵離子,然后再沉淀,所以氯酸鈉的作用是將Fe2+氧化成Fe3+ 。
(2)根據表中數據可知,要沉淀氫氧化鐵,而不沉淀氫氧化銅,則溶液的pH應該控制在3.7~6.0之間;由于不能引入雜質,所以選擇的試劑是cd。
(3)要控制在60℃左右,且保持恒溫,可采用的加熱方法應該是水浴加熱;如果溫度過高,則氫氧化銅會分解生成黑色的氧化銅。
(4)根據反應物和生成物可得出反應的方程式為
2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-。
(5)由于沉淀表面含有吸附的氯離子,所以可以通過檢驗氯離子來判斷,即取最后一次洗滌液,加入硝酸銀、硝酸溶液,無沉淀生成則表明已洗凈。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||
| ||
| 22400w-65V |
| 64V |
| 22400w-65V |
| 64V |
查看答案和解析>>
科目:高中化學 來源: 題型:
 鐵、銅和鋁是人類生活中常用的金屬.
鐵、銅和鋁是人類生活中常用的金屬.查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
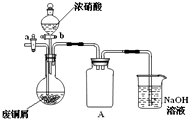 堿式碳酸銅[Cu2(OH)2CO3]是一種用途廣泛的化工原料,實驗室以廢銅屑為原料制取堿式碳酸銅的步驟如下:
堿式碳酸銅[Cu2(OH)2CO3]是一種用途廣泛的化工原料,實驗室以廢銅屑為原料制取堿式碳酸銅的步驟如下:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com