

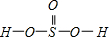 ,Se為+4價,而H2SeO4的分子結構為
,Se為+4價,而H2SeO4的分子結構為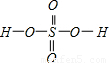 ,Se為+6價,后者Se原子吸電子能力強;
,Se為+6價,后者Se原子吸電子能力強; =3,有1對孤對電子對,為V形;SO32-離子中心原子S原子的價層電子對數為
=3,有1對孤對電子對,為V形;SO32-離子中心原子S原子的價層電子對數為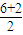 =4,有1對孤對電子對,為三角錐型,
=4,有1對孤對電子對,為三角錐型,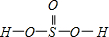 ,Se為+4價,而H2SeO4的分子結構為
,Se為+4價,而H2SeO4的分子結構為 ,Se為+6價,后者Se原子吸電子能力強,則羥基上氫原子更容易電離出H+,
,Se為+6價,后者Se原子吸電子能力強,則羥基上氫原子更容易電離出H+,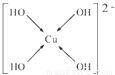 ,故答案為:
,故答案為: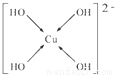 ;
; ×8+
×8+ ×6=4,含Cu:4,所以化學式為CuCl,故答案為:CuCl.
×6=4,含Cu:4,所以化學式為CuCl,故答案為:CuCl.

科目:高中化學 來源: 題型:
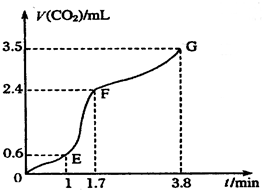 Ⅰ現欲用碳酸鈣固體和稀鹽酸反應制取CO2氣體,請回答下列問題:
Ⅰ現欲用碳酸鈣固體和稀鹽酸反應制取CO2氣體,請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:


查看答案和解析>>
科目:高中化學 來源: 題型:
| m | 2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com