
【題目】氰![]() ,硫氰
,硫氰![]() 等稱為擬鹵素,與鹵素單質性質相似,它們的陰離子與也鹵素陰離子性質相似,陰離子的還原性順序為:
等稱為擬鹵素,與鹵素單質性質相似,它們的陰離子與也鹵素陰離子性質相似,陰離子的還原性順序為:![]() ,又知,擬鹵素形成的無氧酸和含氧酸一般為弱酸,下列反應中,不合理的是( )
,又知,擬鹵素形成的無氧酸和含氧酸一般為弱酸,下列反應中,不合理的是( )
A.![]() 濃
濃![]()
![]()
![]()
B.![]()
C.![]()
D.![]()
科目:高中化學 來源: 題型:
【題目】某些牙膏中含有茶多酚,茶多酚是茶葉中多酚類物質的總稱,是目前尚不能人工合成的純天然、 多功能、高效能的抗氧化劑和自由基凈化劑。其中沒食子兒茶素(GC)的結構簡式如圖所示,下列關于GC的敘述中正確的是( )
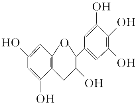
A.分子中所有的原子共面
B.1 mol GC與6 mol NaOH恰好完全反應
C.能發生氧化反應、取代反應、消去反應,難發生加成反應
D.遇FeCl3溶液不發生顯色反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氧化鋅煙灰中主要含有鋅、鉛、銅、氧、砷、氯等元素。氨法溶浸氧化鋅煙灰可制取高純鋅,工藝流程如圖所示。
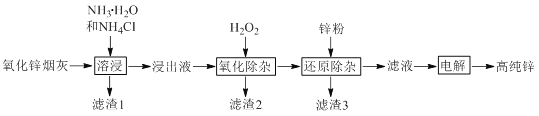
已知氧化鋅煙灰經溶浸后,其中的鋅、鉛、銅、氧、砷元素不同程度的進入浸出液中,其中鋅和砷元素分別以Zn(NH3)42+、AsCl52-的形式存在。
回答下列問題:
(1)Zn的原子序數為30,其在元素周期表中的位置為____________。
(2)鋅浸出率與溫度的關系如圖所示,分析30℃時鋅浸出率最高的原因為______________。
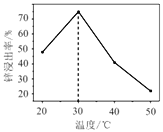
(3)“氧化除雜”中,AsCl52-轉化為As2O5膠體吸附聚沉除去,溶液始終接近中性。該反應的離子方程式__________________________________________。
(4)“濾渣3”除鋅外,主要成分為___________________。
(5)“電解”時陽極區放出一種無色無味的氣體,將其通入滴有KSCN的FeCl2溶液中,無明顯現象,該氣體是___________(寫名稱)。電解后的電解液經補充_________(寫一種物質的化學式)后可返回至__________________(填流程中的操作名稱)循環利用。
(6)ZnCl2溶液一次水解可獲得產物Zn(OH)xCly,取10.64g該水解產物,經二次水解、緞燒后,可得氧化鋅8.1g(假設各步均轉化完全)。則一次水解產物的化學式為_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學與生產和生活等聯系緊密。下列說法正確的是( )
A.“白色污染”泛指聚乙烯、聚丙烯等塑料污染,它們的分子內部都含有雙鍵
B.聚丙烯酸酯類涂料(![]() )是目前流行的墻面涂料之一,它是通過縮聚反應形成的
)是目前流行的墻面涂料之一,它是通過縮聚反應形成的
C.制作手術縫合線或人造器官材料可以是聚乳酸或聚氨酯等
D.制作航天服的聚酯纖維和用于光纜通信的光導纖維都屬于新型有機高分子材料
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某課題組利用CO2催化氫化制甲烷,研究發現HCOOH是CO2轉化為CH4的中間體,即:![]() ,鎳粉是反應I、II的催化劑。CH4、HCOOH、H2的產量和鎳粉用量的關系如圖所示(僅改變鎳粉用量,其他條件不變):
,鎳粉是反應I、II的催化劑。CH4、HCOOH、H2的產量和鎳粉用量的關系如圖所示(僅改變鎳粉用量,其他條件不變):
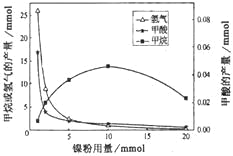
由圖可知,當鎳粉用量從1mmol增加到10mmol,反應速率的變化情況是( )
A.反應I的速率增加,反應II的速率不變
B.反應I的速率不變,反應II的速率增加。
C.反應I、II的速率均增加,且反應I的速率增加得快
D.反應I、II的速率均增加,且反應II的速率增加得快
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溴化碘![]() 的化學性質與鹵素單質相似,能與大多數金屬反應生成金屬鹵化物,和某些非金屬單質反應生成相應的鹵化物,跟水反應的方程式為IBr+H2O=HBr+HIO。下列有關IBr的敘述中,不正確的是( )
的化學性質與鹵素單質相似,能與大多數金屬反應生成金屬鹵化物,和某些非金屬單質反應生成相應的鹵化物,跟水反應的方程式為IBr+H2O=HBr+HIO。下列有關IBr的敘述中,不正確的是( )
A.IBr是雙原子分子
B.在很多反應中,IBr是強氧化劑
C.IBr和NaOH溶液反應生成NaBr和NaIO
D.IBr和水反應時,既是氧化劑又是還原劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求作答:
(1)有機物命名:
①![]() ______________________________(習慣命名法);
______________________________(習慣命名法);
②(CH3)2CHCH2CH(NH2)COOH_____________________________________(系統命名法)。
(2)書寫化學方程式:
①ClCH2CH2COONH4與氫氧化鈉的乙醇溶液共熱_______________;
②對苯二甲酸(![]() )和乙二醇一定條件下的縮聚反應______________。
)和乙二醇一定條件下的縮聚反應______________。
(3)①某芳香烴的分子式為C8H10,它的一氯代物有二種,則其結構簡式為_______;
②環己烷(C6H12)的屬于環烷烴的同分異構體,其中含三元環(三角形)的有_______種。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,除標出的元素外,表中的每個編號代表一種元素。請根據要求回答問題:

(1)②的元素符號是__________;該元素的最高價氧化物的電子式為__________;
(2)⑤和⑥兩種元素的非金屬性強弱關系是:⑤________⑥(填“>”或“<”);
(3)①和③兩種元素組成的化合物中含有的化學鍵為__________(填“離子鍵”或“共價鍵”)
(4)④和⑥兩種元素組成的化合物與AgNO3溶液反應的離子方程式為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一體積為1 L的密閉容器中,通入一定量的CO和H2O,在850 ℃ 發生如下反應:CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH<0。CO和H2O濃度變化如圖:
CO2(g)+H2(g) ΔH<0。CO和H2O濃度變化如圖:

(1)0~4 min的平均反應速率v(CO)=__________________mol·(L·min)-1。
(2)850 ℃時,平衡常數K=___________________。
(3)850 ℃時,若向該容器中充入1.0 mol CO、3.0 mol H2O,則CO的平衡轉化率為___________。
(4)能判斷該反應達到化學平衡狀態的依據是________(填選項序號)。
a.v正(H2)=v逆(H2O) b.c(CO2)=c(CO)
c.容器中氣體密度不變 d.1 mol H—H鍵斷裂的同時斷裂2 mol H—O鍵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com