
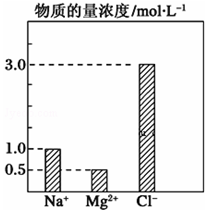
 在0.2L由NaCl、MgCl2、CaCl2組成的混合液中,部分離子濃度大小如圖所示,回答下列問題:
在0.2L由NaCl、MgCl2、CaCl2組成的混合液中,部分離子濃度大小如圖所示,回答下列問題:分析 ①由圖可知,c(Na+)=1.0mol/L,c(Mg2+)=0.5mol/L,結合n=cV、m=nM計算;
②結合電荷守恒計算c(Ca2+),結合n=cV、c=$\frac{n}{V}$計算.
解答 解:①由圖可知,c(Na+)=1.0mol/L,該混合液中,NaCl的物質的量為0.2L×1.0mol/L=0.2mol;c(Mg2+)=0.5mol/L,含溶質MgCl2的質量為0.2L×0.5mol/L×95g/mol=9.5g,
故答案為:0.2;9.5;
②由電荷守恒可知2c(Ca2+)+c(Na+)+2c(Mg2+)=c(Cl-),解得:c(Ca2+)=$\frac{3.0-1.0-0.5×2}{2}$=0.5mol/L,混合液中CaCl2的物質的量為:0.2L×0.5mol/L=0.1mol,該混合液加水稀釋至體積為1L,稀釋后溶液中Ca2+的物質的量濃度為:c=$\frac{0.1mol}{1L}$=0.1mol/L,
故答案為:0.1.
點評 本題考查了物質的量、物質的量濃度的計算,題目濃度中等,明確稀釋過程中溶質的物質的量不變及電荷守恒的應用方法為解答關鍵,注意熟練掌握物質的量濃度概念及計算方法.


科目:高中化學 來源: 題型:選擇題
| A. | 2H2O2═2H2O+O2↑ | B. | 2FeCl2+Cl2═2FeCl3 | ||
| C. | Pb2++2Cl-═PbCl2↓ | D. | Sn2++2Fe3+═Sn4++2Fe2+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時,純水中含有的H+數為1×10-7NA | |
| B. | 常溫常壓下,31g白磷與紅磷的混合物中含有磷原子數為NA | |
| C. | 35.5gCl2參加氧化還原反應,轉移的電子數可能為NA | |
| D. | 7.8gNa2O2晶體中所含離子的總數為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 上述反應涉及兩種基本反應類型 | B. | 丹砂的主要成分是硫化汞 | ||
| C. | “積變”屬于復分解反應 | D. | 丹砂“燒之”涉及氧化還原反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
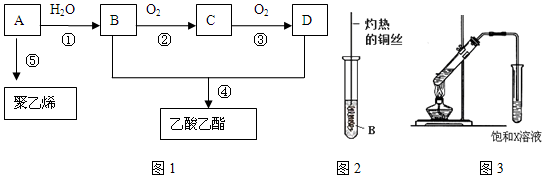
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0℃時水結冰 | |
| B. | CaO(s)+CO2(g)═CaCO3(s)△H=-175.7kJ/mol | |
| C. | (NH4)2CO3(s)═NH4HCO3(s)+NH3(g)△H=+74.9kJ/mol | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋅溶于醋酸:Zn+2H+=Zn2++H2↑ | |
| B. | 氯氣與溴化鈉溶液:2Br-+Cl2=Br2+2Cl- | |
| C. | 氯化鋁與氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 氯氣溶于水:Cl2+H2O?2H++Cl-+ClO- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸 | B. | KSCN溶液 | C. | 氨水 | D. | 燒堿溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com