
| A | B | M | X | Z |
| 最簡氫化物是含氫量最高的有機物 | 單質為氣體,元素原子中成對電子數比未成對電子數多一個 | 最簡氫化物的水溶液呈酸性 | 原子核外有5種能量不同的電子,最外層有3個電子 | 最高價氧化物對應的水化物為最強酸 |
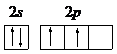
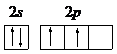
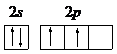 ,
,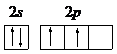 ;
;

 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案科目:高中化學 來源: 題型:
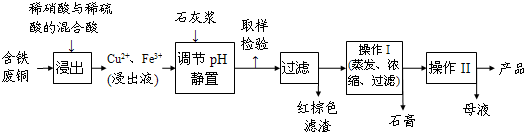
| 溫度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 膽礬 | 32 | 44.6 | 61.8 | 83.8 | 114 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| n(CH3OH) |
| n(CO) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com