
| A. | 將鈉塊投入到硫酸銅溶液中,可析出單質銅 | |
| B. | 將鈉塊長時間暴露在空氣中的最終產物是Na2CO3 | |
| C. | Na2O與Na2O2陰陽離子個數比相同 | |
| D. | Na2O2能使品紅溶液褪色且原理與SO2相同 |
分析 A、鈉和鹽溶液反應時,先和水反應,如果能發生復分解反應,則再發生復分解反應;
B、因鈉與空氣中氧氣極易反應,致使鈉表面變暗,氧化鈉與空氣中的水蒸氣反應生成白色固體氫氧化鈉,氫氧化鈉易潮解表面變成溶液,氫氧化鈉是強堿與空氣中的酸性氣體反應,生成白色帶結晶水的固體Na2CO3.10H2O,十水碳酸鈉易風化生成白色粉末碳酸鈉;
C、Na20是由鈉離子和氧離子構成的離子化合物,Na202是由鈉離子和過氧根離子構成的離子化合物;
D、Na2O2能使品紅溶液褪色是過氧化鈉的強氧化性,而SO2生成無色不穩定的大分子.
解答 解:A、鈉投入硫酸銅溶液時,鈉和水反應生成氫氧化鈉和氫氣,氫氧化鈉再和硫酸銅發生復分解反應生成氫氧化銅藍色沉淀,所以得不到金屬單質銅,故A錯誤;
B、因鈉與空氣中氧氣極易反應,致使鈉表面變暗,氧化鈉與空氣中的水蒸氣反應生成白色固體氫氧化鈉,氫氧化鈉易潮解表面變成溶液,氫氧化鈉是強堿與空氣中的酸性氣體反應,生成白色帶結晶水的固體Na2CO3.10H2O,十水碳酸鈉易風化生成白色粉末碳酸鈉,故B正確;
C、Na20是由鈉離子和氧離子構成的離子化合物,電子式為 ,所以陰陽離子個數比是1:2,Na202是由鈉離子和過氧根離子構成的離子化合物,電子式為
,所以陰陽離子個數比是1:2,Na202是由鈉離子和過氧根離子構成的離子化合物,電子式為 ,陰陽離子個數比是1:2,故C正確;
,陰陽離子個數比是1:2,故C正確;
D、Na2O2能使品紅溶液褪色是過氧化鈉的強氧化性,而SO2生成無色不穩定的大分子,所以兩的褪色的原理不同,故D錯誤;
故選BC.
點評 本題主要考查了鈉的性質與用途,注意知識的積累,學生要知道二氧化硫的漂白是生成無色不穩定的大分子,而過氧化鈉具有強氧化性,難度不大.


科目:高中化學 來源: 題型:推斷題

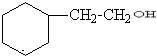 .
.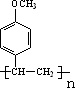 .
.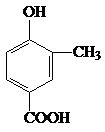 +CH3CH2OH$?_{△}^{濃H_{2}SO_{4}}$
+CH3CH2OH$?_{△}^{濃H_{2}SO_{4}}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
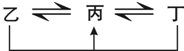 有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系:
有A、B、C、D、E、F六種前四周期的元素,原子序數依次增大,A、B、C、D、E均為短周期元素,D和F元素對應的單質為日常生活中常見金屬.A原子核內只有一個質子,元素A與B形成的氣態化合物甲具有10e-、空間構型為三角錐形,C元素原子的最外層電子數是其電子層數的3倍,C與E同主族.圖中均含D或F元素的物質均會有圖示轉化關系: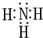 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 物質 | 雜質 | 試劑 | 主要操作 | |
| A | Cu | Fe | 鹽酸 | 過濾 |
| B | AlCl3 | NaAlO2 | 鹽酸 | - |
| C | FeCl2溶液 | FeCl3 | Fe | - |
| D | NaHCO3溶液 | Na2CO3 | CO2 | - |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若有0.2mol氧化劑反應,則轉移電子的物質的量為1.0mol | |
| B. | 若氧化產物比還原產物多0.35mol,生成8.96LN2(標準狀況) | |
| C. | 若氧化產物比還原產物多0.35mol,有0.050molKNO3被氧化 | |
| D. | KNO3的氧化性強于N2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 僅用新制氫氧化銅懸濁液(可以加熱)不能通過化學方法完成對葡萄糖溶液、乙醇和乙酸溶液的鑒別 | |
| B. | 利用加碳酸鈉飽和溶液和分液的方法可以除去乙酸乙酯中的乙酸和乙醇 | |
| C. | CH3CH2CH2OH和CH3CH2CH2Cl的同分異構體數目相同 | |
| D. | 石油的分餾、裂化,煤的干餾,都是通過化學變化獲得新物質的工業生產方法 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1:1:1 | B. | 1:1:3 | C. | 1:3:1 | D. | 3:1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 摩爾是國際單位制中的一種物理量 | B. | 摩爾是物質的量的單位 | ||
| C. | 摩爾簡稱摩,它的符號是mol | D. | 1 mol氧原子可表示為“1 mol O” |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 全部 | B. | 只有①④ | C. | 只有①③④ | D. | 只有①②④ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com