
【題目】化學與生產、生活密切相關,下列有關說法正確的是
A. 由地溝油加工合成的“生物柴油”與柴油成分相同
B. 煤的液化是將煤處理成清潔能源的一種物理方法,可減少PM2.5引起的危害
C. 海水提鎂、煉鐵、制造玻璃等工業都用到石灰石
D. 食鹽中加碘單質可以減少碘缺乏癥
科目:高中化學 來源: 題型:
【題目】對于A2 + 3B2![]() 2C+D的反應來說,以下化學反應速率的表示中,反應速率最快的是( )
2C+D的反應來說,以下化學反應速率的表示中,反應速率最快的是( )
A.v(B2) =0.8mol(Ls)-1 B.v(A2) =0.4 mol(Ls)-1
C.v(C) =0.6 mol(Ls)-1 D.v(D) =0.1 mol(Ls)-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化氯(ClO2,黃綠色易溶于水的氣體)是一種安全穩定、高效低毒的消毒劑。工業上通過惰性電極電解氯化銨和鹽酸的方法制備,其原理如圖所示:
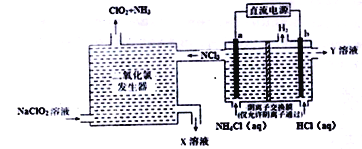
下列說法不正確的是
A. b電極接電源的負極,在b極區流出的Y溶液是稀鹽酸
B. 二氧化氯發生器中排出的X溶液中溶質主要為NaCl和NaOH
C. 電解過程中二氧化氯發生器中產生2.24L(標準狀況)NH3,則b極產生0.6gH2
D. 電解池a極的電極反應式為NH4+-6e-+4OH-+3Cl-=NCl3+4H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】完成下列實驗所選擇的裝置或儀器(夾持裝置已略去)正確的是
A.用CCl4提取溴水中的Br2[來 | B.從KI和I2的固體混合物中回收I2 | C.吸收NH3(極易溶于水),并防止倒吸 | D.工業酒精制備無水酒精 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(1)在80 g密度為d g/cm3的硫酸鐵溶液中,含有2.8 g Fe3+離子,則此溶液中SO42-的物質的量濃度為_____________
(2)由N2和CO2組成的混合氣體的密度在同溫、同壓下是氫氣密度的16倍,則該混合氣體中N2和CO2的體積比為_______________________
(3)標準狀況下,1.12LNOx氣體質量為2.3g,則x的值為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的值,下列說法正確的是
A. 100g質量分數為46%的乙醇水溶液中含有氧原子數為4NA
B. 若將1 mol氯化鐵完全轉化為氫氧化鐵膠體,則分散系中膠體微粒數為NA
C. 向大量水中通入1 mol氯氣,反應中轉移的電子數為NA
D. 電解精煉銅,當電路中通過的電子數目為0.2NA時,陽極質量減少6.4 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】關于下列各實驗裝置的敘述中,正確的是

A. 裝置①不可用于實驗室制取少量NH3或O2
B. 可用從a處加水的方法檢驗裝置②的氣密性
C. 實驗室可用裝置③收集HCl
D. 驗證溴乙烷發生消去反應生成烯烴的實驗可利用裝置④進行
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室可用KMnO4和濃鹽酸反應制取氯氣。
KMnO4+HCl(濃)=KCl+MnCl2+Cl2↑+H2O(未配平)
(1)配平化學方程式,并用單線橋標出電子轉移的方向和數目__________。
(2)將上述配平的化學方程式改寫為離子方程式__________。
(3)濃鹽酸在反應中顯示出來的性質是________。
①只有還原性 ②還原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若產生0.5 mol Cl2,則被氧化的HCl_____mol,轉移的電子的數目約為______。
(5)一定條件下,KMnO4還可以氧化其他還原性物質。___MnO4—+___C2O42—+_____=______Mn2++__CO2↑+____,完成上述離子方程式,此反應中,發生氧化反應的物質是__;若轉移1 mol電子,生成標準狀況下CO2______L。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫酸鋅可用于制造鋅鋇白、印染媒染劑等。用鋅白礦(主要成分為ZnO,還含有FeO、CuO、SiO2等雜質)制備ZnSO4·7H2O的流程如下。
已知:Ksp[Fe(OH)3]=4.0×1038,Ksp[Cu(OH)2]=2.2×1020

(1)“濾渣1”的主要成分是_______(填化學式)。“酸浸”過程中,為了提高鋅元素浸出速率,可采取的措施有:①適當提高酸的濃度,②_______(填一種)。
(2)“氧化”過程中,發生氧化還原反應的離子方程式是_______。
(3)“沉淀”過程中,加入ZnO產生Fe(OH)3沉淀的原因是_______。
(4)加入適量ZnO固體,若只析出Fe(OH)3沉淀而未析出Cu(OH)2沉淀,且測得沉淀后的溶液中c(Fe3+)=4.0×1014mol/L,此時溶液中c(Cu2+)的取值范圍是_______mol/L。
(5)加入適量鋅粉的作用是_______。
(6)由濾液得到ZnSO47H2O的操作依次為_______、_______、過濾、洗滌、干燥。實驗室中過濾操作需要使用的玻璃儀器有燒杯、_______、_______。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com