
【題目】下列反應中,既屬于氧化還原反應,又屬于吸熱反應的是
A.鋅片與稀硫酸的反應 B.灼熱的碳與水蒸氣的反應
C.甲烷在空氣中的燃燒反應 D.Ba(OH)2·8H2O與NH4Cl的反應
科目:高中化學 來源: 題型:
【題目】已知X為一種常見酸的濃溶液,能使蔗糖粉末變黑.A與X反應的轉化關系如圖所示,其中反應條件及部分產物均已略去,則下列有關說法正確的是( ) 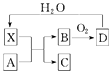
A.X使蔗糖變黑的現象主要體現了X的強氧化性
B.若A為鐵,則足量A與X在室溫下即可完全反應
C.若A為碳單質,則將C通入少量的澄清石灰水中,最后有白色沉淀產生
D.工業上,B轉化為D的反應條件為加熱、使用催化劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到的氣體其物質的量為a mol,向反應后的溶液中(存在Cu2+和SO42﹣)加入足量NaOH,產生藍色沉淀,過濾,洗滌,灼燒,得到CuO 12.0g,若上述氣體為NO和NO2的混合物,且體積比為1:1(在相同條件下),則a可能為( )
A.0.80
B.0.70
C.0.60
D.0.40
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用含少量鎂的鋁粉制取純凈的Al(OH)3,下列操作步驟可行的組合是
①加鹽酸溶解 ②加燒堿溶液溶解 ③過濾 ④通入足量二氧化碳 ⑤加過量燒堿溶液 ⑥加過量鹽酸
A.②③④③B.①⑤④③C.①⑤③⑥③D.①⑤⑥③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/mol
Na2O2(s)+CO2(g)=Na2CO3(s)+![]() O2(g)ΔH=-226kJ/mol
O2(g)ΔH=-226kJ/mol
根據以上熱化學方程式判斷,下列說法正確的是
A. CO的燃燒熱為283 kJ
B. 如圖可表示由CO生成CO2的反應過程和能量關系
C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol
D. CO(g)與Na2O2(s)反應放出509 kJ熱量時,電子轉移數為6.02×1023
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分,請回答有關問題:
主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中化學性質最不活潑的元素,其原子結構示意圖為 .
(2)③元素與⑩元素兩者核電荷數之差是
(3)設計實驗方案:比較⑦與⑩單質氧化性的強弱,請將方案填入下列空格. 實驗原理(化學方程式):
實驗現象:
結論:
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用可再生能源代替石油和煤已經成為未來發展的趨勢。甲醇作為重要的可再生能源具有廣泛的開發和應用前景。工業上常利用反應CO(g)+2H2(g)![]() CH3OH(g)△H<0來合成甲醇.
CH3OH(g)△H<0來合成甲醇.
(1)經研究發現在230℃~270℃時合成最為有利.為探尋合成氣最合適的起始組成比,分別在230℃、250℃和270℃時進行實驗,實驗結果如下圖。230℃的實驗結果所對應的曲線是______(填字母);從提高CO轉化率的角度等綜合分析,該溫度下工業生產適宜采用的合成氣組成n(H2):n(CO)的比值范圍是______(填字母).

A.1~1.5B.2.5~3C.3.5~4.5
(2)制甲醇所需要的氫氣,可通過下列反應制取:H2O(g)+CO(g)![]() H2(g)+CO2(g)△H<0,某溫度下該反應的平衡常數K=1.回答下列問題:
H2(g)+CO2(g)△H<0,某溫度下該反應的平衡常數K=1.回答下列問題:
①該溫度下,若起始時c(CO)=2mol/L,c(H2O)=3mol/L,反應進行一段時間后,測得CO的濃度為1mol/L,則此時該反應v(正)______v(逆)(填“>”、“<”或“=”).
②若降低溫度,該反應的K值將______(填“增大”、“減小”或“不變”).
(3)甲醇是一種化工原料,工業上合成甲醇的反應:CO(g)+2H2(g)![]() CH3OH(g)△H=-90.8kJ/mol.
CH3OH(g)△H=-90.8kJ/mol.
若在溫度、容積相同的3個密閉容器中,按不同方式投入反應物,保持恒溫、恒容,測得反應達到平衡時的有關數據如下:
容器 | 甲 | 乙 | 丙 |
反應物投入量 | 1molCO、2molH2 | 1molCH3OH | 2molCO、4molH2 |
CH3OH的濃度(mol/L) | c1 | c2 | c3 |
反應的能量變化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
①容器內壓強P:P甲、P乙與P丙的關系是______(用“>”、“<”或“=”表示);
②變化的熱量數值Q中,Q1與Q2的和是______(填具體數值).
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氯氣可用于制取漂白劑和自來水消毒。
(1)將氯氣通入水中制得氯水,氯水可用于漂白,其中起漂白作用的物質是 __________(填寫
化學式)。
(2)“84”消毒液也可用于漂白,其工業制法是控制在常溫條件下,將氯氣通入NaOH溶
液中,反應的離子方程式為__________。
(3)同學們探究“84”消毒液在不同pH下使紅紙褪色的情況,做了如下實驗:
步驟1:將5mL市售“84”消毒液稀釋100倍,測得稀釋后溶液的pH=12;
步驟2:取稀釋后溶液各20 mL分別加入3個潔凈的小燒杯中;
步驟3:用硫酸將3個燒杯內溶液的pH分別調至10、7和4。(溶液體積變化忽略不計)
步驟4:在3個燒杯中分別放入大小相同的紅紙,觀察現象,記錄如下:
燒杯 | 溶液的pH | 現象 |
a | 10 | 10 min后,紅紙基本不褪色;4h后紅紙褪色 |
b | 7 | 10 min后,紅紙顏色變淺;4 h后紅紙褪色 |
c | 4 | 10 min后,紅紙顏色變得更淺;4h后紅紙褪色 |
已知,溶液中Cl2、HC1O和ClO-物質的量分數(α) 隨pH變化的關系如右圖所示:
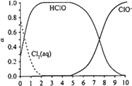
①由實驗現象可獲得以下結論:溶液的pH在4 ~10范圍內,pH越大,紅紙褪色________。
②結合圖像進行分析,b、c兩燒杯中實驗現象出現差異的原因是________。
(4)由于氯氣會與自來水中的有機物發生反應,生成對人體有害的物質,人們嘗試研究并使用新的自來水消毒劑,如ClO2氣體就是一種新型高效含氯消毒劑。
①一種制備ClO2的方法是將SO2通入硫酸酸化的NaC1O3溶液中,反應的離子方程式為__________。
②另一種制備ClO2的方法是用NaClO3與鹽酸反應,同時有Cl2生成,產物中Cl2體積約占1/3。則每生成0.5 mol ClO2,轉移__________mole-。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一密閉容器中有HCHO、H2和O2混合氣體共20g,放入足量Na2O2用電火花引燃,使其完全反應,Na2O2增重8g,則原混合氣體中O2的質量分數是
A. 40% B. 33.3% C. 60% D. 36%
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com