研究性學習小組同學選擇“過氧化氫生成氧氣的快慢與什么因素有關”的課題進行探究.以下是他們探究的主要過程:
【假設】過氧化氫生成氧氣的快慢與催化劑有關.
【實驗方案】常溫下,在兩瓶相同體積的過氧化氫溶液中分別加入相同質量的二氧化錳和紅磚粉,測量各生成一瓶(相同體積)氧氣所需的時間.
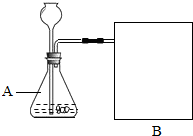
【進行記錄】下圖是他們進行實驗的裝置圖.此實驗中a處宜采用的氣體收集方法是排水法,并補充完整裝置圖.
【實驗記錄】
| 實驗編號 |
1 |
2 |
| 反應物 |
6%H2O2 |
6%H2O2 |
| 催化劑 |
1g MnO2 |
1g 紅磚粉 |
| 時間 |
35s |
152s |
【結論】該探究過程得出的結論是
在相同條件下,過氧化氫溶液生成氧氣的快慢與催化劑種類有關
在相同條件下,過氧化氫溶液生成氧氣的快慢與催化劑種類有關
.
【反思】過氧化氫在常溫下分解緩慢,加入二氧化錳或紅磚粉后反應明顯加快,若要證明二氧化錳和紅磚粉是該反應的催化劑,還需增加實驗來驗證它們在化學反應前后的
質量
質量
和
化學性質
化學性質
是否改變.
過氧化氫生成氧氣的快慢還與哪些因素有關?請你幫助他們繼續探究.(只要求提出假設和實驗方案)
【假設】
過氧化氫溶液的濃度能夠影響反應的速率
過氧化氫溶液的濃度能夠影響反應的速率
.
【實驗方案】
在溫度、相同質量的相同催化劑的條件下,采用等質量但不同的濃度的過氧化氫溶液來進行實驗,然后測量收集相同體積的氣體所需的時間
在溫度、相同質量的相同催化劑的條件下,采用等質量但不同的濃度的過氧化氫溶液來進行實驗,然后測量收集相同體積的氣體所需的時間
.

